Fonction de reproduction et différences entre espèces
2011
| ANALYSE |
11-
Fonctionnement des testicules
La spermatogenèse et la spermiogenèse sont les processus cellulaires qui produisent des cellules sexuelles mâles matures. Ces processus ont lieu dans les tubes séminifères des testicules de l’homme pubère, comme le montre la figure 11.1 . La maturation épididymaire, se déroulant lors du transit des spermatozoïdes dans l’épididyme, est indispensable pour l’obtention d’un gamète mature physiologiquement fonctionnel.
. La maturation épididymaire, se déroulant lors du transit des spermatozoïdes dans l’épididyme, est indispensable pour l’obtention d’un gamète mature physiologiquement fonctionnel.
 . La maturation épididymaire, se déroulant lors du transit des spermatozoïdes dans l’épididyme, est indispensable pour l’obtention d’un gamète mature physiologiquement fonctionnel.
. La maturation épididymaire, se déroulant lors du transit des spermatozoïdes dans l’épididyme, est indispensable pour l’obtention d’un gamète mature physiologiquement fonctionnel.Spermatogenèse
La spermatogenèse se déroule chez l’homme au sein des tubules séminifères et est un phénomène continu chez l’homme adulte. Schématiquement, le testicule peut être divisé en deux compartiments : le compartiment tubulaire où se déroule la spermatogenèse et le compartiment interstitiel, situé entre les tubules séminifères.
Dans le compartiment interstitiel vont être retrouvés plusieurs éléments cellulaires dont les cellules de Leydig qui sont à l’origine de la sécrétion de testostérone, hormone, qui permettra la masculinisation de l’individu et notamment le développement des organes androgéno-dépendants, l’acquisition et le maintien des caractères sexuels secondaires. D’autres éléments cellulaires vont également être retrouvés dans le compartiment interstitiel comme des macrophages, des précurseurs de cellules de Leydig ou des cellules péritubulaires disposées contre le tubule séminifère. Enfin, des capillaires lymphatiques peuvent être mis en évidence ainsi que des capillaires sanguins, à endothélium continu, capillaires qui participent à la barrière hémo-testiculaire.
Dans le compartiment tubulaire, deux grands types de cellules vont être retrouvés : les cellules de Sertoli et les cellules de la lignée germinale.
 | Figure 11.1 Schéma du testicule et de l’épididyme, lieux de la spermatogenèse et de la maturation du gamète mâle, chez l’homme |
Les cellules de Sertoli sont de grandes cellules à noyaux encochés qui vont de la membrane basale à la lumière du tube séminifère. Ce sont les cellules de soutien de la spermatogenèse et le nombre de cellules de Sertoli serait un élément important en relation avec le nombre de gamètes produit chez l’homme. Ces cellules de Sertoli acquièrent un caractère différencié à la puberté, elles sont non seulement les cellules de soutien mais également les cellules nourricières de la spermatogenèse notamment de par le nombre de facteurs de croissances sécrétés, de par les contacts physiques avec les cellules germinales. Elles ont un rôle essentiel dans les régulations paracrines (dans le testicule) mais également endocrines (hors testicule, par exemple sur l’hypophyse). Enfin les cellules de Sertoli participent grâce aux jonctions serrées au pôle basal du tube séminifère, à la barrière hémo-testiculaire.
Les cellules germinales sont composées de trois grandes catégories de cellules correspondant à des phases de la spermatogenèse. La phase de division implique les spermatogonies et permet la continuité de la spermatogenèse chez l’adulte. La phase de méiose concerne les spermatocytes et permet la création de cellules haploïdes et le brassage génétique. Enfin, pendant la phase de différenciation, la spermatide va subir un processus majeur de différenciation aboutissant au spermatozoïde.
Phase de division
La phase de division met en jeu les spermatogonies qui sont des cellules diploïdes (2n chromosomes) sièges de divisions cellulaires classiques. Il existe trois sortes de spermatogonies selon leur degré de différenciation ou de division : Ad, noyau sombre (dark), cellule souche de la spermatogenèse, en contact avec la membrane basale ; Ap, noyau pâle, sans vacuole nucléaire qui par mitose donne des spermatogonies B ; B, noyau à chromatine en agrégat périphérique, contact avec membrane basale moins important que pour Ad ou Ap. Chez l’homme adulte, les spermatogonies Ad peuvent être considérées comme des cellules souches de la spermatogenèse ; elles sont quiescentes et ne rentrent en division probablement que s’il existe un déficit cellulaire en aval. Elles peuvent se diviser pour donner des spermatogonies Ap. Les spermatogonies Ap vont se diviser pour donner deux Ap ou pour donner deux spermatogonies B. On estime qu’elles donnent une B tous les 16 jours. Les spermatogonies B se divisent et donnent les spermatocytes I. Le fait que les spermatogonies Ad se divisent en Ap fait qu’il existe un véritable renouvellement de ces cellules permettant ainsi un maintien continu de la spermatogenèse. Ces cellules sont situées dans le compartiment basal du tube séminifère, les Ad et Ap étant en contact étroit avec la membrane basale.
Phase de méiose
La phase de méiose met en jeu les spermatocytes. Le spermatocyte I issu de la division des spermatogonies B est le siège, pendant la période qui précède la prophase de la première division de la méiose, d’une activité de synthèse très importante qui se traduit par une augmentation du cytoplasme et un doublement de la qualité d’ADN (2n chromosomes, 4ADN). Cette cellule (parfois appelé auxocyte) est la plus volumineuse de la spermatogenèse observée sur les coupes tissulaires. Elle est le siège de la première division de la méiose, la mitose réductionnelle qui entraîne la séparation des chromosomes homologues appariés, pour aboutir au spermatocyte II, cellule haploïde ayant n chromosomes mais 2ADN. Ce spermatocyte est rapidement le siège de la mitose équationnelle de la méiose qui va avoir pour résultat une cellule haploïde à n chromosomes et n ADN : la spermatide.
Phase de différenciation
La phase de différenciation appelée spermiogenèse, concerne la spermatide qui est une cellule ronde issue de la mitose équationnelle de la méiose. Cette cellule ronde subit une différenciation très poussée, avec notamment plusieurs événements d’importance. Il s’agit tout d’abord de la mise en place de l’acrosome, à partir de la confluence de vésicules sécrétées par l’appareil de Golgi, qui va venir recouvrir les deux tiers antérieurs du noyau. Pendant la transformation nucléaire, les histones sont remplacées par des protéines de transition puis par des protamines, ce qui va avoir pour conséquences une extrême compaction du matériel nucléaire et une protection du génome. Les histones représenteront, dans le spermatozoïde, seulement 20 % environ des protéines nucléaires. Il est à noter lors de ces déplacements, l’induction de cassures dans l’ADN qui doivent être réparées pour avoir un génome normal. Par ailleurs, le noyau du spermatozoïde va acquérir une forme spécifique de l’espèce.
Se produit ensuite la mise en place du flagelle, l’axonème du flagelle ayant pour origine le centriole distal, le centriole proximal qui joue un rôle après la fécondation se situant juste en dessous de la pièce connective assurant la cohésion entre la tête et le flagelle du spermatozoïde. Puis un manchon de mitochondrie se met en place au niveau de la pièce intermédiaire du flagelle. Enfin, la plus grande partie du cytoplasme est phagocytée par la cellule de Sertoli lors de la spermiation c’est-à-dire la libération du spermatozoïde dans la lumière du tubule séminifère.
Plusieurs points doivent être soulignés :
• la continuité de la spermatogenèse chez l’adulte grâce au renouvellement des spermatogonies Ap ;
• la durée de la spermatogenèse spécifique de l’espèce, elle est chez l’homme de 74 jours ;
• l’existence de ponts intercytoplasmiques entre les populations cellulaires ;
• l’existence de cellules souches quiescentes, les spermatogonies Ad, pouvant être réactivées ;
• la nécessité du transit épididymaire qui a une importance majeure en physiologie car c’est lors du transit épididymaire que le spermatozoïde va achever sa maturation.
Il est dès lors compréhensible qu’une altération de la physiologie épididymaire, par un facteur environnemental, peut avoir des conséquences sur les fonctions du spermatozoïde pouvant avoir un effet y compris sur le développement embryonnaire.
Enfin, le dernier point concerne la barrière hémo-testiculaire qui est constituée par la paroi non fenêtrée des capillaires, les cellules péri-tubulaires, la membrane basale du tubule séminifère et la cellule de Sertoli au niveau des jonctions. Cette barrière a un rôle sélectif et protège par là même les cellules haploïdes qui sont situées dans le compartiment adluminal du tubule séminifère.
Contrôle neuro-endocrinien de la fonction testiculaire
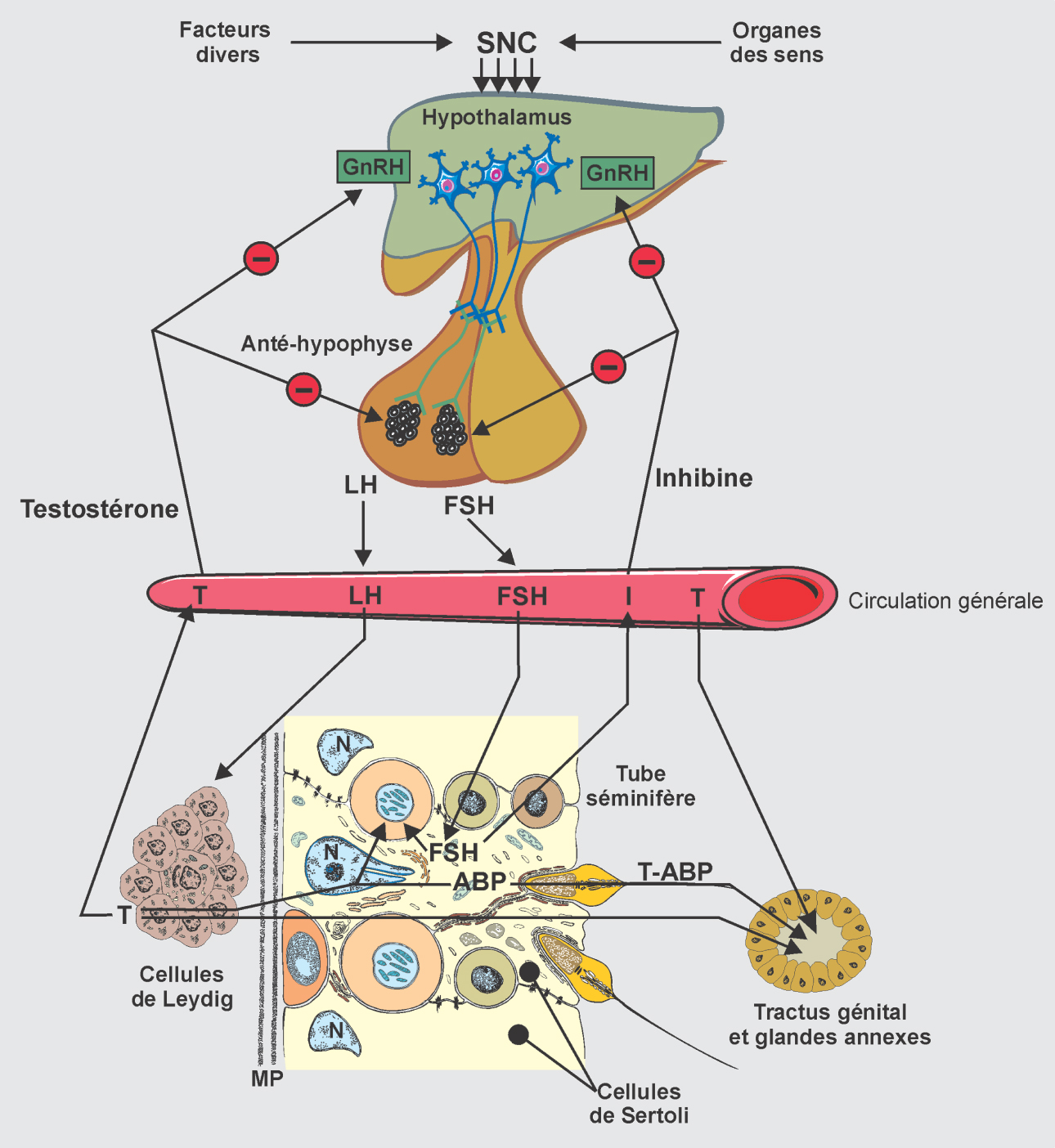
Le « chef d’orchestre » de la fonction testiculaire est la production pulsatile de GnRH (Gonadotropin Releasing Hormone) par des neurones de l’hypothalamus, production très augmentée à la période pubertaire, alors que s’installe la fonction testiculaire. La GnRH provoque la sécrétion hypophysaire, elle-même pulsatile, de deux hormones, la FSH et la LH (figure 11.2 ).
).
 ).
).Schématiquement, la FSH, en association avec la testostérone, permet le développement des cellules de Sertoli et la spermatogenèse donc la fonction exocrine du testicule (excrétion des spermatozoïdes) alors que la LH assure la multiplication des cellules de Leydig et la sécrétion de testostérone, fonction endocrine du testicule.
La stéroïdogenèse est commandée par la LH qui se fixe sur des récepteurs membranaires des cellules de Leydig ; les cellules de Leydig sécrètent alors des androgènes, essentiellement de la testostérone (T) ; la testostérone pénètre dans le compartiment tubulaire où elle se lie à une glycoprotéine de liaison, l’ABP (Androgen Binding Protein) pour conditionner le développement de l’épithélium séminal et le bon fonctionnement des voies génitales ; la testostérone libre passe dans le sang et exerce deux actions : une action positive sur le tractus génital et les glandes annexes et principalement après action de l’aromatase et transformation en œstradiol, un rétrocontrôle sur la sécrétion de LH et FSH, soit indirectement sur les neurones hypothalamiques, soit directement sur les cellules gonadotropes hypophysaires.
La FSH se fixe sur des récepteurs membranaires des cellules de Sertoli et joue un triple rôle : elle active la spermatogenèse par l’intermédiaire du cytoplasme sertolien ; elle stimule la formation d’ABP et provoque la sécrétion d’inhibine, hormone exerçant un rétrocontrôle négatif sur la sécrétion de FSH, soit sur les neurones hypothalamiques en diminuant la sécrétion de la GnRH, soit directement sur les cellules gonadotropes hypophysaires.
Il existe également des sécrétions autocrines – la sécrétion de la testostérone exerce une rétro-inhibition sur l’activité des enzymes de la stéroïdogenèse à l’intérieur de la cellule de Leydig – et des sécrétions paracrines entre la cellule de Sertoli et la cellule de Leydig. La testostérone peut être aromatisée en œstradiol dans la cellule de Sertoli, l’œstradiol inhibera par voie paracrine la sécrétion de testostérone dans la cellule de Leydig (et par voie endocrine la sécrétion de FSH).
Comme tous les organes, les testicules, les voies génitales et les glandes annexes sont sous double contrôle, hormonal (neuro-endocrinien) et nerveux (système nerveux sympathique).
Régulation thermique
Chez les mammifères, une spermatogenèse normale nécessite une hypothermie physiologique : la température des testicules doit être plus basse que la température corporelle. Chez l’homme, une température testiculaire d’environ 33-35 °C permet un fonctionnement optimal de la spermatogenèse. Cette hypothermie relative (euthermie testiculaire) est maintenue grâce au système vasculaire particulier qui permet, par des échanges thermiques à contre courant, un refroidissement du sang artériel arrivant au testicule et également grâce au système scrotal, qui par ces capacités d’adaptation, va permettre les échanges entre le scrotum et le milieu extérieur et ainsi refroidir le contenu scrotal. Par ailleurs, il faut noter que l’épididyme est également un organe thermosensible nécessitant un environnement thermique abaissé. Les conséquences d’une élévation de la température épididymo-testiculaire ont été étudiées chez l’animal et l’homme. Chez l’homme, une faible augmentation de la température (n’atteignant toutefois pas la température corporelle) a pour conséquence une altération quantitative de la spermatogenèse, diminution majeure de la quantité de spermatozoïdes produits avec à l’extrême une azoospermie, mais également une altération qualitative de la spermatogenèse (Mieusset et Bujan, 1995 ).
).
 ).
).Cette notion de thermodépendance de la fonction épididymo-testiculaire concernant la production des gamètes et leur qualité doit être bien connue d’autant plus que les perturbations des systèmes de régulation thermique, certaines habitudes de vie ou l’exposition professionnelles à des sources de chaleur peuvent modifier l’équilibre thermique qui permet un fonctionnement optimal.
Bibliographie
[1] MIEUSSET R, BUJAN L. Testicular heating and its possible contributions to male infertility: a review.
Int J Androl. 1995;
18:169- 184

→ Aller vers SYNTHESE