L’acrodermatite entéropathique (AE) est un syndrome héréditaire rare de déficience en zinc, transmis selon un mode autosomique récessif. Apparaissant dès la naissance ou au moment du sevrage [ 1], l’AE se définit théoriquement par la présence de trois symptômes pathognomoniques une dermatite acrale (des extrémités) et péri-orificielle, une diarrhée et une alopécie [ 2]. Ces symptômes sont la conséquence précoce d’une déficience nutritionnelle en zinc due à une malabsorption dans le duodénum et le jéjunum. Le corps humain ne possédant pas de véritable réserve de zinc, la déficience s’étend rapidement à tout l’organisme et se manifeste par un tableau clinique extrêmement vaste, reflétant le rôle physiologique crucial de cet oligo-élément si aucun traitement n’est apporté, le manque de zinc conduit à terme à une défaillance organique généralisée et, finalement, à la mort de l’individu [2]. L’importance d’un diagnostic correct est donc d’autant plus grande que, lorsqu’il est posé, une simple supplémentation orale quotidienne de zinc permet de faire disparaître tous les symptômes en quelques jours.
En 2002, nous avons cloné un nouveau gène, SLC39A4, dont les caractéristiques nous ont suggéré son rôle déterminant dans la pathogénie de l’AE [ 3]. Nous avons ainsi observé que SLC39A4 se localisait dans le locus chromosomique de susceptibilité à l’AE déterminé par K. Wang et al. en 8q24.3 [ 4], qu’il était exprimé dans le duodénum et le jéjunum - les deux sites intestinaux incriminés dans l’AE [1, 5] - et qu’il codait pour une protéine dont la structure est fortement homologue avec celle des transporteurs membranaires connus pour absorber le zinc dans la cellule (Figure 1). De plus, tous les patients atteints d’AE alors inclus dans l’étude présentaient des mutations délétères de SLC39A4, la coségrégation se révélant parfaite entre le génotype et le phénotype au sein des familles des patients [3]. Une étude parallèle confirmait l’altération de SLC39A4 pour d’autres familles atteintes d’AE et révélait que, chez la souris, la protéine Slc39a4 était exprimée sur la face apicale des entérocytes des villosités intestinales, précisément là où s’effectue l’absorption du zinc [ 6].
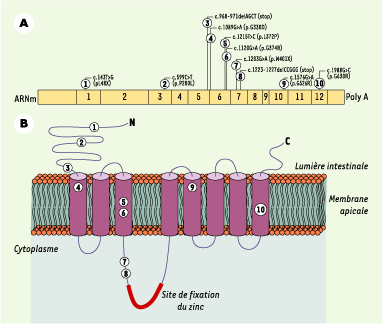
| Figure 1. Mutations délétères du gène SLC39A4 observées chez des patients atteints d’acrodermatite entéropathique. A. Localisation dans la séquence ARNm de mutations tronquantes (1, 3, 7 et 8) et faux-sens validées par expression cellulaire in vitro (2, 4, 5, 6, 9 et 10). B. Localisation des mutations protéiques correspondantes dans la structure secondaire du transporteur Slc39a4. |
Récemment, la fonction d’absorption spécifique du zinc par Slc39a4 a été prouvée expérimentalement par la transfection de son ARNm dans des modèles cellulaires aussi différents que des cellules embryonnaires humaines et des ovocytes de xénope [ 7] (S. Küry et N. Ford, données non publiées). Des études in vivo chez la souris ont montré, quant à elles, que l’activité de transport de Slc39a4 dans l’intestin grêle est inversement proportionnelle à la richesse en zinc des nutriments. Lorsque l’apport alimentaire est carencé en zinc, les transcrits ARNm entérocytaires de SLC39A4 augmentent et les nombreuses protéines synthétisées se localisent majoritairement dans la membrane apicale (Figure 2). Au contraire, un excès de zinc provoque une diminution de la transcription et une séquestration des protéines Slc39a4 par endocytose dans des compartiments intracellulaires [7].
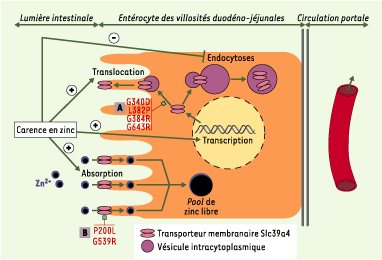
| Figure 2. Physiopathologie de l’absorption entérocytaire du zinc par Slc39a4. L’activité de transport de zinc par Slc39a4, inversement proportionnelle à la concentration de zinc des aliments, résulte de la modulation du contrôle des phénomènes activateurs (transcription de SLC39A4 et translocation membranaire vers la surface apicale) et inhibiteurs (endocytose vésiculaire intracytoplasmique). Les mutations faux-sens présentées par des patients atteints d’acrodermatite entéropathique entraînent des altérations soit de la glycosylation de Slc39a4 (A), ce qui empêche sa translocation membranaire, soit de sa conformation, ce qui inhibe sa fonction de transporteur de zinc (B). |
La régulation fine de SLC39A4 en fonction des apports alimentaires de zinc suggère le rôle prépondérant de ce gène dans l’homéostasie du zinc, justement en cause chez les patients atteints d’AE. Or, des expériences d’expression fonctionnelle cellulaire ont démontré que les mutations faux-sens observées chez ces patients induisent une diminution d’absorption du zinc par Slc39a4 (Figure 2) [ 8] (S. Küry et N. Ford, données non publiées) certaines empêchent la localisation de Slc39a4 dans la membrane apicale en altérant sa glycosylation protéique, tandis que d’autres affectent sa conformation fonctionnelle [8]. Ainsi, la preuve est désormais faite du lien de causalité existant entre les anomalies de SLC39A4 et l’AE.
La caractérisation du gène codant pour l’AE nous a servi à mettre au point un test moléculaire de SLC39A4 pour la détection des porteurs de mutations au sein des familles à risque, afin de pouvoir proposer un traitement précoce aux malades. Si le dépistage prénatal ne s’impose pas réellement, l’intérêt du test parental est, en revanche, accru dans les familles consanguines, en particulier celles de l’Afrique du Nord où la prévalence de l’AE est relativement forte. En pratique, ce test génétique devrait constituer une aide précieuse au diagnostic de l’AE, que la clinique seule ne permet souvent pas d’établir avec confiance en raison de tableaux cliniques incomplets, ou au contraire trop complexes [ 9]. D’après les résultats obtenus pour une quarantaine de patients, l’efficacité de ce test s’avère remarquable puisque, chez près de 90 des individus examinés, nous avons retrouvé des mutations délétères de SLC39A4 [ 10].
Sur un plan fondamental, certains résultats étonnants de ce test nous amènent à considérer l’existence possible d’un second gène impliqué dans l’AE. Celui-ci pourrait avoir un rôle essentiel dans la pathogénie des 10 environ de cas d’AE apparemment non liés à SLC39A4. Des mutations de ce second gène pourraient également potentialiser l’effet délétère de celles de SLC39A4, expliquant ainsi l’AE sévère de quelques patients chez lesquels nous n’avons identifié qu’une mutation hétérozygote de SLC39A4 [10]. Il n’est pas non plus exclu que cet autre gène soit à l’origine de l’acrodermatite-like, un syndrome dans lequel le nourrisson allaité par sa mère présente des symptômes cliniques identiques à l’AE. Dans ce cas, la mère présente un déficit de transport de zinc dans le lait, à l’origine de la déficience en zinc de son enfant. Par analyse mutationnelle, nous avons montré que le gène responsable n’était ni SLC39A4, ni SLC30A4 - le gène incriminé dans le syndrome murin orthologue lethal milk. Or, nous avons observé que des mutations hétérozygotes de SLC39A4 pouvaient exceptionnellement induire une carence en zinc du lait maternel [9]. Cela suggère par conséquent que l’acrodermatite-like et les formes d’AE non liées à SLC39A4 pourraient avoir une origine génétique commune. De toute évidence, l’identification de ce second gène constitue la prochaine étape décisive de la recherche sur l’AE elle devrait permettre à la fois d’améliorer la fiabilité du test diagnostique de l’AE et mieux comprendre la remarquable efficacité de la supplémentation en zinc chez les patients touchés par cette affection.