Salmonella enterica est une bactérie pathogène causant une variété de maladies chez l’homme et l’animal. Spécifique à l’homme, le serovar Typhi est l’agent étiologique de la fièvre typhoïde, une infection systémique dont on évalue les ravages à quelque 16 millions de nouveaux cas et à plus de 600 000 morts par année. La crainte de travailler avec cette bactérie très pathogène et l’absence d’un modèle animal adéquat compliquent l’étude des mécanismes de virulence de Typhi. En fait, la majorité des connaissances sur Typhi proviennent d’extrapolations à partir d’études utilisant Typhimurium, un serovar apparenté, dans un modèle murin de fièvre typhoïde.
La survie de Salmonella dans les macrophages est conditionnelle à l’expression de plusieurs gènes qu’il importe d’identifier pour prévenir et guérir les infections causées par cette bactérie. Les biopuces sont couramment utilisées pour déterminer le profil global d’expression génique dans des conditions qui miment l’infection. Cependant les limites intrinsèques de cette approche ne permettent pas l’identification des gènes bactériens exprimés in vivo. Les facteurs limitants comprennent la faible quantité d’ARN bactérien et la courte demi-vie de l’ARNm non polyadénylé qui, de plus, se retrouve mélangé avec l’ARNr et l’ARN provenant de l’hôte. Quant à elle, la technique SCOTS (selective capture of transcribed sequences) permet l’identification de gènes bactériens exprimés dans les cellules de l’hôte par clonage et séquençage des transcrits [ 1]. Nous avons récemment réussi à combiner les qualités de ces deux approches [ 2]. En effet, les transcrits bactériens obtenus par la technique SCOTS ont été utilisés en conjonction avec les biopuces, ce qui nous a permis d’obtenir le profil global d’expression génique de la bactérie à partir de macrophages humains infectés [2].
Grâce à la technique SCOTS, l’ARN total de macrophages humains THP-1 infectés a été isolé et converti en ADNc contenant les amorces spécifiques par transcriptase inverse. Cet ADNc initial contient un mélange correspondant à l’ARN eucaryote et procaryote. L’ADNc bactérien de ce mélange a été capturé par hybridation avec l’ADN génomique bactérien et ensuite amplifié grâce aux amorces spécifiques. Dans notre cas, trois cycles de capture ont été effectués. L’ADNc provenant de chacune de ces étapes a été marqué et utilisé pour l’hybrider à des biopuces de Salmonella [ 3]. Nos résultats indiquent qu’une faible proportion des transcrits provenant de l’ADNc initial présentent un signal assez fort pour être détectés (Figure 1). Ces résultats démontrent le peu de sensibilité obtenu lorsque l’ADNc initial est utilisé et confirment les limites d’identification directe de transcrits bactériens durant l’infection. En revanche, le nombre de gènes détectés augmente avec les cycles successifs de la méthode SCOTS (Figure 1). Ainsi, nous avons confirmé que la complexité de l’ADNc obtenu par la technique SCOTS était suffisante pour obtenir le transcriptome bactérien in vivo.
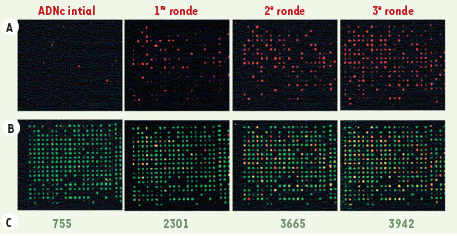
| Figure 1.
Reproduction d’une portion des biopuces hybridées avec l’ADNc initial ou l’ADNc capturé avec SCOTS, provenant de macrophages infectés 2 heures après la phagocytose (T2). A. ADNc seulement marqué avec le fluorochrome Cy5 (rouge).B. ADNc et ADN génomique marqué avec le fluorochrome Cy3 (vert). C. Nombre de gènes détectés (signal plus grand que celui du bruit de fond). |
Nous avons donc utilisé la technique SCOTS pour obtenir de l’ADNc de Typhi à partir du surnageant de macrophages infectés, après la phagocytose (T0), à 2h (T2), 8h (T8) et 24h (T24) post-infection [2]. Nous avons mis en évidence une différence d’expression significative de 36 % du génome de Typhi, la répression de 138 gènes et l’induction de 117 gènes, comparés au surnageant de culture. Parmi les gènes induits, plusieurs facteurs de virulence connus ont été identifiés, corroborant nos résultats, ainsi que plusieurs gènes aux fonctions inconnues, qui pourraient correspondre à de nouveaux facteurs de virulence. Les résultats de biopuces ont été confirmés en quantifiant l’expression de certains gènes par PCR quantitatif en temps réel [ 4].
Le chromosome de Salmonella possède plusieurs insertions de larges régions d’ADN qui contiennent des gènes de virulence que l’on nomme îlots de pathogénicité (SPI). Les SPIs jouent un rôle clé dans la pathogenèse de Salmonella. SPI-1 et SPI-2 codent pour deux systèmes de sécrétion de type trois ayant des rôles différents : SPI-1 participe à l’invasion tandis que SPI-2 contribue à la survie intracellulaire [ 5]. Chez Typhi, les gènes de SPI-1 ont été identifiés comme étant induits au début de l’infection (T0) et, par la suite, réprimés pour le reste de l’infection (Figure 2). Les gènes de SPI-2 sont induits au début de l’infection, ainsi que pour toute la durée de l’infection (Figure 2). Ces résultats concordent avec le rôle biologique de ces SPI et valident nos résultats.
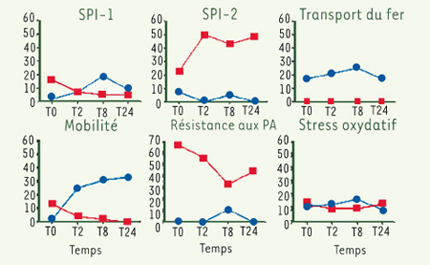
| Figure 2.
Analyse de l’expression de gènes regroupés selon leur fonction. Nombre de gènes (%), dans chacune des classes, qui sont significativement induits (courbe rouge) ou réprimés (courbe bleue) (p < 0,001, changement d’expression de plus de 2 fois par rapport au surnageant). PA : peptides antimicrobiens. |
De plus, Typhi répond fortement aux peptides antimicrobiens (PA) présents à l’intérieur de la vacuole des macrophages en induisant les gènes de résistance qui modifient les lipopolysaccharides de la membrane bactérienne (Figure 2). Les gènes participant à la mobilité, ainsi qu’au transport du fer, un élément essentiel à la croissance des bactéries, sont réprimés chez Typhi lors de l’infection, suggérant que le fer est disponible dans la vacuole (Figure 2). Il n’y a pas eu de différence dans l’expression des gènes prenant part au stress oxydatif (Figure 2).
La comparaison des transcriptomes de Typhi et Typhimurium (récemment publié [ 6]) a révélé certaines différences. L’induction constitutive du régulateur transcriptionnel de gènes de virulence PhoP est observée chez Typhi durant l’infection ; en revanche, il n’y a pas de différence d’expression chez Typhimurium. Contrairement à Typhimurium qui utilise le gluconate comme source de carbone, Typhi semble plutôt se servir des acides gras. Effectivement, le gène aceA codant pour l’isocitrate lyase, une enzyme permettant l’utilisation des acides gras via le cycle du glyoxylate, est induit à partir de 8 h post-infection, tandis qu’il n’est pas induit chez Typhimurium 12 h post-infection.
En conclusion, notre étude a démontré que l’utilisation de la technique SCOTS et des biopuces permet d’obtenir le transcriptome d’une bactérie intracellulaire dans des conditions normales d’infection. Le transcriptome de Typhi à partir de macrophages infectés a ainsi été obtenu et manifeste un profil attendu pour les gènes de virulence. La caractérisation de certains gènes inconnus exprimés durant l’infection sera importante pour élucider les mécanismes de pathogénie de Typhi, ouvrant la voie au développement d’une meilleure approche préventive et thérapeutique.