Cancer
Personnaliser le traitement
La Journée mondiale contre le cancer, le 4 février, est l’occasion de faire le point sur les stratégies de lutte développées par les chercheurs. Médecine personnalisée et génomique ont le vent en poupe.
Prendre en compte les caractéristiques d’un patient et celles de sa tumeur afin de proposer le traitement le plus adapté, c’est l’adage de la médecine personnalisée. « Peut-on donc, pour chaque patient, reconstruire les anomalies moléculaires des cellules qui ont abouti à la formation d’une tumeur ? C’est la question à laquelle cette nouvelle médecine doit répondre », formalise Fabrice AndréFabrice André
Unité 981 Inserm/ Paris 11, Biomarqueurs prédictifs et nouvelles stratégies moléculaires en thérapeutique anticancéreuse, cancérologue et chercheur en pathologie mammaire à l’Institut Gustave-Roussy. Pour cela, plusieurs obstacles doivent être surmontés.
Unité 981 Inserm/ Paris 11, Biomarqueurs prédictifs et nouvelles stratégies moléculaires en thérapeutique anticancéreuse, cancérologue et chercheur en pathologie mammaire à l’Institut Gustave-Roussy. Pour cela, plusieurs obstacles doivent être surmontés.
L’aide du "virtuel"
D’abord, cette approche personnalisée est-elle techniquement réalisable ? La logistique à déployer est de fait impressionnante : on doit prélever un échantillon de la tumeur, le traiter de façon adéquate, procéder à une analyse génomique puis étudier les résultats. Les techniques de haut-débitTechniques de haut-débit
Elles permettent d’étudier à très grande échelle la structure du génome. auxquelles il faut faire appel existent bel et bien mais elles sont utilisées par les chercheurs dans leur laboratoire. Peut-on s’en servir en routine pour la prise en charge des malades ? « C’est possible en France grâce à notre modèle de soins, explique Fabrice André. Une vingtaine de centres de lutte contre le cancer disposant d’un plateau technique opérationnel sont d’ailleurs unis dans cette action. » Ensuite, on doit identifier des biomarqueurs et des cibles thérapeutiques. « Nous devons trouver les anomalies à l’origine de la progression tumorale. C’est un peu un travail d’archéologue, où l’on doit remonter le fil des événements. » L’informatique est alors d’une grande aide pour créer des outils, qui, au milieu d’une multitude d’événements génomiques (mutations, répétitions de séquences…), vont pouvoir identifier les plus importants. « Nous sommes en train de développer un logiciel qui reproduit, de façon virtuelle, le fonctionnement d’une cellule. Une fois les anomalies rentrées dans ce programme, on pourra alors vérifier ce qui se produit dans la cellule. » Enfin, il s’agit bien sûr de trouver un médicament adapté. Si l’on ne s’intéresse qu’à un seul aspect de la tumeur, c’est assez « facile ». Exemple avec l’herceptine, mise sur le marché européen dès l’an 2000. Dans certains types de cancer du sein, les cellules tumorales surexpriment à leur surface un récepteur HER2, qui contrôle en partie leur croissance. L’herceptine injectée va se fixer sur ces récepteurs et bloquer ainsi leur action. « Mais lorsqu’on prend en compte plusieurs anomalies, la tâche se complique, souligne le chercheur. Il y a trop peu de patients concernés présentant les mêmes caractéristiques. Et on ne peut pas les réunir en cohorte pour développer des essais cliniques et tester l’efficacité des molécules. C’est là que l’élaboration d’une cellule virtuelle, dans laquelle on peut rentrer toutes ces données, devient essentielle. » On teste alors un panel de molécules pour trouver celles aux meilleurs effets thérapeutiques.
Elles permettent d’étudier à très grande échelle la structure du génome. auxquelles il faut faire appel existent bel et bien mais elles sont utilisées par les chercheurs dans leur laboratoire. Peut-on s’en servir en routine pour la prise en charge des malades ? « C’est possible en France grâce à notre modèle de soins, explique Fabrice André. Une vingtaine de centres de lutte contre le cancer disposant d’un plateau technique opérationnel sont d’ailleurs unis dans cette action. » Ensuite, on doit identifier des biomarqueurs et des cibles thérapeutiques. « Nous devons trouver les anomalies à l’origine de la progression tumorale. C’est un peu un travail d’archéologue, où l’on doit remonter le fil des événements. » L’informatique est alors d’une grande aide pour créer des outils, qui, au milieu d’une multitude d’événements génomiques (mutations, répétitions de séquences…), vont pouvoir identifier les plus importants. « Nous sommes en train de développer un logiciel qui reproduit, de façon virtuelle, le fonctionnement d’une cellule. Une fois les anomalies rentrées dans ce programme, on pourra alors vérifier ce qui se produit dans la cellule. » Enfin, il s’agit bien sûr de trouver un médicament adapté. Si l’on ne s’intéresse qu’à un seul aspect de la tumeur, c’est assez « facile ». Exemple avec l’herceptine, mise sur le marché européen dès l’an 2000. Dans certains types de cancer du sein, les cellules tumorales surexpriment à leur surface un récepteur HER2, qui contrôle en partie leur croissance. L’herceptine injectée va se fixer sur ces récepteurs et bloquer ainsi leur action. « Mais lorsqu’on prend en compte plusieurs anomalies, la tâche se complique, souligne le chercheur. Il y a trop peu de patients concernés présentant les mêmes caractéristiques. Et on ne peut pas les réunir en cohorte pour développer des essais cliniques et tester l’efficacité des molécules. C’est là que l’élaboration d’une cellule virtuelle, dans laquelle on peut rentrer toutes ces données, devient essentielle. » On teste alors un panel de molécules pour trouver celles aux meilleurs effets thérapeutiques.
Les tumeurs du foie séquencées
C’est dans la même optique que l’équipe de Jessica Zucman-RossiJessica Zucman-Rossi
Unité 674 Inserm/Paris 7, Génomique fonctionnelle des tumeurs solides, à l’hôpital Saint-Louis, s’attelle à cataloguer les tumeurs du foie. Dans le cadre du consortium international de génomique du cancer, piloté par l’Institut national du cancer, les chercheurs ont pour mission de séquencerSéquencer
Déterminer l’ordre linéaire des nucléotides de l’ADN d’une cellule tumorale. 500 tumeurs hépatiques. « Alors que celui du génome humain a pris une dizaine d’années, le séquençage d’une tumeur peut désormais se faire en 10 à 20 jours seulement. C’est l’évolution des technologies qui permet cette prouesse. » Les résultats préliminaires dévoilent surtout la complexité de l’accumulation des altérations génomiques. Jugez plutôt : pour une tumeur du foie, on compte entre 5 et 120 mutations ! « Chaque tumeur résulte d’une combinaison unique de mutations. » À terme bien sûr, les chercheurs espèrent pouvoir proposer des médicaments personnalisés en fonction des combinaisons d’anomalies.
Unité 674 Inserm/Paris 7, Génomique fonctionnelle des tumeurs solides, à l’hôpital Saint-Louis, s’attelle à cataloguer les tumeurs du foie. Dans le cadre du consortium international de génomique du cancer, piloté par l’Institut national du cancer, les chercheurs ont pour mission de séquencerSéquencer
Déterminer l’ordre linéaire des nucléotides de l’ADN d’une cellule tumorale. 500 tumeurs hépatiques. « Alors que celui du génome humain a pris une dizaine d’années, le séquençage d’une tumeur peut désormais se faire en 10 à 20 jours seulement. C’est l’évolution des technologies qui permet cette prouesse. » Les résultats préliminaires dévoilent surtout la complexité de l’accumulation des altérations génomiques. Jugez plutôt : pour une tumeur du foie, on compte entre 5 et 120 mutations ! « Chaque tumeur résulte d’une combinaison unique de mutations. » À terme bien sûr, les chercheurs espèrent pouvoir proposer des médicaments personnalisés en fonction des combinaisons d’anomalies.
Avec 5 000 nouveaux cas par an, en France, ces cancers sont bien moins fréquents que ceux du sein ou de la prostate. Malheureusement, ils sont très agressifs et souvent diagnostiqués tardivement. « Seuls 20 % des malades, au moment du diagnostic, ont accès à des thérapies à visée curative. Pour le moment, très peu de molécules ont prouvé leur efficacité. Mais les résultats d’essais cliniques prometteurs devraient bientôt être publiés. » La médecine personnalisée semble donc être un nouvel atout précieux de la cancérologie.
Julie Coquart
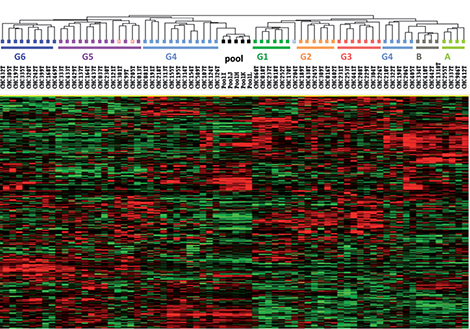
Ⓒ Jessica Zucman-Rossi/Unité 674 Inserm/Inserm
- ☞ Fabrice André :
- Unité 981 Inserm/ Paris 11, Biomarqueurs prédictifs et nouvelles stratégies moléculaires en thérapeutique anticancéreuse ⌆
- ☞ Jessica Zucman-Rossi :
- Unité 674 Inserm/Paris 7, Génomique fonctionnelle des tumeurs solides ⌆
