| dc.contributor.author | Bertin, Aurélie | - |
| dc.contributor.author | Mangenot, Stéphanie | - |
| dc.date.accessioned | 2014-08-13T07:20:58Z | |
| dc.date.available | 2014-08-13T07:20:58Z | |
| dc.date.issued | 2008 | fr_FR |
| dc.identifier.citation | Bertin, Aurélie ; Mangenot, Stéphanie ; Structure et dynamique de la particule cœur de nucléosome, Med Sci (Paris), 2008, Vol. 24, N° 8-9; p. 715-719 ; DOI : 10.1051/medsci/20082489715 | fr_FR |
| dc.identifier.issn | 1958-5381 | fr_FR |
| dc.identifier.uri | http://hdl.handle.net/10608/6502 | |
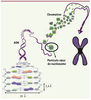
| dc.description.abstract | La chromatine, formée de l’enroulement d’ADN autour d’un cœur d’histones, s’organise suivant différents niveaux de compaction : de la particule cœur de nucléosome (NCP pour nucleosome core particle) à l’organisation en chromosomes dans le noyau. La structure du premier niveau d’organisation de la chromatine, la NCP, a été déterminée sans ambiguïté par cristallographie. L’organisation de la chromatine est dynamique et régulée par de nombreux facteurs pour que l’ADN soit accessible et la chromatine fonctionnelle. Notamment, des modifications post-traductionnelles des histones altèrent les charges de leurs extrémités amino- et carboxy- terminales et sont ainsi susceptibles de réguler le degré de compaction de la chromatine. Des facteurs de remodelage permettent également le glissement relatif de l’ADN autour des histones et augmentent son accessibilité | fr |
| dc.description.abstract | In eukaryotic cell, a few meters of DNA are compacted in nuclear compartment of a few microns. This high level of compaction is an important way to regulate gene expression. In the present paper, we present a description of the organization of DNA into its first level of compaction: the nucleosome core particle. The structure of the nucleosome has been described at an atomic resolution more than 10 years ago, where DNA is wrapped around an octamer of histones. Post-translational modifications affecting histone tails have been shown to regulate the chromatin degree of compaction and thus the gene expression and regulation. The structure of the NCP is far from being frozen and is highly dynamic. Remodeling factors can induce DNA sliding around the histones, DNA transaction processes such as transcription and replication. | en |
| dc.language.iso | fr | fr_FR |
| dc.publisher | EDK | fr_FR |
| dc.relation.ispartof | M/S revues | fr_FR |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [ISSN papier : 0767-0974 ; ISSN numérique : 1958-5381], 2008, Vol. 24, N° 8-9; p. 715-719 | fr_FR |
| dc.subject.mesh | Animaux | fr |
| dc.subject.mesh | Chromatine | fr |
| dc.subject.mesh | ADN | fr |
| dc.subject.mesh | Hétérochromatine | fr |
| dc.subject.mesh | Histone | fr |
| dc.subject.mesh | Humains | fr |
| dc.subject.mesh | Modèles moléculaires | fr |
| dc.subject.mesh | Conformation d'acide nucléique | fr |
| dc.subject.mesh | Nucléosomes | fr |
| dc.title | Structure et dynamique de la particule cœur de nucléosome | fr |
| dc.title.alternative | Structure and dynamic of the nucleosome core particle | en |
| dc.type | Article | fr_FR |
| dc.contributor.affiliation | University of California Berkeley, Molecular and Cellular Biology Department, Berkeley CA 94720-3220, États-Unis | fr_FR |
| dc.contributor.affiliation | Université Paris-Sud, 15, rue Georges Clémenceau, 91405 Orsay Cedex, France. | fr_FR |
| dc.contributor.affiliation | Institut Curie, UMR168-CNRS, 26, rue d’Ulm, 75248 Paris Cedex 05, France | fr_FR |
| dc.identifier.doi | 10.1051/medsci/20082489715 | fr_FR |
| dc.identifier.pmid | 18789217 | fr_FR |