| dc.contributor.author | Vidalain, Pierre-Olivier | - |
| dc.contributor.author | Lucas-Hourani, Marianne | - |
| dc.contributor.author | Helynck, Olivier | - |
| dc.contributor.author | Tangy, Frédéric | - |
| dc.contributor.author | Munier-Lehmann, Hélène | - |
| dc.date.accessioned | 2018-05-30T11:35:57Z | |
| dc.date.available | 2018-05-30T11:35:57Z | |
| dc.date.issued | 2015 | |
| dc.identifier.citation | Vidalain, Pierre-Olivier ; Lucas-Hourani, Marianne ; Helynck, Olivier ; Tangy, Frédéric ; Munier-Lehmann, Hélène ; Activation de la réponse innée antivirale par des inhibiteurs de la biosynthèse des pyrimidines : Les surprises d’un criblage phénotypique, Med Sci (Paris), 2015, Vol. 31, N° 1 ; p. 98-104 ; DOI : 10.1051/medsci/20153101019 | |
| dc.identifier.issn | 1958-5381 | |
| dc.identifier.uri | http://hdl.handle.net/10608/8554 | |
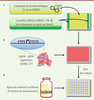
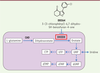
| dc.description.abstract | Les virus à ARN sont responsables de maladies graves telles que la grippe, la dengue, l’hépatite C, la rougeole ou la bronchiolite des nourrissons. Ils représentent également une menace émergente en raison des échanges internationaux et des bouleversements écologiques liés aux activités humaines. Notre compréhension des mécanismes cellulaires qui contrôlent la réplication virale a fortement progressé ces dernières années, et il apparaît que des composés capables de cibler la cellule hôte, plutôt que le virus lui-même, pourraient inhiber un large éventail de virus à ARN. Ainsi, différents laboratoires privés et universitaires sont en quête de molécules stimulant la réponse antivirale innée des cellules hôtes. Une stratégie intéressante consiste à rechercher des molécules induisant l’expression des ISG (interferon-stimulated genes), lesquels constituent un vaste ensemble de gènes antiviraux activés en particulier par les interférons de type I. Pour atteindre cet objectif, nous avons mis au point un test phénotypique basé sur des cellules humaines transfectées avec un gène rapporteur luciférase sous contrôle d’un élément de réponse aux interférons (ISRE). Ce système a été utilisé pour cribler une chimiothèque d’environ 54 000 composés. Parmi les molécules sélectionnées, nous avons montré que le composé DD264 stimule la réponse immunitaire innée dans les cultures cellulaires, et présente une activité antivirale à large spectre. En recherchant la cible de ce composé, nous avons montré qu’il inhibe la voie de biosynthèse de novo des pyrimidines, et notamment la quatrième enzyme de cette voie métabolique, la dihydroorotate déshydrogénase (DHODH). Ainsi, nos résultats établissent de façon surprenante un lien fonctionnel nouveau entre la voie de biosynthèse des pyrimidines et la réponse innée antivirale. | fr |
| dc.description.abstract | RNA viruses are responsible for major human diseases such as flu, bronchitis, dengue, hepatitis C or measles. They also represent an emerging threat because of increased worldwide exchanges and human populations penetrating more and more natural ecosystems. Recent progresses in our understanding of cellular pathways controlling viral replication suggest that compounds targeting host cell functions, rather than the virus itself, could inhibit a large panel of RNA viruses. In particular, several academic laboratories and private companies are now seeking molecules that stimulate the host innate antiviral response. One appealing strategy is to identify molecules that induce the large cluster of antiviral genes known as Interferon-Stimulated Genes (ISGs). To reach this goal, we have developed a phenotypic assay based on human cells transfected with a luciferase reporter gene under control of an interferon-stimulated response element (ISRE). This system was used in a high-throughput screening of chemical libraries comprising around 54,000 compounds. Among validated hits, compound DD264 was shown to boost the innate immune response in cell cultures, and displayed a broad-spectrum antiviral activity. While deciphering its mode of action, DD264 was found to target the fourth enzyme of de novo pyrimidine biosynthesis, namely the dihydroorotate dehydrogenase (DHODH). Thus, our data unraveled a yet unsuspected link between pyrimidine biosynthesis and the innate antiviral response. | en |
| dc.language.iso | fr | |
| dc.publisher | Éditions EDK, Groupe EDP Sciences | |
| dc.relation.ispartof | M/S Revues | |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [ISSN papier : 0767-0974 ; ISSN numérique : 1958-5381], 2015, Vol. 31, N° 1; p. 98-104 | |
| dc.subject.mesh | Antiviraux | fr |
| dc.subject.mesh | Évaluation préclinique de médicament | fr |
| dc.subject.mesh | Antienzymes | fr |
| dc.subject.mesh | Tests de criblage à haut débit | fr |
| dc.subject.mesh | Humains | fr |
| dc.subject.mesh | Immunité innée | fr |
| dc.subject.mesh | Oxidoreductases acting on CH-CH group donors | fr |
| dc.subject.mesh | Phénotype | fr |
| dc.subject.mesh | Pyrimidines | fr |
| dc.subject.mesh | Bibliothèques de petites molécules | fr |
| dc.subject.mesh | Virus | fr |
| dc.subject.mesh | isolation et purification | fr |
| dc.subject.mesh | pharmacologie | fr |
| dc.subject.mesh | effets des médicaments et substances chimiques | fr |
| dc.subject.mesh | antagonistes et inhibiteurs | fr |
| dc.subject.mesh | biosynthèse | fr |
| dc.subject.mesh | analyse | fr |
| dc.subject.mesh | immunologie | fr |
| dc.title | Activation de la réponse innée antivirale par des inhibiteurs de la biosynthèse des pyrimidines : Les surprises d’un criblage phénotypique | fr |
| dc.title.alternative | Stimulation of the antiviral innate immune response by pyrimidine biosynthesis inhibitors: a surprise of phenotypic screening | en |
| dc.type | Article | |
| dc.contributor.affiliation | Unité de génomique virale et vaccination, département de virologie, Institut Pasteur, CNRS UMR 3569, 28, rue du Docteur Roux, 75724 Paris Cedex 15, France | |
| dc.contributor.affiliation | Unité de chimie et biocatalyse, département de biologie structurale et chimie Institut Pasteur, CNRS UMR3523, 28, rue du Docteur Roux, 75724 Paris Cedex 15, France | |
| dc.identifier.doi | 10.1051/medsci/20153101019 | |
| dc.identifier.pmid | 25658737 | |