| |
| Med Sci (Paris). 35(12): 949–956. doi: 10.1051/medsci/2019191.Les limites des inhibiteurs de points de contrôle
immunitaire et la gestion de leur toxicité Marie Kostine,1* Aurélien Marabelle,2 Thierry Schaeverbeke,1 and Maria Kfoury2 1Service de rhumatologie, hôpital Pellegrin,
Bordeaux,
France 2Institut Gustave Roussy, Villejuif, France |
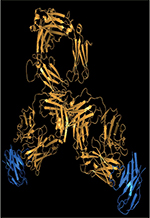
L’étude des mécanismes par lesquels les cancers échappent à l’immunovigilance a permis de
révéler le rôle de diverses molécules (points de contrôle, ou
checkpoints) qui inhibent la réponse immunitaire: notamment CTLA-4
(cytotoxic T-lymphocyte-associated protein 4) et PD-1
(programmed cell death 1)/PD-L1 (programmed cell
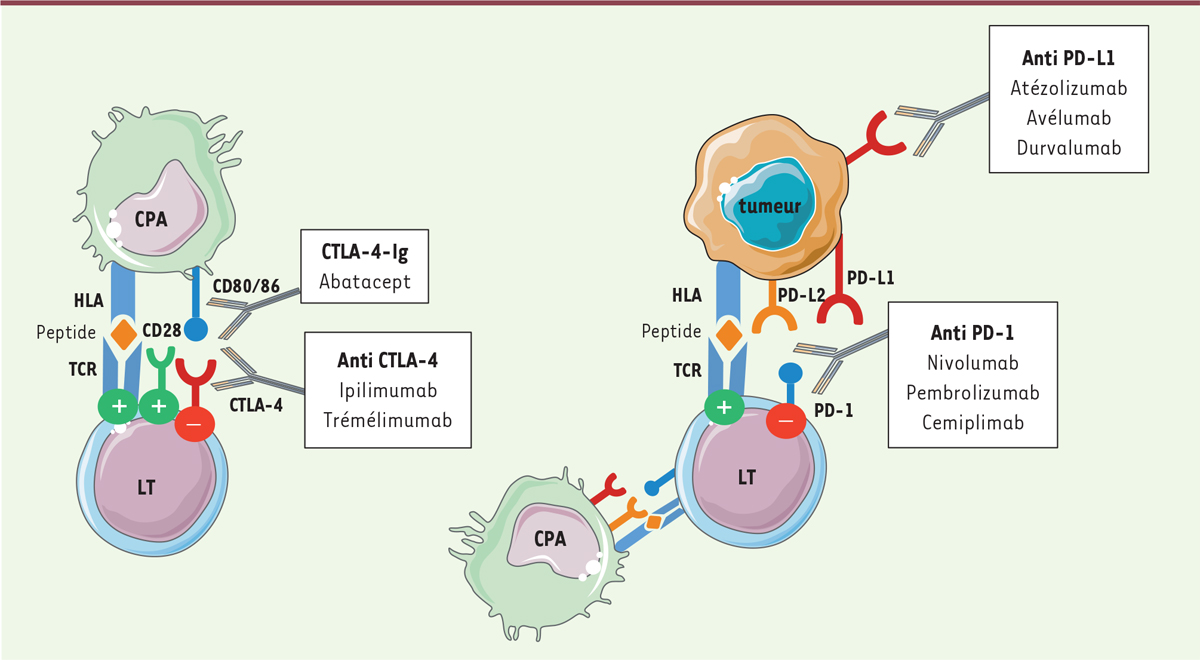
death-ligand 1). Les ICI sont des anticorps thérapeutiques qui ciblent ces
co-signaux inhibiteurs entre cellules tumorales ou cellules présentatrices d’antigènes
et lymphocytes T, activant ou réactivant ainsi une immunité cellulaire T anti-tumorale
(Figure 1). Après leurs
résultats spectaculaires dans le mélanome métastatique, puis dans les cancers du poumon
inopérables, les cancers du rein et urothéliaux, certains cancers digestifs, certains
lymphomes, plus d’une centaine d’essais cliniques sont actuellement en cours et
l’utilisation des ICI est devenue l’une des stratégies thérapeutiques la plus
prometteuse en oncologie.
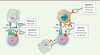 | Figure 1.
Principales thérapeutiques ciblant la co-stimulation.
|
L’obtention d’une réponse tumorale stable, voire la rémission d’un cancer métastatique,
se font souvent au prix d’une toxicité immunologique pouvant concerner tous les organes.
Le spectre de l’auto-immunité induite par ces traitements ne cesse ainsi de s’élargir,
d’autant plus qu’ils sont maintenant utilisés à grande échelle. |
Les effets secondaires immunologiques des inhibiteurs de points de contrôle
immunitaire La rupture de tolérance induite par les inhibiteurs de points de contrôle immunitaire
ne se limite pas à la tumeur. Ils sont susceptibles d’induire des mécanismes de
dysimmunité par perte de tolérance vis-à-vis d’auto-antigènes. Et cela d’autant plus
que la lyse des cellules tumorales, qu’ils induisent en ré-activant le système
immunitaire, aboutit à la libération de médiateurs pro-inflammatoires et de signaux
de danger (ou DAMP pour danger-associated molecular pattern). Ces
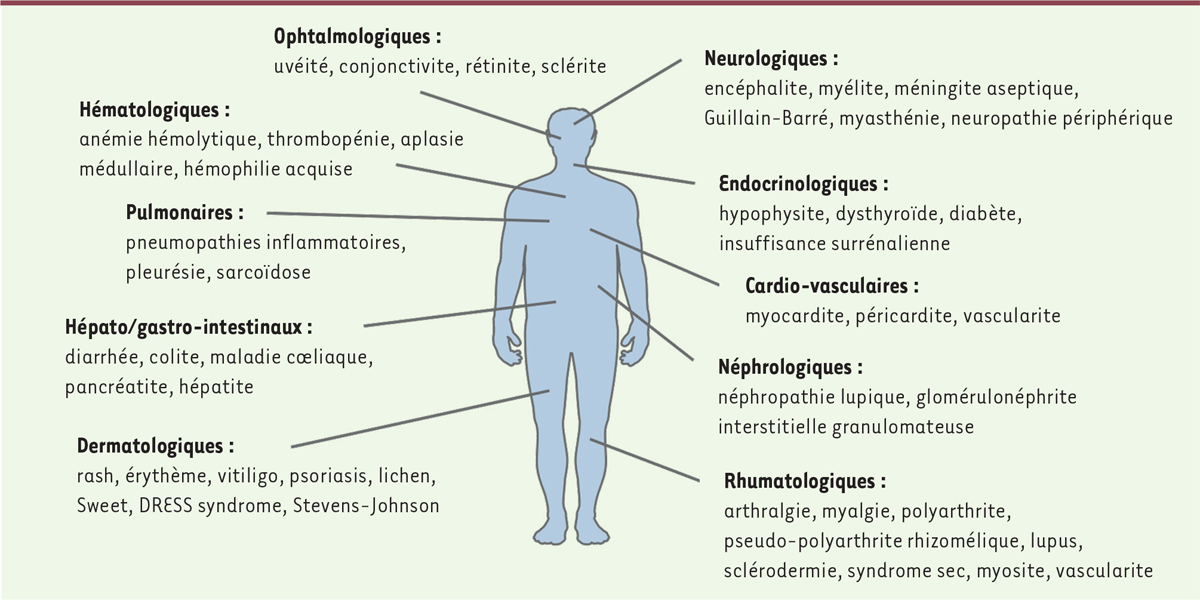
complications ont été décrites sous le nom d’immune-related adverse
events (ou irAE) (Figure
2).
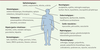 | Figure 2.
Spectre des effets secondaires immunologiques observés sous
inhibiteurs de points de contrôle immunitaire.
|
Ainsi, de nombreux évènements de ce type ont été observés après utilisation des
anticorps anti-CTLA-4, puis avec les anticorps anti-PD-1/PD-L1 et leur combinaison
[1]. Les manifestations
dysimmunitaires induites diffèrent selon le type d’ICI utilisés, en raison de
mécanismes d’action différents. CTLA-4 intervient lors de l’initiation de la réponse
immune dans les organes lymphoïdes, au niveau des lymphocytes T naïfs, mais aussi en
périphérie, au niveau des lymphocytes T régulateurs, ce qui explique le spectre
large et la fréquence plus élevée d’irAE observés avec ces ICI. La voie PD-1/PD-L1,
quant à elle, régule l’activation lymphocytaire T au niveau périphérique ainsi qu’au
sein du microenvironnement tumoral, ce qui restreint le spectre et la fréquence des
irAE qui lui sont associés [2]. Cette toxicité dysimmunitaire survient généralement dans les 3 à 6
premiers mois après l’initiation du traitement. La survenue est plus précoce si des
anticorps anti-CTLA-4 et anti-PD-1 sont combinés ou en cas de traitements
séquentiels avec les deux anticorps [3]. Les toxicités tardives sont moins connues, en raison des périodes de
suivi qui sont limitées. Bien que les irAE puissent concerner tous les organes, les
premières données de rupture de tolérance, issues des essais cliniques, ont révélé
essentiellement des atteintes dermatologiques et digestives, suivies d’atteintes
endocriniennes qui sont parmi les plus fréquentes [4-6]. L’usage des ICI en routine et la diversification de leurs
indications a néanmoins permis l’identification d’irAE plus rares et de plus en plus
variés. Les complications cutanéo-muqueuses sont les plus
fréquentes, observées chez plus de 40 % des patients traités par immunothérapie.
Elles surviennent au cours des premières semaines de traitement [7]: rash non
spécifiques, souvent maculo-papuleux (tronc et extrémités), vitiligo, psoriasis,
lichen et pemphigoïde (Figure
3). Des réactions sévères de type syndrome de
Stevens-Johnson1, de nécrolyse épidermique,
voire de syndrome d’hypersensibilité médicamenteuse (en anglais DRESS, pour
drug reaction [ou rash] with
eosinophilia and systemic symptoms) ont également été rapportées.
 | Figure 3. Vitiligo induit sous traitement anti-PD-1 reçu pour un
mélanome métastatique (collection J. Seneschal,
Bordeaux, France). |
Les complications digestives sont également très
fréquentes, avec des diarrhées observées chez 30 % des patients. D’authentiques
colites inflammatoires peuvent survenir, identiques à celles observées dans la
maladie de Crohn ou les colites microscopiques [8]. Elles mettent en jeu le pronostic vital du
patient en raison du risque de perforation intestinale. Les colites s’observent
principalement avec les anticorps anti-CTLA-4, en monothérapie ou en traitement
combiné, avec une médiane d’apparition de 8 semaines après l’introduction de l’ICI
[9]. Les analyses
histologiques et immunologiques des biopsies ont montré une différence entre les
colites induites sous traitement par anticorps anti-CTLA-4 (infiltrat T
CD4+, forte sécrétion de TNF-a) et celles sous anticorps anti-PD-1
(infiltrat T CD8+, forte proportion de lymphocytes T régulateurs au sein
de la population ICOS[inducible T-cell
costimulator]+CD4+) [10]. Un cas de maladie cœliaque a été rapporté
sous ipilimumab, dans un contexte de diarrhées résistantes aux corticoïdes [11]. Les complications hépatiques sous ICI concernent
environ 3,5 % des patients. Les biopsies hépatiques ont montré des différences
histologiques selon la molécule utilisée, avec une atteinte granulomateuse sous
anticorps anti-CTLA-4 et lobulaire sous anticorps anti-PD-L1 [12]. Des cas d’augmentation du taux de
lipase et d’authentiques pancréatites ont également été rapportés, là aussi plus
fréquemment sous anti-CTLA-4 ou lors de combinaisons d’ICI [13]. Les complications endocriniennes concernent
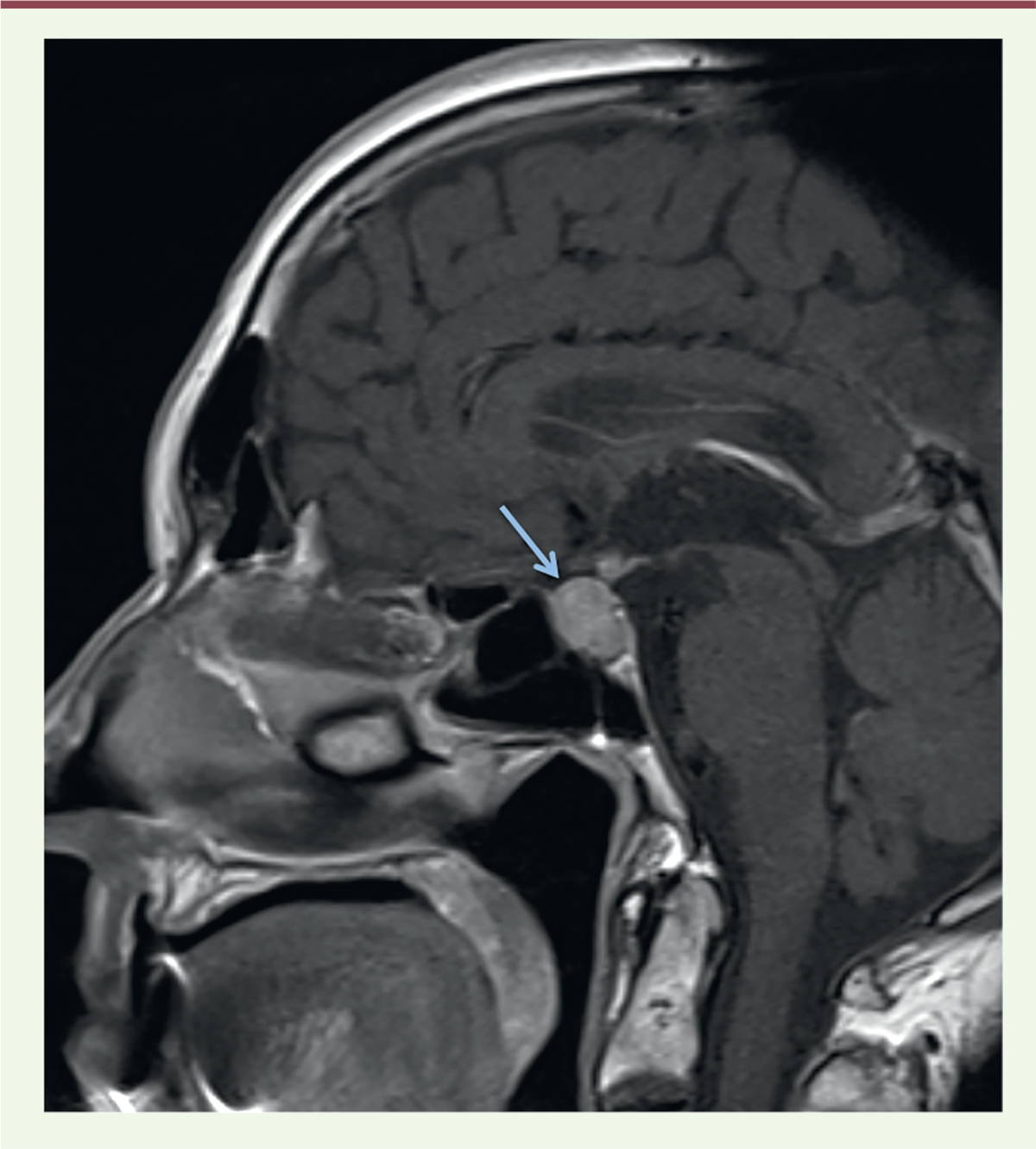
principalement la thyroïde et l’hypophyse (Figure 4), mais la traduction clinique de ces atteintes
aspécifiques (asthénie, faiblesse musculaire) rend le diagnostic difficile. Les
hypophysites auto-immunes font partie des complications endocriniennes rapportées,
principalement sous anticorps anti-CTLA-4, rares sous anticorps anti-PD-1. Elles
présentent les mêmes caractéristiques cliniques, biologiques et radiologiques qu’une
hypophysite lymphocytaire, une pathologie auto-immune rare observée pendant la
grossesse ou en post-partum. La physiopathologie des hypophysites auto-immunes
repose sur la reconnaissance directe des cellules hypophysaires, qui expriment
CTLA-4, par les anticorps anti-CTLA-4, accompagné par une activation du complément
[14]. L’atteinte
thyroïdienne est plus fréquemment observée sous anticorps anti-PD-1 ou en
combinaison, avec une prédominance d’hypothyroïdie. Des hyperthyroïdies ont été
également rapportées, rarement d’authentiques maladies de Basedow2. Plus rarement, une insuffisance surrénalienne primitive ou
un diabète insulino-dépendant se développent sous une forme fulminante. Il est
intéressant de souligner que la majorité des cas de diabète surviennent chez des
patients HLA(human leukocyte antigen)-DR4 dont les sérums, avant
traitement, contiennent dans plus de la moitié des cas des auto-anticorps,
soulignant une auto-immunité pré-existante [15].
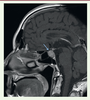 | Figure 4. Hypophysite auto-immune apparue sous anticorps
anti-CTLA-4 (collection M. Haissaguerre,
Bordeaux, France). |
Les complications pulmonaires sont rares, environ 5 %
des patients sous traitement par anticorps anti-PD-L1 et 10 % en cas de combinaison,
mais potentiellement graves. Les aspects radiologiques sont variables et non
spécifiques: pneumopathie organisée cryptogénique (POC), verre dépoli isolé,
pneumopathie interstitielle non spécifique (NSIP) et pneumopathie d’hypersensibilité
(PHS) [16]. La dyspnée et
la toux sont les points d’appel cliniques. Cependant un tiers des patients reste
asymptomatique avec une découverte fortuite du fait d’une imagerie réalisée dans le
cadre du suivi oncologique. De nombreux cas de sarcoïdose sont également rapportés
sous ICI. Les patients sont asymptomatiques dans 25 % des cas et la découverte
fortuite à l’imagerie de suivi oncologique d’adénopathies médiastinales et/ou de
nodules pulmonaires souvent hypermétaboliques, suggèrent une progression tumorale.
La documentation histologique est alors d’un intérêt majeur avant d’envisager
l’arrêt du traitement par ICI [17]. Les complications rhumatologiques sont peu fréquentes
(6-7 %) mais très variées: arthralgies et myalgies, mono-oligoarthrite,
polyarthrite, pseudo-polyarthrite rhizomélique, rhumatisme psoriasique, syndrome
RS3PE (remitting seronegative symmetrical synovitis with pitting
edema, ou polyarthrite aiguë œdémateuse bénigne du sujet âgé), syndrome
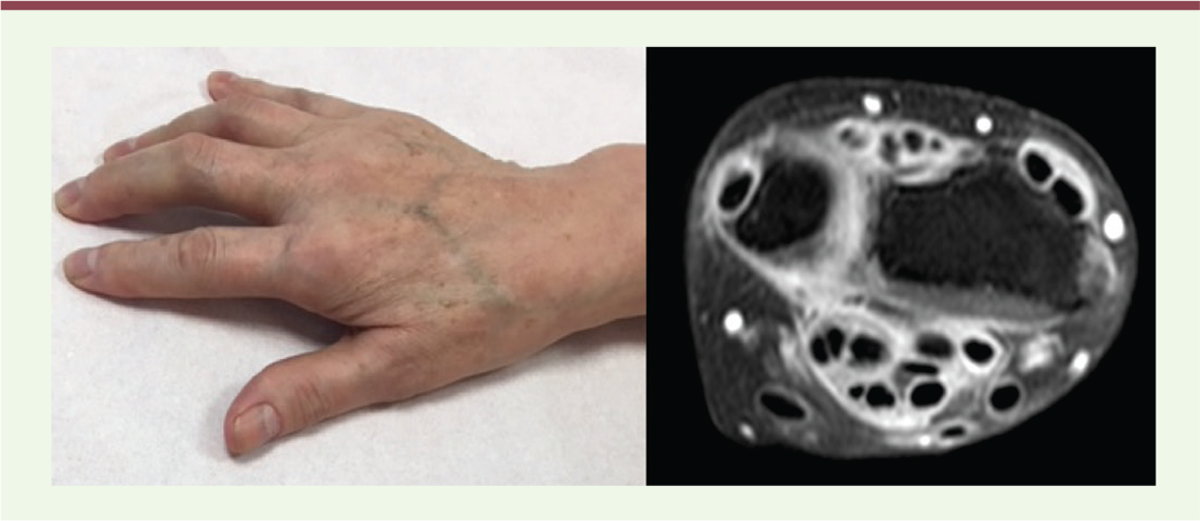
sec, vascularite, lupus, sclérodermie et myosite (Figure 5). Dans certains cas il s’agit d’une
authentique pathologie rhumatologique ou systémique (Gougerot-Sjögren3,, PR [polyarthrite rhumatoïde], vascularite à
ANCA [auto-anticorps anti-cytoplasmiques de neutrophiles], etc.) mais la majorité
des patients ne remplissent pas les critères de classification et présentent donc
plutôt des pathologies rhumatologiques-like. La négativité du
syndrome inflammatoire biologique ou du bilan immunologique ne doit donc pas exclure
le diagnostic d’un irAE rhumatologique/systémique. Les myosites sont fréquemment
associées à une myasthénie (15 %) ou une myocardite. La myasthénie doit être évoquée
devant un ptosis (chute de la paupière supérieure), une diplopie4 et/ou une symptomatologie bulbaire.
 | Figure 5.
Synovite radio-ulnaire distale et ténosynovites des
fléchisseurs et extenseurs observée sous traitement
anti-PD-1.
|
Les complications neurologiques sont rares (1 %) et
très variées, allant de la céphalée modérée à l’encéphalite grave [18]. Parmi les toxicités neurologiques,
ont été décrits: syndrome de Guillain-Barré, myélite, méningite aseptique, myopathie
inflammatoire, myasthénie (possiblement associée à une myosite) et neuropathie
périphérique. Les complications cardiologiques sont potentiellement
fatales, isolées ou compliquant certaines myosites. Il s’agit principalement de la
myocardite, à rechercher absolument en cas de suspicion, par un dosage de la
troponine, un électro-cardiogramme, voire une échographie ou une IRM (imagerie par
résonnance nucléaire) cardiaque [19]. Elle survient habituellement dans les six premières semaines de
traitement par ICI et peut se révéler par une dyspnée ou une douleur thoracique. Les complications rénales concernent 1 à 2 % des
patients sous ICI en monothérapie et jusqu’à 5 % des patients recevant une
combinaison [20]. Il s’agit
principalement de néphrites tubulo-interstitielles aiguës, mais une atteinte
granulomateuse est parfois retrouvée. Une néphrite lupique a été rapportée sous
ipilimumab. Les complications plus rares. Il s’agit de
complications ophtalmologiques et hématologiques (moins de 1 %). Quelques études ont
ainsi rapportés des manifestations ophtalmologiques inflammatoires induites sous
ICI: uvéite, sclérite, rétinite, orbitopathie inflammatoire, voire une maladie de
Vogt-Koyanagi-Harada5. Une étude française
prospective a évalué à 0,4 % la prévalence des irAE ophtalmologiques [21]. Des irAE hématologiques
ont également été décrits: principalement des neutropénies, anémies hémolytiques ou
thrombopénies auto-immunes et anémies aplasiques [22]. Une hémophilie A a aussi été rapportée
sous ipilimumab. |
Effets secondaires immunologiques des inhibiteurs de points de contrôle
immunitaire dans des populations particulières Maladie inflammatoire préexistante. Du fait d’un risque
théorique d’aggravation de la maladie inflammatoire ou auto-immune, les patients
présentant une maladie inflammatoire préexistante ont été exclus des essais
cliniques. Nous disposons néanmoins de plusieurs séries rétrospectives révélant
qu’environ la moitié des patients ont présenté soit des irAE classiques, soit des
exacerbations de la pathologie inflammatoire préexistante, généralement bien
contrôlés par une corticothérapie ou par l’optimisation du traitement
immuno-modulateur [23,
24]. Les données
actuelles ne suggèrent pas de contre-indication aux ICI pour les patients avec une
maladie inflammatoire préexistante, mais des études prospectives de plus larges
effectifs sont nécessaires pour valider ces observations rétrospectives. Malades transplantés. Ces patients nécessitent une
modulation étroite de l’immunosuppression pour maintenir une tolérance du greffon
qu’ils ont reçu et éviter un rejet ou une réaction du greffon contre l’hôte.
L’anticorps anti-CTLA-4, bien qu’ayant une fréquence et un spectre de toxicité plus
large, semble mieux toléré dans cette population que l’anticorps anti-PD-1 [25,26]. Des données précliniques viennent
conforter cette observation en montrant le rôle majeur de la voie PD-1/PD-L1 dans la
tolérance du greffon [27].
Une revue de la littérature récente rapporte un rejet du greffon solide chez 41 %
des patients: 11/23 patients avec greffe rénale, 4/11 patients avec greffe hépatique
et 1/5 patients avec greffe cardiaque, sans différence entre les patients traités
par l’anticorps anti-CTLA-4 et ceux traités par l’anticorps anti-PD-1, et avec délai
médian de 21 jours [28]. La
prise en charge oncologique optimale reste donc à déterminer dans cette
population. Maladie infectieuse chronique (exemple du VIH). Sauf
dans de rares exceptions, les infections virales par le VIH (virus de
l’immunodéficience humaine), le VHB et le VHC (virus de l’hépatite B et C) sont
également des critères d’exclusion des essais cliniques sur les ICI. L’idée
sous-jacente est que ces infections chroniques pourraient altérer la fonction
lymphocytaire T et donc, théoriquement, compromettre l’efficacité de l’ICI, surtout
chez les patients infectés par le VIH qui présentent un taux de lymphocytes T
CD4+ diminué. En réalité, les données rétrospectives disponibles sont
extrêmement rassurantes, sans signal d’alerte sur la toxicité (avec 8,6 % d’irAE
sévères), une charge virale restant indétectable (93 % des cas) et même une
augmentation du nombre de lymphocytes CD4+ [29]. Des essais cliniques évaluant un
traitement par anticorps anti-PD-1 en monothérapie (NCT02595866, NCT03304093) ou en
combinaison avec l’anticorps anti-CTLA-4 (NCT02408861) sont en cours. En attente des
résultats de ces essais, il est considéré qu’une infection virale chronique,
notamment par le VIH, ne représente pas de contre-indication à l’immunothérapie. |
La prise en charge des irAE repose sur leur identification précoce et une
collaboration étroite entre oncologue référent et spécialiste de l’organe touché
[30]. La définition des
grades de sévérité, par symptôme et par organe, est fondée sur la classification
common terminology criteria for adverse events (CTCAE) du
National Cancer Institute, disponible en ligne6. Pour certaines toxicités, cette classification
mérite d’être réévaluée régulièrement [31]. La prise en charge des irAE s’appuie sur le grade défini
par cette classification et les stratégies thérapeutiques reposent sur les
protocoles de gestion des toxicités qui ont été développés par les laboratoires
pharmaceutiques au cours des essais cliniques. |
Les recommandations actuelles Il existe actuellement trois recommandations internationales pour la gestion des irAE
: • Les recommandations de l’ESMO (European society of medical
oncology) [3] • Les recommandations de la SITC (Society for immunotherapy of
cancer) [32] • Les recommandations de l’ASCO (American society of clinical
oncology) [33] Ces recommandations ont été développées principalement par des oncologues. S’y
ajoutent des recommandations spécifiques des sociétés savantes, telles que les
recommandations pour la gestion des irAE endocriniens [34] ou des irAE rhumatologiques. Pour les irAE de grade 1, le traitement symptomatique est privilégié et la
corticothérapie n’est pas indiquée. La corticothérapie est le traitement de 1re
intention pour les irAE de grade 2. La dose recommandée varie entre 0,5 et 1 mg/Kg
selon chaque type d’irAE. Par exemple, une dose inférieure ou égale à 20 mg/j
d’équivalent du corticoïde prednisone est souvent suffisante pour les irAE
rhumatologiques, en complément d’éventuels gestes locaux, si besoin est. Pour les irAE de grade 3, notamment dermatologiques, digestifs, pulmonaires, rénaux,
hématologiques et neurologiques, la corticothérapie proposée est de 1 à 2 mg/Kg par
voie intraveineuse. Des discussions persistent dans les cas d’hépatites
immuno-induites: des résolutions spontanées étant observées, la corticothérapie
systématique est donc souvent débattue [35]. Les autres traitements immunosuppresseurs. Le recours à
d’autres traitements immunosuppresseurs (traitements conventionnels ou biologiques)
peut être nécessaire en cas de persistance ou d’aggravation des irAE sous
corticothérapie, ou en cas de corticorésistance ou de corticodépendance. Les
molécules utilisées dépendent du type d’irAE: le méthotrexate, l’hydroxychloroquine
et la salazopyrine sont les traitements conventionnels les plus utilisés pour les
irAE rhumatologiques, avec un possible sur-risque de réaction d’hypersensibilité
pour la salazopyrine dans cette situation [36-38]. Le mycophénolate mofétil (un immunosuppresseur) est également utilisé
dans certains cas d’hépatites, pneumopathies immuno-induites, myosites et
sclérodermie-like [39]. Fondé sur l’idée d’un parallèle avec les réactions de
greffon contre l’hôte, le tacrolimus a récemment été testé dans des situations
d’irAE (2 colites et 1 éruption sévère avec atteinte muqueuse) en échec de la
corticothérapie et d’un traitement par anticorps anti-TNF-a [40]. L’infliximab a été le premier traitement biologique utilisé dans le traitement des
colites sévères par les gastro-entérologues. Les données concernant les anticorps
anti-TNF-a sont rassurantes pour un usage ponctuel (1 ou 2 perfusions), mais peu de
données existent sur leur utilisation au long cours. Les équipes de rhumatologie
américaines ont également utilisé fréquemment les anticorps anti-TNF-a en cas
d’échec de la corticothérapie. Un essai clinique oncologique de phase I associant
ICI et anti-TNF-a est en cours (NCT03293784). Il devrait apporter des informations
sur l’efficacité de ce traitement et les risques de cette association, utiles pour
notre gestion des irAE sévères. Certains patients ont reçu du tocilizumab pour des
irAE variés, soit à la dose de 4 mg/kg par voie intra-veineuse, avec une
amélioration dans 80 % des cas, soit à la dose de 162 mg bimensuel par voie
sous-cutanée pour des atteintes rhumatologiques [41]. Le rituximab a lui aussi été utilisé, avec
des schémas thérapeutiques différents, chez des patients présentant des irAE
hématologiques ou neurologiques [42]. Une étude de phase II, associant rituximab et anticorps anti-PD-1
chez des patients présentant un lymphome folliculaire a montré une bonne efficacité
et une bonne tolérance [43]. Enfin, le védolizumab, un AcM anti-intégrine α4-β7, approuvé dans les
maladies inflammatoires chroniques intestinales, qui agit en limitant le recrutement
lymphocytaire dans le tractus gastro-intestinal, a aussi été utilisé chez des
patients présentant une colite immuno-induite réfractaire [44]. Le seul signal négatif provient à ce jour
de l’anticorps anti-IL(interleukine)-17, le sécukinumab, utilisé pour le traitement
d’une poussée d’une maladie de Crohn, un psoriasis sévère et des arthralgies
observées sous traitement par l’anticorps anti-PD-1. Il a permis une résolution
complète des irAE au prix de la perte de l’efficacité anti-tumorale initiale [45]. Une publication récente
rapporte l’utilisation de l’anticorps anti-IL-17 dans la gestion d’une atteinte
psoriasique immuno-induite sans altération de la réponse anti-tumorale. Il n’existe pas de données montrant que les patients ayant reçu de tels traitements
pour la gestion d’un irAE aient une moins bonne réponse tumorale. Toutefois,
l’impact à long terme de la corticothérapie et des autres médicaments
immunosuppresseurs dans le cadre du cancer devra être étroitement surveillé. |
Poursuite du traitement oncologique Le traitement oncologique par ICI peut être poursuivi pour les irAE de grade 1, sous
réserve d’une surveillance rapprochée, et avec une vigilance particulière pour les
irAE neurologiques, hématologiques et cardiologiques. Pour les irAE de grade 2, il
est souvent conseillé de suspendre temporairement le traitement jusqu’à résolution
ou retour à un grade 1. Pour les irAE de grade 3, l’arrêt de l’ICI est indiqué, au
moins de façon temporaire, parfois définitif. Sa reprise se discutera lorsque l’irAE
sera résolu ou après un retour à un grade 1. En cas d’irAE de grade 4, l’ICI sera
définitivement arrêté, à l’exception des endocrinopathies. Les endocrinopathies sont
en effet le plus souvent irréversibles et devront être supplémentées à vie. La
survie des patients qui arrêtent le traitement par ICI en raison d’un irAE n’est
toutefois pas altérée [46]. |
Devant la fréquence des diarrhées et colites que l’on observe sous traitement par
anticorps anti-CTLA-4, une prophylaxie par budésonide a été testée, sans
démonstration d’efficacité [47]. Les patients présentant une maladie auto-immune, théoriquement plus
à risque de développer des irAE, sont également concernés, afin de contrôler la
maladie auto-immune dont ils sont atteints avant le début du traitement par l’ICI et
afin de diminuer le risque de poussée et/ou d’irAE. Une étude rétrospective
multicentrique française ayant inclus 112 patients avec maladie auto-immune ou
inflammatoire préexistante (principalement psoriasis, PR, maladie inflammatoire
chronique de l’intestin, spondylarthrite ankylosante, lupus) a montré une survie
sans progression plus courte et un taux de réponse inférieur chez les patients
recevant un traitement immunosuppresseur à l’instauration de l’ICI [48]. De même, il a récemment été
rapporté qu’une corticothérapie supérieure à 10 mg/j d’équivalent prednisone au
début du traitement par l’ICI était associée à une réponse anti-tumorale et des taux
de survie plus faibles [49]. En attendant des études prospectives confirmant ou non ces données, il est prudent
d’essayer de minimiser le traitement par corticoïdes et immunosuppresseurs au moment
de l’introduction de l’ICI. Plusieurs groupes ont démontré que la survenue d’irAE
était associée à une meilleure réponse à l’ICI, suggérant que cette auto-immunité
pourrait interférer avec l’immunité anti-tumorale [50]. Il ne semble donc pas nécessaire de
prévenir les irAE chez tous les patients, mais il est essentiel d’identifier ceux à
risque d’irAE sévères, afin d’anticiper la survenue de ces évènements et d’adapter
les stratégies de prévention et de prise en charge. |
La connaissance des irAE est essentielle pour l’ensemble de la communauté médicale
qui sera confrontée à la prise en charge des patients traités par ICI. La prise en
charge des irAE reste un défi car il est essentiel de contrôler la toxicité
immunologique sans perdre l’efficacité anti-tumorale, et la stratégie optimale reste
à déterminer. La prise en charge des toxicités, plus fréquentes lors des
combinaisons de traitements, est certainement un des enjeux majeurs du développement
de l’immunothérapie. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les
données publiées dans cet article.
|
Footnotes |
1. Boutros
C,
Tarhini
A,
Routier
E, et al.
Safety profiles of anti-CTLA-4 and anti-PD-1 antibodies alone and
in combination . Nat Rev Clin
Oncol.
2016; ; 13:
:473.–486. 2. Pardoll
DM. The blockade of
immune checkpoints in cancer immunotherapy .
Nat Rev Cancer.
2012; ; 12:
:252.–264. 3. Haanen
JBAG,
Carbonnel
F,
Robert
C, et al.
Management of toxicities from immunotherapy: ESMO Clinical
Practice Guidelines for diagnosis, treatment and follow-up .
Ann Oncol.
2018;
29 (suppl (4)):
:iv264.–i6. 4. Belum
VR,
Benhuri
B,
Postow
MA, et al.
Characterisation and management of dermatologic adverse events to
agents targeting the PD-1 receptor . Eur J
Cancer.
2016; ; 60:
:12.–25. 5. Cramer
P,
Bresalier
RS. Gastrointestinal
and Hepatic Complications of Immune Checkpoint Inhibitors .
Curr Gastroenterol Rep.
2017; ; 19: :3.. 6. Byun
DJ,
Wolchok
JD,
Rosenberg
LM,
Girotra
M. Cancer
immunotherapy - immune checkpoint blockade and associated
endocrinopathies . Nat Rev
Endocrinol.
2017; ; 13:
:195.–207. 7. Sibaud
V,
Boulinguez
S,
Pagès
C, et al.
Dermatologic toxicities of immune checkpoint
inhibitors . Ann Dermatol
Venereol.
2018; ; 145:
:313.–330. 8. Bertha
M,
Bellaguara
E,
Kuzel
T,
Hanauer
S. Checkpoint
inhibitor-induced colitis: A new type of inflammatory bowel
disease? . ACG Case Rep J.
2017; ; 4: :e112.. 9. Collins
M,
Michot
JM,
Danlos
FX, et al.
Inflammatory gastrointestinal diseases associated with PD-1
blockade antibodies . Ann
Oncol.
2017; ; 28:
:2860.–2865. 10. Coutzac
C,
Adam
J,
Soularue
E, et al.
Colon immune-related adverse events: Anti-CTLA-4 and anti-PD-1
blockade induce distinct immunopathological entities .
J Crohns Colitis.
2017; ; 11:
:1238.–1246. 11. Gentile
NM,
D’Souza
A,
Fujii
LL, et al.
Association between ipilimumab and celiac
disease . Mayo Clin Proc.
2013; ; 88:
:414.–417. 12. De Martin
E,
Michot
J-M,
Papouin
B, et al.
Characterization of liver injury induced by cancer immunotherapy
using immune checkpoint inhibitors . J
Hepatol.
2018; ; 68:
:1181.–1190. 13. Su
Q,
Zhang
X-C,
Zhang
C-G, et al.
Risk of immune-related pancreatitis in patients with solid tumors
treated with immune checkpoint inhibitors: Systematic assessment with
meta-analysis . J Immunol
Res.
2018; ; 2018:
:1027323.. 14. Postow
MA,
Sidlow
R,
Hellmann
MD. Immune-related
adverse events associated with immune checkpoint blockade .
N Engl J Med.
2018; ; 378:
:158.–168. 15. Stamatouli
AM,
Quandt
Z,
Perdigoto
AL, et al.
Collateral damage: insulin-dependent diabetes induced with
checkpoint inhibitors .
Diabetes.
2018; ; 67:
:1471.–1480. 16. Naidoo
J,
Wang
X,
Woo
KM, et al.
Pneumonitis in patients treated with anti-programmed
death-1/programmed death ligand 1 therapy . J
Clin Oncol.
2017; ; 35:
:709.–717. 17. Firwana
B,
Ravilla
R,
Raval
M, et al.
Sarcoidosis-like syndrome and lymphadenopathy due to checkpoint
inhibitors . J Oncol Pharm
Pract.
2017; ; 23:
:620.–624. 18. Larkin
J,
Chmielowski
B,
Lao
CD, et al.
Neurologic serious adverse events associated with nivolumab plus
ipilimumab or nivolumab alone in advanced melanoma, including a case series
of encephalitis .
Oncologist.
2017; ; 2:
:709.–718. 19. Moslehi
JJ,
Salem
J-E,
Sosman
JA, et al.
Increased reporting of fatal immune checkpoint
inhibitor-associated myocarditis .
Lancet.
2018; ; 391: :933.. 20. Murakami
N,
Motwani
S,
Riella
LV. Renal
complications of immune checkpoint blockade .
Curr Probl Cancer.
2017; ; 41:
:100.–110. 21. Bitton
K,
Michot
J-M,
Barreau
E, et al.
Prevalence and clinical patterns of ocular complications
associated with anti-PD-1/PD-L1 anticancer immunotherapy .
Am J Ophthalmol.
2019; ; 202:
:109.–117. 22. Delanoy
N,
Michot
J-M,
Comont
T, et al.
Haematological immune-related adverse events induced by anti-PD-1
or anti-PD-L1 immunotherapy: a descriptive observational
study . Lancet Haematol.
2019; ; 6:
:e48.–e57. 23. Menzies
AM,
Johnson
DB,
Ramanujam
S, et al.
Anti-PD-1 therapy in patients with advanced melanoma and
preexisting autoimmune disorders or major toxicity with
ipilimumab . Ann Oncol.
2017; ; 28:
:368.–376. 24. Johnson
DB,
Khushalani
NI,
Puzanov
I, et al.
Ipilimumab in metastatic melanoma patients with pre-existing
autoimmune disorders . J Clin
Oncol.
2017; ; 33: (suppl)
:9019.. 25. Davids
MS,
Kim
HT,
Bachireddy
P, et al.
Ipilimumab for patients with relapse after allogeneic
transplantation . N Engl J
Med.
2016; ; 375:
:143.–153. 26. Lipson
EJ,
Bagnasco
SM,
Moore
J, et al.
Tumor regression and allograft rejection after administration of
anti-PD-1 . N Engl J Med.
2016; ; 374:
:896.–898. 27. Tanaka
K,
Albin
MJ,
Yuan
X, et al.
PDL1 is required for peripheral transplantation tolerance and
protection from chronic allograft rejection .
J Immunol.
2007; ; 179:
:5204.–5210. 28. Abdel-Wahab
N,
Safa
H,
Abudayyeh
A, et al.
Checkpoint inhibitor therapy for cancer in solid organ
transplantation recipients: an institutional experience and a systematic
review of the literature . J Immunother
Cancer.
2019; ; 7: :106.. 29. Cook
MR,
Kim
C. Safety and
efficacy of immune checkpoint inhibitor therapy in patients with HIV
infection and advanced-stage cancer: a systematic review .
JAMA Oncol.
2019; ; 5:
:1049.–1054. 30. Champiat
S,
Lambotte
O,
Barreau
E, et al.
Management of immune checkpoint blockade dysimmune toxicities: a
collaborative position paper . Ann
Oncol.
2016; ; 27:
:559.–574. 31. Friedman
CF,
Clark
V,
Raikhel
AV, et al.
Thinking critically about classifying adverse events: incidence
of pancreatitis in patients treated with nivolumab +
ipilimumab . J Natl Cancer
Inst.
2017;; 109. doi: 10.1093/jnci/djw260.. 32. Puzanov
I,
Diab
A,
Abdallah
K, et al.
Managing toxicities associated with immune checkpoint inhibitors:
consensus recommendations from the Society for immunotherapy of cancer
(SITC) toxicity management working group . J
Immunother Cancer.
2017; ; 5: :95.. 33. Brahmer
JR,
Lacchetti
C,
Schneider
BJ, et al.
Management of immune-related adverse events in patients treated
with immune checkpoint inhibitor therapy: American society of clinical
oncology clinical practice guideline . J Clin
Oncol.
2018; ; 36:
:1714.–1768. 34. Castinetti
F,
Albarel
F,
Archambeaud
F, et al.
French Endocrine society guidance on endocrine side-effects of
immunotherapy . Endocr Relat
Cancer.
2018
Oct 1; pii: ERC-18-0320.R1.. 35. Gauci
M-L,
Baroudjian
B,
Zeboulon
C, et al.
Immune-related hepatitis with immunotherapy: are corticosteroids
always needed? . J Hepatol.
2018; ; 69:
:548.–550. 36. Kostine
M,
Rouxel
L,
Barnetche
T, et al.
Rheumatic disorders associated with immune checkpoint inhibitors
in patients with cancer-clinical aspects and relationship with tumour
response: a single-centre prospective cohort study .
Ann Rheum Dis.
2017; ; 77:
:393.–398. 37. Roberts
J,
Smylie
M,
Walker
J, et al.
Hydroxychloroquine is a safe and effective steroid-sparing agent
for immune checkpoint inhibitor-induced inflammatory
arthritis . Clin Rheumatol.
2019; ; 38:
:1513.–1519. 38. Ford
M,
Sahbudin
I,
Filer
A, et al.
High proportion of drug hypersensitivity reactions to
sulfasalazine following its use in anti-PD-1-associated inflammatory
arthritis . Rheumatology.
2018; ; 57:
:2244.–2246. 39. Friedman
CF,
Proverbs-Singh
TA,
Postow
MA. Treatment of the
immune-related adverse effects of immune checkpoint inhibitors: a
review . JAMA Oncol.
2016; ; 2:
:1346.–1353. 40. Beardslee
T,
Draper
A,
Kudchadkar
R. Tacrolimus for
the treatment of immune-related adverse effects refractory to systemic
steroids and anti-tumor necrosis factor α therapy .
J Oncol Pharm Pract.
2019; ; 25:
:1275.–1281. 41. Stroud
CR,
Hegde
A,
Cherry
C, et al.
Tocilizumab for the management of immune mediated adverse events
secondary to PD-1 blockade . J Oncol Pharm
Pract.
2019; ; 25:
:551.–557. 42. Khan
U,
Ali
F,
Khurram
MS, et al.
Immunotherapy-associated autoimmune hemolytic
anemia . J Immunother
Cancer.
2017; ; 5: :15.. 43. Westin
JR,
Chu
F,
Zhang
M, et al.
Safety and activity of PD1 blockade by pidilizumab in combination
with rituximab in patients with relapsed follicular lymphoma: a single
group, open-label, phase 2 trial . Lancet
Oncol.
2014; ; 15:
:69.–77. 44. Bergqvist
V,
Hertervig
E,
Gedeon
P, et al.
Vedolizumab treatment for immune checkpoint inhibitor-induced
enterocolitis . Cancer Immunol
Immunother.
2017; ; 66:
:581.–592. 45. Esfahani
K,
Miller
WH. Reversal of
autoimmune toxicity and loss of tumor response by interleukin-17
blockade . N Engl J Med.
2017; ; 376:
:1989.–1991. 46. Schadendorf
D,
Wolchok
JD,
Hodi
FS, et al.
Efficacy and safety outcomes in patients with advanced melanoma
who discontinued treatment with nivolumab and ipilimumab because of adverse
events: a pooled analysis of randomized phase II and III
trials . J Clin Oncol.
2017; ; 35:
:3807.–3814. 47. Weber
J,
Thompson
JA,
Hamid
O, et al.
A randomized, double-blind, placebo-controlled, phase II study
comparing the tolerability and efficacy of ipilimumab administered with or
without prophylactic budesonide in patients with unresectable stage III or
IV melanoma . Clin Cancer
Res.
2009; ; 15:
:5591.–5598. 48. Tison
A,
Quéré
G,
Misery
L, et al.
Safety and efficacy of immune checkpoint inhibitors in patients
with cancer and preexisting autoimmune diseases: a nationwide multicenter
retrospective study . Arthritis
Rheum.
2019: 10.1002/art.41068. 49. Arbour
KC,
Mezquita
L,
Long
N, et al.
Impact of baseline steroids on efficacy of programmed cell
death-1 and programmed death-ligand 1 blockade in patients with
non-small-cell lung cancer . J Clin
Oncol.
2018; ; 36:
:2872.–2878. 50. Haratani
K,
Hayashi
H,
Chiba
Y, et al.
Association of immune-related adverse events with nivolumab
efficacy in non-small-cell lung cancer . JAMA
Oncol.
2018; ; 4:
:374.–378. |