2007
1-
Tendances séculaires de la croissance
L'étude de l'interaction entre croissance et nutrition est une discipline classique de l'anthropologie. Ces études restent indispensables en épidémiologie pour évaluer les influences de facteurs mésologiques et pour situer l'état de santé à la fois d'un individu ou d'une population. En termes individuels, les enquêtes de croissance permettent d'établir des normes et donc de situer les enfants sortant de la normalité, aussi bien en excès qu'en insuffisance. Elles permettent donc d'aborder des problèmes aussi divers que celui de l'obésité, des carences nutritionnelles, des maladies ou des syndromes génétiques, des différences socioéconomiques, voire même de facteurs psychologiques (Susanne et coll., 2003

).
Dès le XIXe siècle, Quételet (1796-1874) nota cette relation entre nutrition et croissance pour le poids et la taille de nouveau-nés à l'Hospice de la Maternité de Bruxelles, ainsi que pour les courbes de croissance observées à Bruxelles. Il inventa l'indice de Quételet (poids en kg divisé par la taille au carré), connu ensuite comme l'indice de masse corporelle (IMC ou BMI de la littérature anglophone).
La technique anthropométrique est non invasive, simple, rapide et reproductible ; elle est adéquate au travail sur le terrain et dans des enquêtes épidémiologiques. Taille, poids, périmètre du bras, plis sous-cutanés sont de bons indicateurs des conditions nutritionnelles, ainsi que les périmètres abdominal et de la hanche dans l'indication du type d'obésité. Ces indicateurs peuvent servir au dépistage de malnutrition protéino-énergétique ainsi que de l'obésité (Rebato, 2003

).
Croissance et développement
L'analyse détaillée de la croissance et du développement se fait essentiellement sur la base de données longitudinales, c'est-à-dire des données sérielles du même sujet, permettant d'établir la courbe de croissance individuelle. La figure 1.1

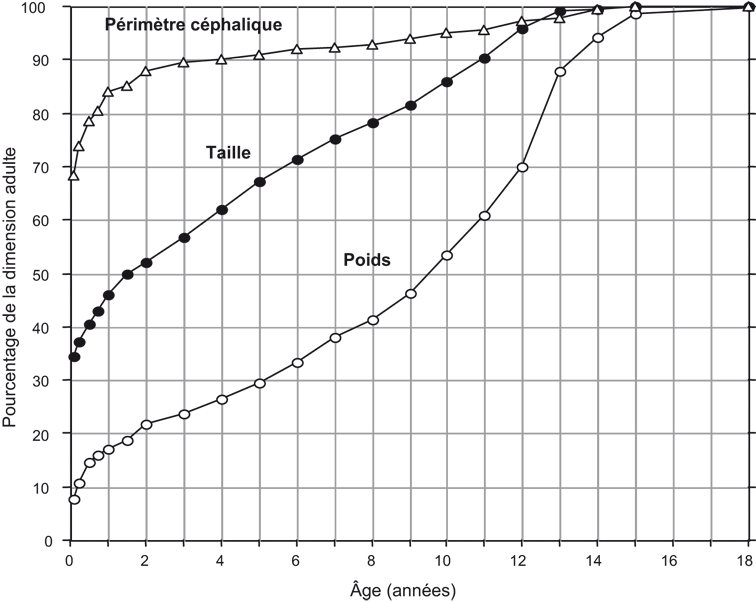
illustre à partir d'un exemple les trois types principaux de courbes de croissance de dimensions corporelles : la courbe de croissance staturale typique des longueurs (longueur des jambes par exemple) et de certaines largeurs (comme la largeur des épaules et des hanches) ; la courbe de croissance pondérale et la courbe de croissance du périmètre céphalique. Dans ce dernier cas, à la naissance, l'enfant a déjà atteint une large part de la dimension finale ; cette courbe est similaire pour toutes les dimensions crâniennes ainsi que pour les dimensions du visage.
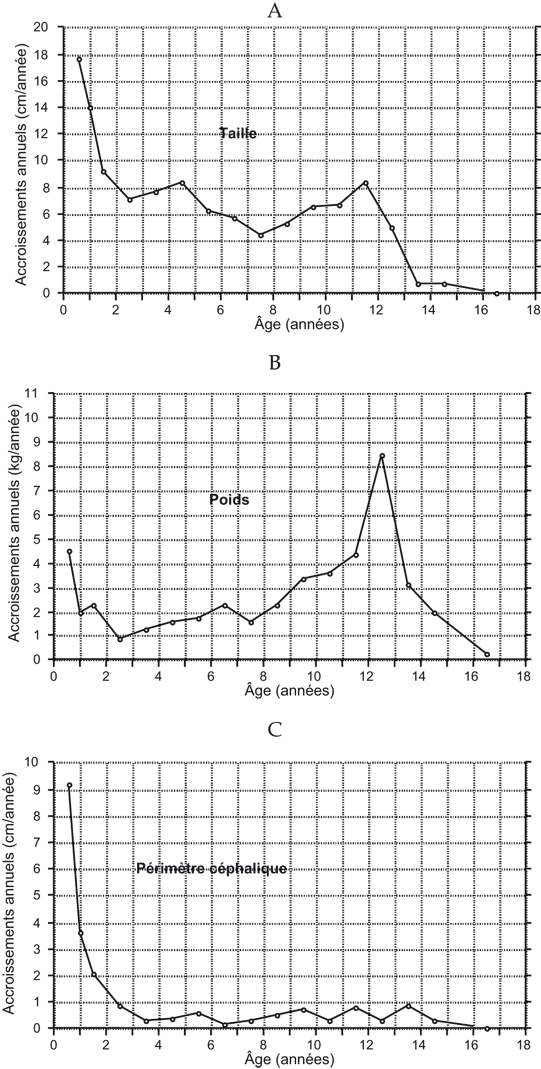
La figure 1.2A

montre que la vitesse de croissance staturale est caractérisée par une période d'accroissement rapide, mais néanmoins décélérante, durant les deux premières années de la croissance postnatale ; elle est suivie d'une période de vitesse de croissance staturale plus ou moins constante, parfois interrompue par un ou plusieurs petits pics de croissance pré-pubertaires (Butler et coll., 1989

; Hauspie et Chrzastek-Spruch, 1993

). Cette période est suivie par la période pubertaire ou l'adolescence, caractérisée par la présence d'un pic de croissance pubertaire.
La croissance du poids diffère de celle de la taille, dans la mesure où le début de la croissance pubertaire n'est pas marqué par un âge auquel la vitesse est minimale. Au contraire, un minimum de la vitesse de croissance pondérale est généralement constaté vers l'âge de 2-3 ans (figure 1.2 B

) (Tanner et coll., 1966a

), après lequel la vitesse augmente graduellement. La courbe de vitesse de croissance du périmètre crânien est caractérisée par une vitesse rapide mais fortement décélérante durant la première année postnatale (figure 1.2 C

). Vers l'âge de 2 ans, la vitesse de croissance chute en dessous de 1 cm/an, et cela pour le reste de la période de croissance. Les dimensions de la tête et du visage ne montrent pas de pic de croissance pubertaire.
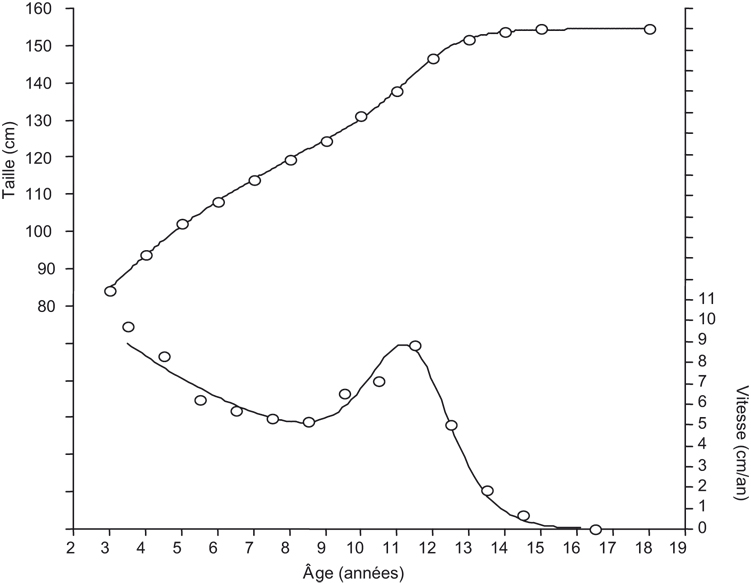
La vitesse de croissance illustre clairement la dynamique de la croissance. La figure 1.3

illustre cette vitesse calculée comme la première dérivée d'un exemple de courbe lissée de croissance de la taille par rapport à l'âge. La figure 1.3

illustre donc le fait que la taille, caractérisée par une période d'accroissement rapide à la naissance, décélère durant les deux premières années (la petite enfance) ; cette période est suivie par une période de vitesse plus stable (légèrement décélérante ou constante) pendant l'enfance, caractérisée parfois par un ou plusieurs petits pics de croissance pré-pubertaires. Cette période de l'enfance est de durée variable selon le sexe et la vitesse de maturation de l'enfant. Cette période est suivie par la période pubertaire ou l'adolescence, caractérisée par une accélération de la croissance staturale et un pic de croissance pubertaire. Après ce pic, la vitesse de croissance staturale diminue rapidement et la croissance se termine à l'âge adulte, atteint actuellement vers 16-17 ans chez les filles et 18-19 ans chez les garçons. Naturellement, les facteurs de variation sont multiples, entre populations, entre individus et entre les deux sexes ; cette variation concerne aussi bien le
timing de développement que la taille elle-même à chaque âge.
Les études longitudinales, basées sur des mesures séquentielles, permettent de décrire avec précision ces modes de croissance. Les courbes de croissance peuvent être considérées comme « lisses », même si des études récentes, basées sur des techniques précises (telles que la knémométrie) et des mesures fréquentes (journalières ou hebdomadaires), indiquent des irrégularités de rythme de croissance (Hermanussen, 1998

; Lampl, 1999

).
De nombreux modèles mathématiques (plus de 200 fonctions) ont été proposés pour décrire et lisser la courbe de croissance (Marubini et Milani 1986

; Bogin, 1988

; Hauspie, 1989

et 1998a

). Les avantages et désavantages des modèles les plus utilisés ont été envisagés par Hauspie et coll. (1991

) et par Hauspie et Chrzastek-Spruch (1999

). Le modèle I de Preece et Baines (PB1) est très couramment utilisé pour décrire la croissance de la taille et des dimensions post-crâniennes entre l'âge de 2-5 ans et l'âge adulte (Preece et Baines, 1978

) ; la fonction logistique triple (Bock et Thissen, 1980

) et le modèle JPA-2 (Jolicoeur et coll., 1992

) le sont lorsque la courbe est étudiée à partir de la naissance.
Des données biologiques, telles que l'âge de la vitesse minimale juste avant le pic de croissance pubertaire, l'âge au pic de croissance pubertaire, la vitesse de croissance à ces âges, et la durée du pic de croissance pubertaire, peuvent être estimées par le modèle I de Preece et Baines (PB1). Le modèle PB1 permet donc une interprétation fonctionnelle de la courbe de croissance :
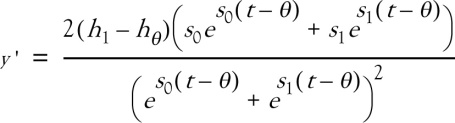
où y =taille en cm, t=âge en années, et h1, hθ, s0, s1, θ sont les cinq paramètres de la fonction. Le paramètre h1 correspond à l'asymptote supérieure de la fonction et représente donc une estimation de la dimension finale. hθ est la dimension atteinte à l'âge θ. Les paramètres s0 et s1 sont des constantes de vitesse, contrôlant respectivement la vitesse de croissance pré-pubertaire et pubertaire. La modélisation est donc une technique qui permet de résumer l'étude longitudinale de la croissance d'un individu en un petit nombre de paramètres ; les moyennes de ces paramètres au niveau d'une population, introduites dans le modèle mathématique, permettent de calculer une courbe de croissance lisse caractéristique de cette population et la courbe de vitesse de croissance instantanée est obtenue par la première dérivée de la fonction. Dans le cas du modèle PB1, la courbe de vitesse de croissance est :
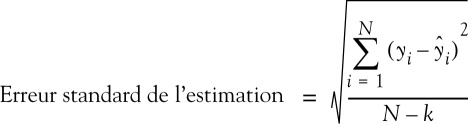
La figure 1.3

illustre l'ajustement du modèle PB1 et les accroissements annuels ainsi que la courbe de vitesse de croissance instantanée. Les valeurs des paramètres du modèle PB1 figurent dans le tableau 1.I

. L'erreur standard de l'estimation, qui correspond à la racine carrée de la variance résiduelle, est souvent utilisée comme une mesure de la qualité de l'ajustement.
Erreur standard de l'estimation
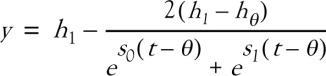
avec
yi la taille à l'âge
xi,

la valeur de la courbe ajustée à l'âge
xi,
N le nombre de mesures de la taille, et
k le nombre de paramètres dans le modèle (5 dans le cas du modèle PB1).
« On considère l'ajustement d'un modèle de croissance comme adéquat, si l'erreur standard de l'estimation est de l'ordre de l'erreur de mesure de la variable en question (typiquement 0,5 cm pour la taille). Au contraire, un biais systématique dans l'ajustement peut être estimé par un test de « runs », par exemple (Siegel, 1956

) » (Hauspie, 2003

).
Pour d'autres caractères corporels, tels que le poids, l'indice de la masse corporelle (IMC ou BMI) et les plis cutanés, des modèles non-structurels, comme des fonctions polynomiales, sont plus utilisés (Largo et coll., 1978

; Gasser et coll., 1984

).
Au niveau de la puberté, ces modèles sont donc particulièrement utiles puisqu'ils permettent d'estimer des paramètres biologiques tels que l'âge, la dimension et la vitesse au début du pic de croissance pubertaire et au moment de la vitesse maximale lors de l'adolescence.
Tableau 1.I Paramètres de la fonction et paramètres biologiques obtenus par l'ajustement du modèle 1 de Preece et Baines (PB1) aux données longitudinales de la Fille n° 29 de l'Étude Belge de la Croissance de l'Enfant Normal (d'après Hauspie, 2003)
|
Paramètres de la fonction
|
Paramètres biologiques
|
|
h1
|
154,4 cm
|
|
hθ
|
143,7 cm
|
|
S0
|
0,1374
|
|
S1
|
1,450
|
|
θ
|
11,63 années
|
|
Variance résiduelle
|
0,144 cm2
|
|
Erreur standard de l'estimation
|
0,380 cm
|
|
Âge au début du pic
|
8,33 années
|
|
Taille au début du pic
|
121,2 cm
|
|
Vitesse au début du pic
|
5,1 cm/an
|
|
Âge à la vitesse maximale
|
11,18 années
|
|
Taille à la vitesse maximale
|
139,8 cm
|
|
Vitesse maximale
|
8,9 cm/an
|
|
Accroissement pubertaire
|
33,2 cm
|
Comme nous l'avons déjà indiqué, les facteurs de variation sont nombreux et ne concernent pas uniquement des variations de taille atteinte à chaque âge, mais également le rythme de croissance, et la vitesse avec laquelle un individu atteint sa taille finale. Cette vitesse de maturation est corrélée à d'autres marqueurs de maturation, tels que les caractères sexuels secondaires ou l'âge osseux.
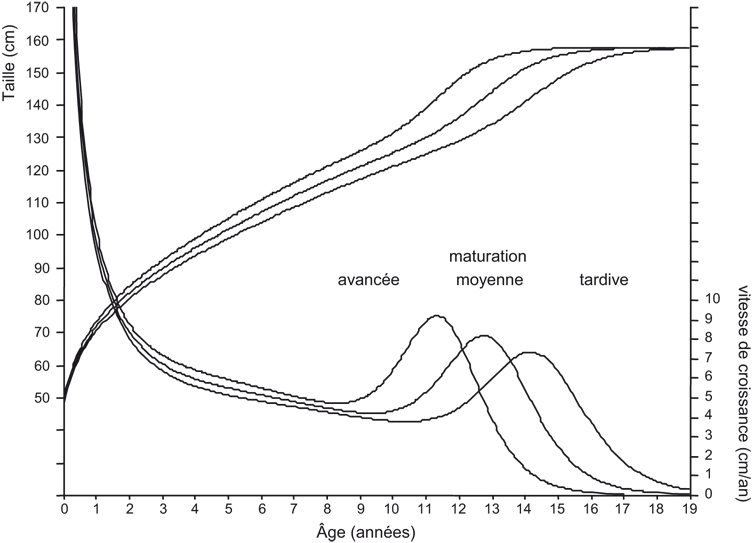
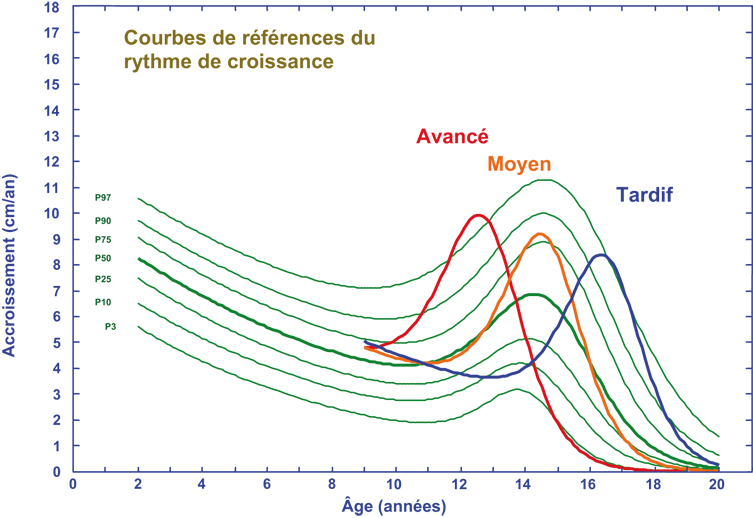
La figure 1.4

illustre un exemple théorique soulignant les effets principaux de la variation du rythme de croissance sur la forme de la courbe de croissance. Le graphique montre la taille atteinte, ainsi que la vitesse de croissance de la taille, pour des enfants à maturation avancée, moyenne et tardive, ayant la même taille à la naissance et à l'âge adulte. Ces trois sujets théoriques ont le même potentiel pour atteindre une certaine taille finale, mais ils diffèrent considérablement en ce qui concerne le temps nécessaire pour arriver à cette maturation complète. Par conséquent, on observe des différences considérables de la taille et de la forme de la courbe de croissance entre ces trois degrés de rythme de croissance tout au long de la période de l'enfance et surtout à l'adolescence. L'effet de différences de rythme de croissance sur la taille atteinte est d'autant plus grand que l'enfant devient plus âgé et que la pente de la courbe de croissance est plus aiguë, ce qui explique que l'effet de différences de rythme de croissance sur la taille atteinte est plus prononcé lors du pic de croissance pubertaire (Hauspie, 2003

).
Cet exemple est théorique mais correspond cependant au fait que dans des populations réelles, il n'y a quasiment pas de corrélations entre la taille finale et l'âge auquel s'installe le pic de croissance pubertaire (Largo et coll., 1978

; Cameron et coll., 1982

; Zacharias et Rand, 1983

; Marshall et Tanner 1986

; Malina et Bouchard, 1991

; Beunen et coll., 1994

; Bielicki et Hauspie, 1994

; Qin et coll., 1996

; Gasser et coll., 2001

). Ainsi par exemple, les enfants à maturation avancée ont une période de croissance moins longue mais une vitesse de croissance plus élevée pendant l'enfance et, surtout au moment du pic de croissance pubertaire. Au contraire, des enfants à maturation tardive auront une période de croissance plus longue mais le pic de croissance pubertaire sera moins élevé. Il existe donc une corrélation négative entre la vitesse maximale lors du pic de croissance pubertaire et l'âge auquel cette vitesse maximale est atteinte : ceci est le cas pour la taille et bien d'autres caractères (Tanner et coll., 1976

; Largo et coll., 1978

; Hauspie, 1980

).
Normes de croissance
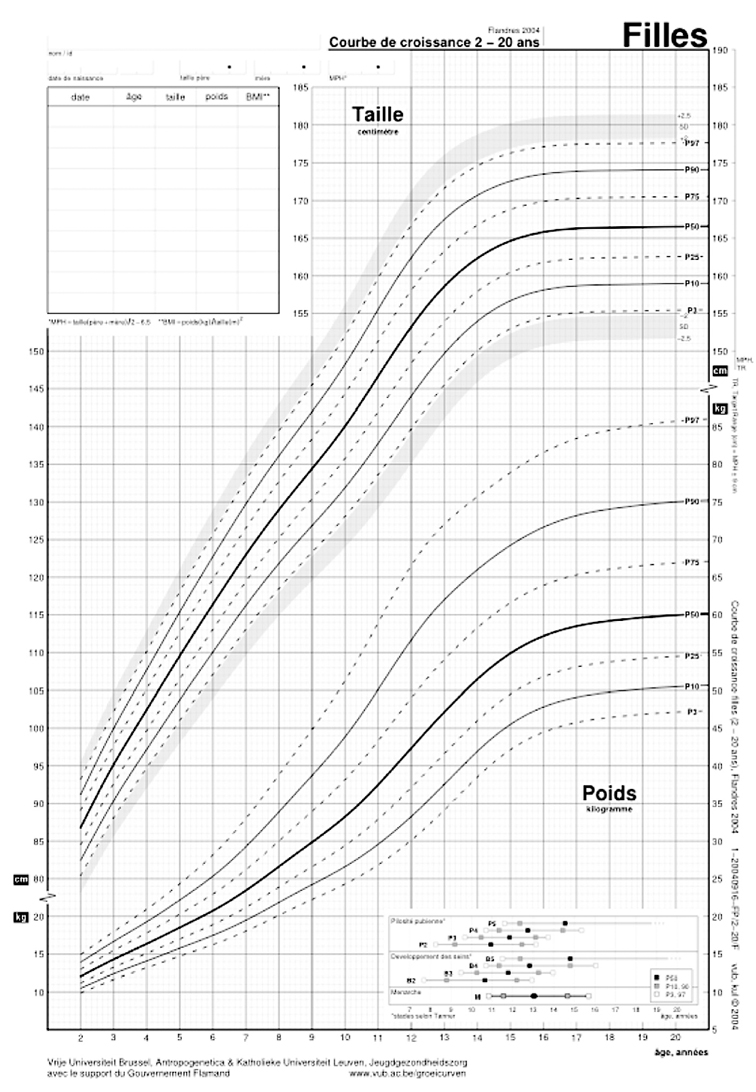
Si ce que nous avons décrit provient essentiellement d'études longitudinales, la majorité des études de croissance sont en fait transversales, c'est-àdire réalisées à partir de mesures uniques prises chez des sujets différents à chaque âge. Les résultats des études transversales peuvent être intéressants également, car ils permettent d'estimer la tendance centrale d'une population et la variation de données de croissance à chaque âge. C'est aussi à partir de données transversales que des courbes percentilées (ou normes de croissance ou courbes de référence) sont établies, illustrant la croissance « moyenne » et les limites de la variation « normale » dans une population. Ces études transversales de la croissance sont donc intéressantes au niveau épidémiologique et au niveau de l'analyse de l'influence des facteurs génétiques et mésologiques. Les figures suivantes illustrent les courbes percentilées établies récemment pour la population flamande (Belgique) pour la taille et le poids (figure 1.5

) et pour l'IMC (figure 1.6

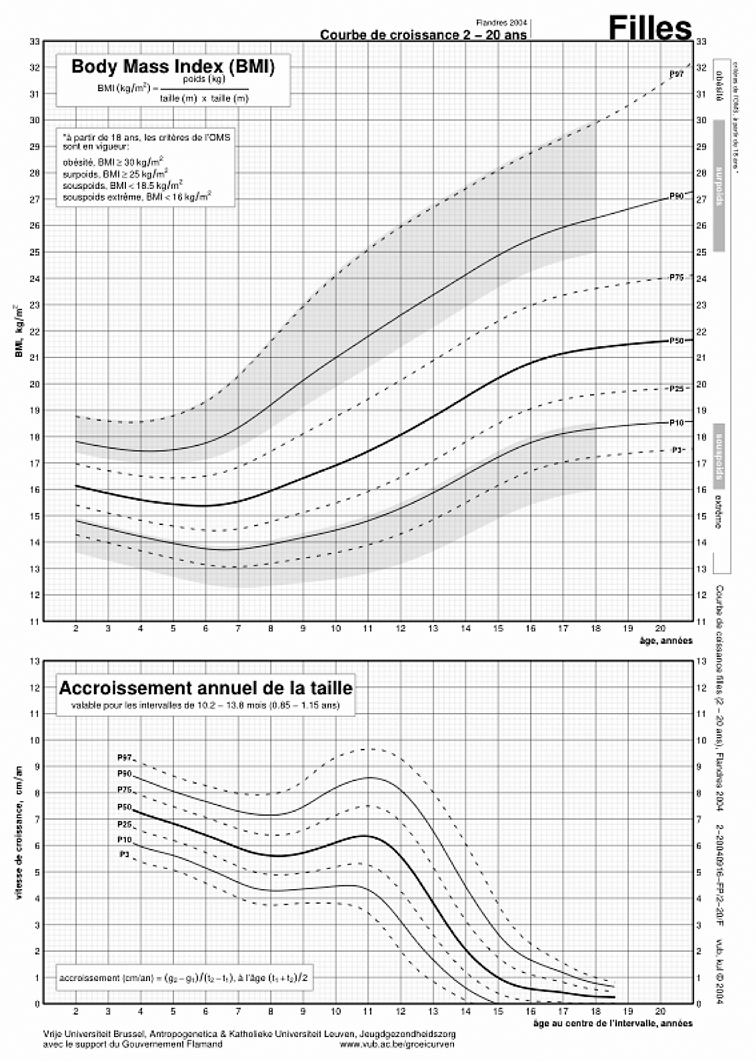
) (Hauspie, 2005

).
Cependant, ces courbes ne permettent pas d'analyser la dynamique du processus de croissance individuel. Elles sont statiques et leur caractère moyen atténue les caractéristiques de la poussée de croissance pubertaire. Ainsi, dans la courbe d'accroissement des moyennes (il ne s'agit donc pas d'une vitesse), la hauteur du pic de croissance pubertaire est réduite, et la poussée de croissance pubertaire est également beaucoup plus étalée. La figure 1.6

illustre ces courbes d'accroissement des moyennes pour la même population que la figure 1.5

. L'allure d'une courbe moyenne d'une étude transversale diffère nettement de celle de courbes individuelles longitudinales. Pendant la puberté, la courbe de croissance d'un enfant ne suit pas une des lignes percentilées des normes de croissance transversale et ces lignes percentilées ne permettent pas d'évaluer la normalité de l'évolution de la croissance dans le temps. Cependant, on peut tenir compte dans des courbes de référence de ces différences de rythme de croissance (Tanner et coll., 1966a

et b

). Wachholder et Hauspie (1986

) et Hauspie et Wachholder (1986

) ont par exemple utilisé des courbes de « constantes-moyennes » pour estimer l'allure typiquement moyenne (Hauspie, 1989

), alors que les courbes de référence pour les enfants à maturation avancée ou tardive étaient obtenues par une analyse de régression des paramètres du modèle Preece et Baines (PB1) sur l'âge à la vitesse maximale lors de la puberté (Wachholder et Hauspie, 1986

; Hauspie et Wachholder, 1986

). La figure 1.7

illustre de telles courbes pour la population de Sarsuna-Barisha (Hauspie et coll., 1980

).
Dimorphisme sexuel
Des différences de croissance entre les deux sexes existent à tous les âges, c'est-à-dire dès la vie fœtale jusqu'à l'adulte, mais elles sont peu prononcées avant la puberté. Le dimorphisme sexuel des caractéristiques anthropométriques s'établit essentiellement pendant la période pubertaire. En termes de courbe de croissance moyenne de taille, les dimensions corporelles sont légèrement supérieures chez les garçons pendant l'enfance, puis il y aura une période d'à peu près deux ans où les filles auront des dimensions plus élevées que celles des garçons (en raison des poussées de croissance pubertaire plus précoces des filles) ; enfin au moment de leur puberté, les garçons deviennent plus grands que les filles pour quasiment toutes les dimensions corporelles.
À nouveau, les données longitudinales permettent de mieux comprendre comment ce dimorphisme sexuel s'établit au cours du processus de croissance (Tanner et coll., 1976

; Hauspie et coll., 1985

; Hauspie, 1986

; Koziel et coll., 1995

). En effet, en comparant les courbes de constantes moyennes des garçons et des filles, obtenues après ajustement d'un modèle mathématique aux sujets individuels de l'échantillon, on peut décomposer le dimorphisme sexuel de la taille adulte en trois parties :
• la différence d'accroissement pubertaire entre les deux sexes ;
• la différence de croissance pré-pubertaire, c'est-à-dire à l'âge où les filles commencent leur poussée de croissance pubertaire ;
• la différence de croissance due à la croissance pubertaire plus tardive des garçons, c'est-à-dire le gain de croissance acquis par les garçons entre l'âge du début de la poussée de croissance pubertaire des filles et des garçons.
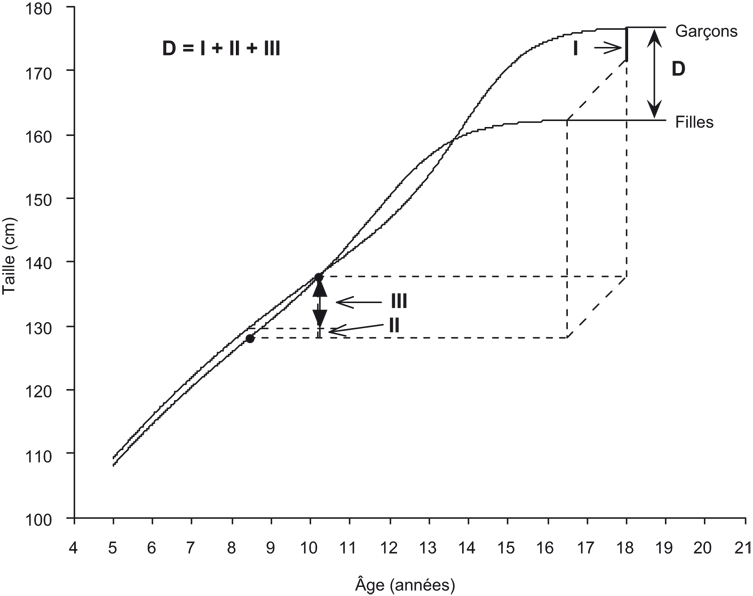
La figure 1.8

montre les courbes de constantes moyennes pour la population belge. Le début de la poussée de croissance pubertaire est indiqué par les points noirs, alors que l'accroissement pubertaire est la croissance acquise depuis le début de la poussée de croissance pubertaire jusqu'à la taille finale.
Le tableau 1.II

montre les résultats d'une telle analyse pour la population belge en ce qui concerne la taille et la taille assis (Hauspie, 2003

).
Tableau 1.II Décomposition du dimorphisme sexuel de la taille et de la taille assis en trois composantes additives (population belge : Koziel et coll., 1995)
La partie I est due à la différence d'accroissement pubertaire, la partie II est due à la différence de croissance pré-pubertaire, et la partie III à la différence due au retard de l'installation de la poussée de croissance pubertaire chez les garçons
| |
Taille (cm)
|
Taille assis (cm)
|
|
Dimorphisme
|
13,5
|
6,5
|
|
I
|
4,9
|
2,8
|
|
II
|
0,4
|
0,5
|
|
III
|
8,2
|
3,2
|
Le tableau 1.II

indique que le dimorphisme sexuel de la taille adulte était de 13,5 cm dans la population belge, décomposé en 0,4 cm de différences pré-pubertaires de taille, 4,9 cm de pic pubertaire plus élevé chez les garçons et surtout 8,2 cm dû au retard dans le
timing de la poussée de croissance pubertaire chez les garçons.
Loesch et coll. (1995

) ont suggéré que le début plus précoce de la puberté chez les filles est associé à une sécrétion plus précoce d'œstrogènes, qui accélère plus la maturation squelettique que la croissance en taille, et réduit donc le gain en taille pendant la période pubertaire. Chez les garçons, la testostérone stimule la croissance en taille et accélère la maturation squelettique.
Des tendances similaires s'observent pour la taille assis, alors que la largeur des épaules est plus grande chez les garçons dû à un plus grand accroissement pubertaire. Pour la largeur des hanches, le dimorphisme est quasiment inexistant avant la puberté ou à l'âge adulte ; en effet, l'accroissement pubertaire est plus important chez les filles mais il est quasiment entièrement compensé par le gain en largeur des hanches chez les garçons en raison de leur période de croissance pré-pubertaire prolongée (Hauspie et coll., 1985

).
Modèle multifactoriel
Les paramètres de croissance correspondent à un modèle multifactoriel sous influence de facteurs génétiques polygéniques mais aussi de facteurs mésologiques.
Au niveau génétique, des études longitudinales de la croissance dans des échantillons de jumeaux ou des échantillons familiaux ont clairement démontré que le rythme de croissance est déterminé génétiquement (Hauspie et coll., 1982

; Sharma, 1983

; Mueller, 1986

; Byard et coll., 1993

; Hauspie, 1998b

). Ainsi, une étude de Hauspie et coll. (1994

) sur des jumeaux monozygotes et dizygotes montre une composante génétique importante, en particulier dans la variation de l'âge au pic de croissance pubertaire. L'influence génétique peut être évaluée par un cœfficient d'héritabilité, défini comme la proportion de la variation due aux facteurs génétiques par rapport à la variation totale. Cependant, dans l'examen des relations familiales, à la composante génétique s'ajoute la transmissibilité culturelle et mésologique.
L'influence des conditions mésologiques est aussi abondamment illustrée. Dans des conditions de vie médiocre, la croissance et le développement peuvent être freinés, pour permettre ainsi à l'enfant de mieux répondre à ses besoins physiologiques et métaboliques. Lorsque les conditions environnementales s'améliorent, on observera une période de croissance de rattrapage jusqu'au moment où la trajectoire originale de sa croissance est à nouveau atteinte (Tanner, 1986

; Golden, 1998

). Mais si la période de stress dure trop longtemps, la croissance répondra à un modèle de maturation tardive. Les exemples sont nombreux, que ce soit pour des raisons de malnutrition chronique mais légère (Hansen et coll., 1971

), des raisons médicales de maladies chroniques comme l'asthme (Hauspie et coll., 1977

et 1979

), des raisons de stress psychosocial (Widdowson, 1951

; Powell et coll., 1967

; Skuse, 1998

), des raisons de milieu familial socialement défavorisé (Bielicki, 1986

), ou encore chez des enfants vivant à haute altitude (Malik et Hauspie, 1986

). « Tous ces enfants sont légèrement en retard pour atteindre leur poussée de croissance pubertaire, la maturation sexuelle et la taille finale. Au contraire, la taille finale n'est, en moyenne, pas réduite (c'est-à-dire conforme à la moyenne de la population), sauf si les conditions contraignantes sont trop sévères (Froment, 1986

; Tanner, 1986

) » (Hauspie, 2003

).
Évolution séculaire en Europe
Les anthropologues ont de longue date illustré les changements séculaires de la croissance en liaison avec les processus d'industrialisation et de modernisation. En effet, on observe dans les pays européens depuis le XIX
e siècle, une croissance et un développement plus rapides, des tailles moyennes plus élevées et une maturation plus précoce (Bodzsar et Susanne, 1998

; Susanne et coll., 2001

) (figures 1.9

et 1.10

).
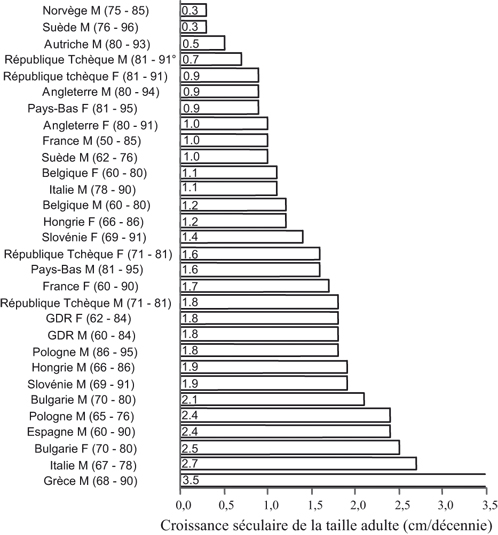
Bodzsar et Susanne (1998

) ont montré que l'évolution séculaire de la taille continue à être observée dans la plupart des régions européennes (figure 1.11

) : elle est plus faible dans les pays nordiques comme la Suède et la Norvège (de l'ordre de 0,3 cm par décennie) et plus élevée dans les pays de l'est et du sud (2,5 cm par décennie en Pologne, Espagne, Bulgarie, Italie et 3,5 cm par décennie en Grèce). En Europe occidentale, elle reste de l'ordre de 1 cm par décennie (Hauspie et coll., 1997

).
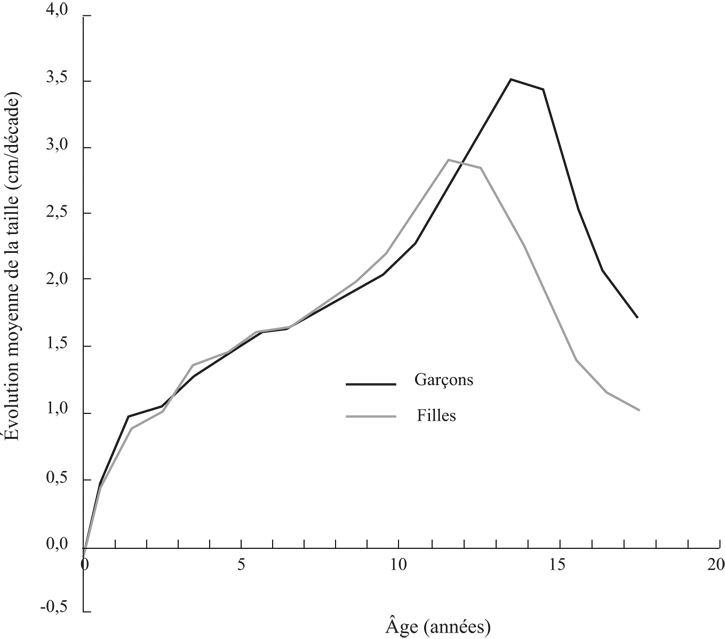
L'évolution séculaire peut s'observer en trois périodes distinctes : avant 2 ans où l'évolution est faible ; de 2 ans à la puberté, où l'évolution est plus élevée liée à l'accélération pubertaire ; et post-pubertaire où l'évolution atteint celle de l'âge adulte (figure 1.12

).
Évolution séculaire de la taille
À la naissance, les changements séculaires sont négligeables (Ward et Ward, 1984

; Garn, 1987

; Rosenberg, 1988

). Ils prennent place cependant dès les premières années de vie, mais l'évolution séculaire de la taille est souvent plus élevée durant la période pubertaire : Eveleth et Tanner (1990

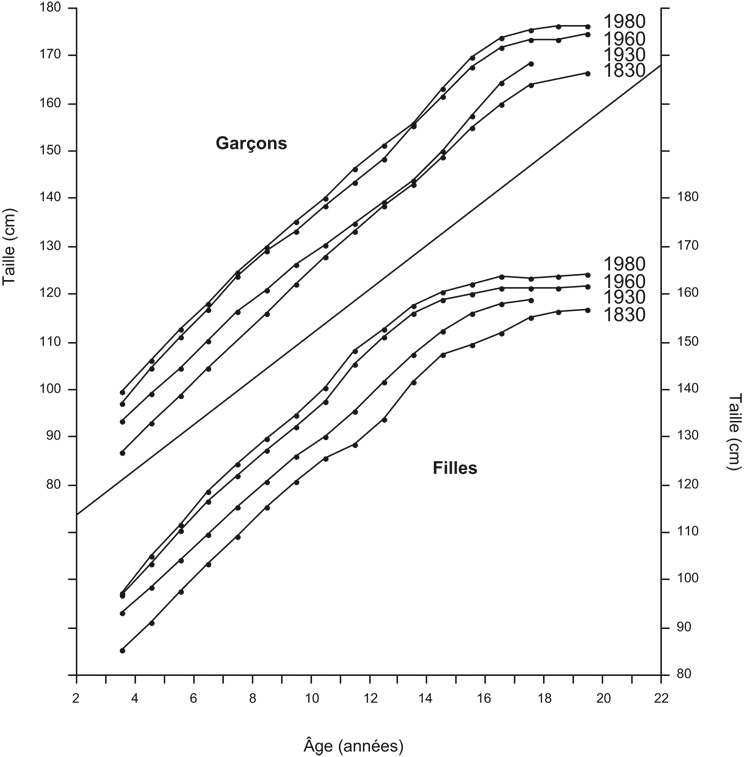
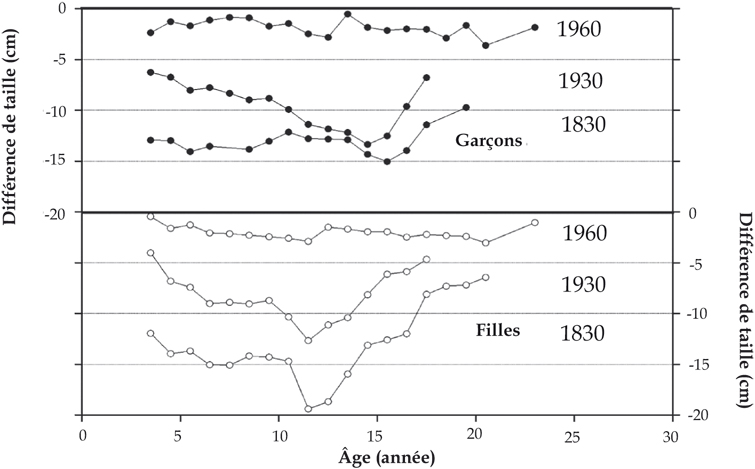
) évaluent, pour la période 1880-1980, les changements à 1,5 cm par décennie pendant l'enfance, 2,5 cm par décennie pendant la puberté et à 1 cm par décennie à l'âge adulte. En fait, cette observation est liée au développement pubertaire progressivement plus précoce. Ainsi, la figure 1.13

relative à l'évolution séculaire en Belgique montrant les différences entre les données de 1980 avec celles de 1960, 1930 et 1830, met en évidence des différences plus élevées pendant l'âge de la puberté mais uniquement par rapport à 1930 et 1830 où l'augmentation est due à l'accroissement de taille mais aussi à une accélération de tempo. Au contraire, par rapport à 1960, les différences observées sont du même ordre de grandeur : dans ce cas, les différences ne sont plus dues qu'à l'accroissement de taille.
Dans d'autres régions européennes, le changement séculaire n'est également pas plus élevé pendant la puberté que pendant l'enfance, c'est le cas pour la Norvège et la Pologne (au niveau urbain). Cette observation n'est cependant pas encore générale, les données tchèques, slovènes, polonaises et celles de Jena témoignent encore d'un effet d'accélération (Bodzsar et Susanne, 1998

).
Couplée aux changements de rythme de croissance, la durée du processus de croissance diminue. Certains moments de cette croissance se déroulent donc plus précocément, comme le début de la croissance pubertaire, l'âge au pic de croissance pubertaire.
L'évolution séculaire ne s'est naturellement pas réalisée de manière linéaire : ainsi, pour la Belgique, et l'âge au pic de croissance pubertaire (PHV) estimé par le modèle Preece et Baines, l'évolution a été lente de 1830 à 1920 (0,34 mois/décennie), plus rapide de 1930 à 1960 (3,44 mois/décennie) et plus lent à nouveau à partir de 1960 (1,14 mois/décennie) (Susanne et Vercauteren, 1997

; Vercauteren, 2003

).
Actuellement, l'évolution séculaire de la taille à l'âge adulte se ralentit ou est même stoppée dans certains pays européens. Deux raisons peuvent expliquer cette décélération, soit que les conditions mésologiques sont devenues optimales pour l'expression complète du génotype, soit que les conditions mésologiques cessent de s'améliorer dans les dernières décennies (Susanne et Bodzsar, 1998

; Hauspie et Vercauteren, 2004

).
L'évolution séculaire de la taille est essentiellement liée à celle de la longueur des membres inférieurs (Himes, 1979

; Tanner et coll., 1982

; Vercauteren et coll., 1983

; Tanner, 1990

; Susanne, 1993

; Takaishi, 1995

).
Certains auteurs (Eveleth et Tanner, 1990

; Kuh et coll., 1991

) mentionnent une plus grande plasticité des garçons, c'est-à-dire que les garçons seraient plus plastiques aux changements mésologiques, seraient plus affectés par de mauvaises conditions et croîtraient plus rapidement lorsque les conditions sont favorables.
Évolution séculaire d'autres mensurations
L'évolution séculaire ne se limite naturellement pas à la taille mais implique l'ensemble des dimensions et des proportions corporelles. Par rapport à la taille, le diamètre biacromial, la longueur des bras et les dimensions thoraciques diminueraient.
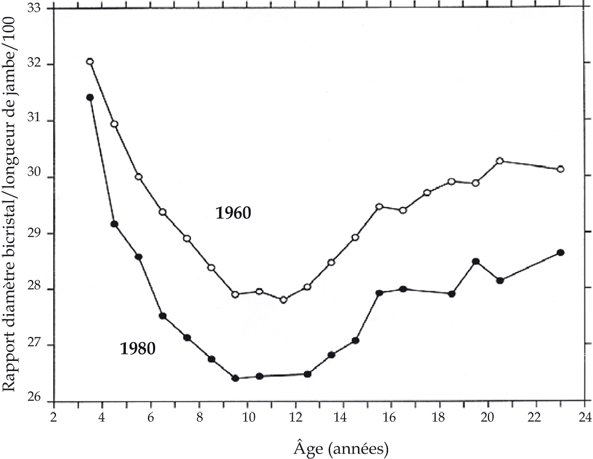
Concernant les diamètres du bassin, la littérature est contradictoire (Susanne et Bodzsar, 1998

; Susanne et coll., 2001

) mais indique souvent un type de silhouette plus longiligne, comme en Belgique (Susanne, 1993

; Vercauteren et coll., 1998

), Suède (Lindgren, 1998

) et Allemagne (Jaeger, 1998

) (figure 1.14

), bien que des différences régionales et socioéconomiques existent.
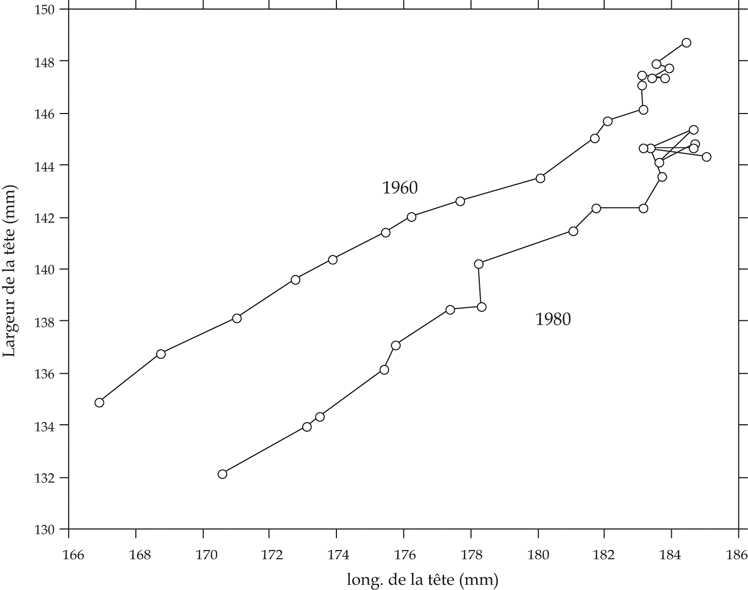
Au niveau des dimensions céphaliques, des changements séculaires s'observent aussi, comme une face plus étroite, une réduction de la largeur céphalique combinée à une augmentation de la longueur céphalique, et donc connue sous le nom de débrachycéphalisation : ces observations concernent notamment la Belgique (Vercauteren et coll., 1983

; Susanne et coll., 1988

; Vercauteren et coll., 1998

), la Bulgarie (Stoev et Yordanov, 1998

), la France (Demoulin, 1998

), l'Allemagne (Jaeger, 1998

), la Hongrie (Gyenis, 1994

) et la République tchèque (Vignerova et Blaha, 1998

) (figure 1.15

).
Évolution séculaire du poids
Avec l'évolution séculaire de la taille, il est normal d'observer des changements de poids, aussi bien chez les enfants que les adultes (Liestol et Rosenberg, 1995

; Susanne et coll., 2001

).
Cependant, dans les périodes 1970, un poids relatif moins élevé a été observé comme en Tchéquie (Vignerova et Blaha, 1998

, pour les filles de plus de 15 ans), en Slovénie (Stefancic et Tomazo-Ravnik, 1998, à partir de 13 ans), en Belgique (Susanne, 1993

; Hauspie et coll., 1997

, à partir de 13 ans) et à Jena (Jaeger, 1998

, aux tailles supérieures à 150 cm).
À partir des années 1980, des travaux démontrant une tendance inverse vers un alourdissement relatif ont été publiés par Cernerud (1993

) et Lindgren (1998

) pour la Suède, Liestol et Rosenberg (1995

) pour la Norvège, Rona (1998

) pour l'Angleterre, Sorensen et Price (1990

) pour le Danemark, Kiess et coll. (2001

) pour l'Allemagne (ces auteurs observent une augmentation du 97
e percentile alors que le 3
e percentile reste constant) ainsi que Zellner et coll. (2004

) pour l'Allemagne (figure 1.16

).
Cela reflète l'épidémie croissante d'obésité observée dans le monde occidental. Elle est le plus souvent documentée par une augmentation d'IMC (ou de plis cutanés ou de circonférences) : son évolution suit un autre timing que celle de la taille et répond manifestement à une autre étiologie.
L'obésité adulte manifeste des signes d'augmentation depuis les années 1970 en Europe, mais seulement après 1980 chez les enfants ; ces signes sont apparus plus tôt aux États-Unis (Bielicki et coll., 2000

). L'obésité est actuellement observée à des âges de plus en plus jeunes (Bundred et coll., 2001

; Zellner et coll., 2004

).
L'évolution du poids à la naissance est peu sensible, et ne semble pas suivre un processus d'évolution séculaire. En fait, durant la seconde moitié du XIX
e siècle, on a noté une baisse du poids à la naissance (Ward et Ward, 1984

; Rosenberg, 1988

). Au XX
e siècle, il est resté stable mais il existe des signes récents aux États-Unis d'une augmentation, liée probablement à l'obésité maternelle (Alberman, 1991

) et à une augmentation de diabète gestationnel.
Diverses populations ne présentent pas d'évolution séculaire, il s'agit essentiellement de pays en voie de développement comme les Yucatec Maya de Mexico (McCullough, 1982), les Indiens du Guatémala (Bogin et McVean, 1984

), les Khatris en Inde (Sethi et coll., 1995

), les Indiens Xingu au Brésil (Eveleth et coll., 1974

), à Hyderabab en Inde (Shatrugna et Rao, 1987

).
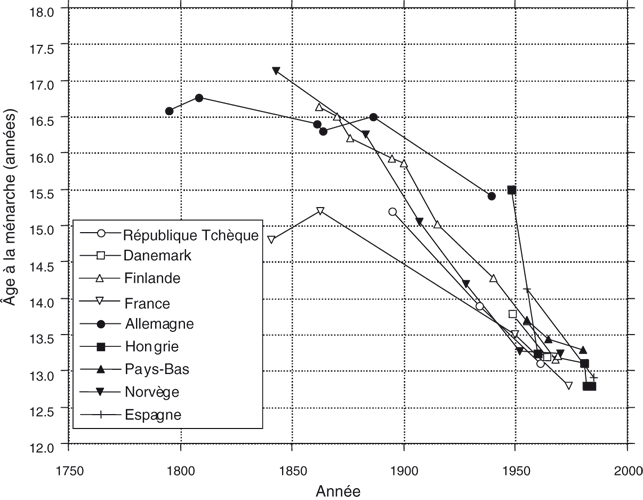
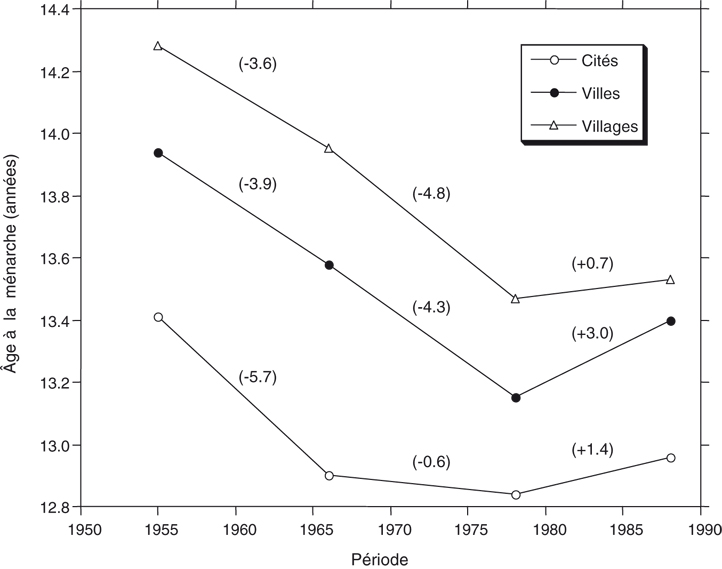
Mais, également en Europe, pendant les périodes mésologiquement difficiles une évolution négative peut être observée. C'est le cas en Pologne, vers les années 1980 pour l'âge à la ménarche (Hulanicka et Waliszko, 1991

) (figure 1.17

) ; c'est aussi le cas en Europe au début du XIX
e siècle pour la taille sous l'effet de la révolution industrielle, et de faibles récoltes (Komlos, 1985

; Floud et coll., 1990

), et également durant les deux guerres mondiales (Eiben, 1989

).
Et en France ?
Une synthèse de l'évolution séculaire en France a été effectuée par Demoulin (1998

). Cette observation d'évolution séculaire est essentiellement basée sur des tailles masculines adultes, à savoir des conscrits de 18-20 ans qui cependant n'ont pas atteint nécessairement leur taille définitive. L'évolution séculaire y est de 0,7 cm par décennie entre 1900 et 1960 et de 1 à 2 cm par décennie entre 1960 et 1990.
Une autre étude française commencée en 1984-1985 dans les mêmes conditions que l'étude de référence française (Sempé et coll., 1979

) a montré que les enfants actuels sont plus grands et ont un poids plus élevé. Elle montre également un avancement du rebond d'adiposité et une vitesse augmentée de la croissance au début de la vie (Deheeger et Rolland-Cachera, 2004

; Rolland-Cachera et coll., 2006

).
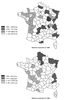
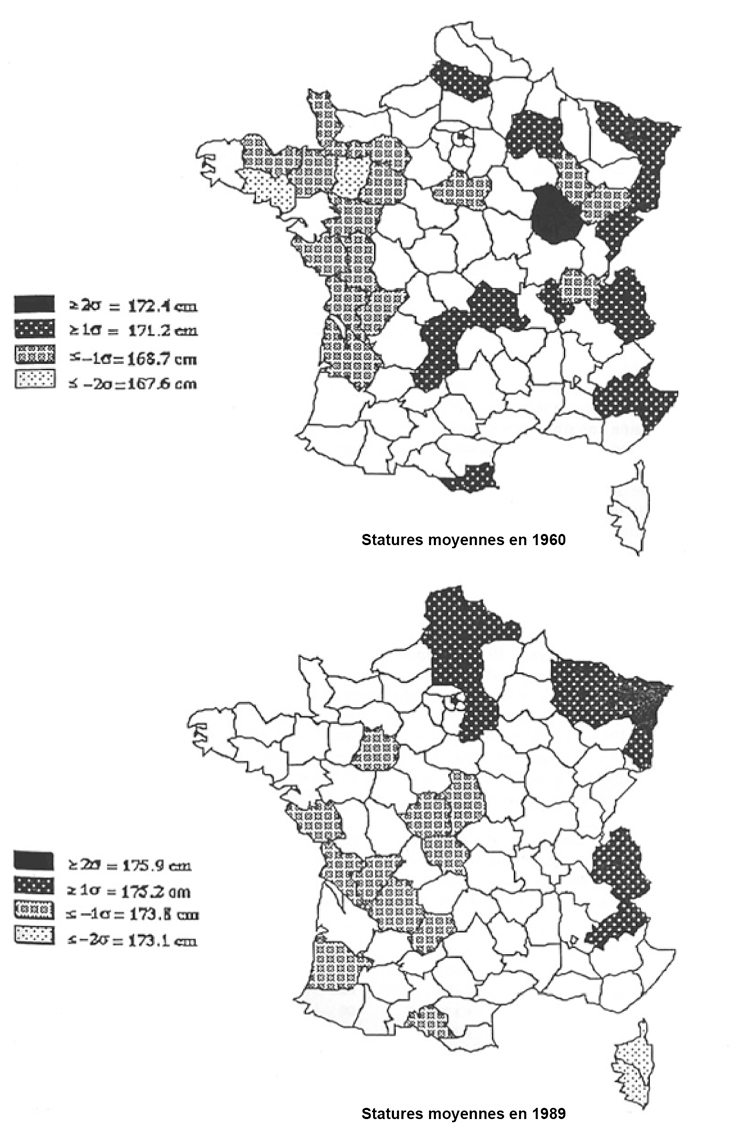
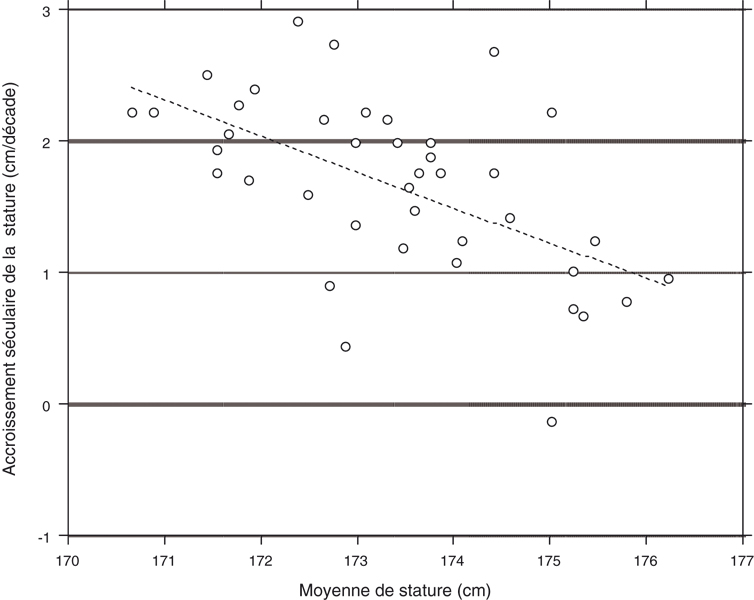
L'analyse de moyennes de taille masculine par département montre, à part une hétérogénéité inter-départementale de taille, une augmentation plus élevée entre 1960 et 1989 pour les départements où la taille moyenne était initialement moins élévée, résultant donc en une diminution de l'hétérogénéité inter-départementale en 1989 (Pineau, 1993

). À titre d'exemple, la figure 1.18

illustre la situation en 1989, où un gradient nord-est vers sud-ouest est observé, des tailles les plus élevées au nord et nord-est vers les moins élevées au sud et sud-ouest.
La diminution de l'âge à la ménarche est bien illustrée également, au moins sur la région parisienne. Entre 1840 et 1980, elle a diminué de 2 ans, soit environ 0,15 an par décennie. Elle était en 1980 de 12,8 ans (écart-type : 1,3).
Le mode de croissance a été étudié par trois enquêtes longitudinales dans la région parisienne :
• enfants nés en 1987-1990 et suivis de la naissance à 2 ans (Demoulin, 2003

) ;
• enfants nés en 1984 et suivis de 10 mois à 8 ans (Deheeger et coll., 1994

) ;
• enfants nés de 1953 à 1960 et suivis jusqu'à 21 ans (Sempé et coll., 1979

; Rolland-Cachera et coll., 1991

).
Des études plus récentes concernant des données transversales ou des données longitudinales d'enfants nés après les années 1960 manquent. Les courbes de références de la population française figurant dans le carnet de santé ont été établies à partir de l'étude de Sempé et coll. (1979

) et Rolland-Cachera et coll. (1991

) (voir en annexe 2).
Facteurs affectant l'évolution séculaire
L'évolution séculaire résulte de l'effet combiné d'un accroissement de taille à chaque âge et d'une accélération du processus de croissance : elle s'observe dès les premières années de la vie. La majeure partie de l'évolution séculaire de la taille adulte est d'ailleurs atteinte dès l'âge de 2 ans. L'accélération de la croissance implique pour sa part un raccourcissement de la période totale de croissance, ainsi, l'âge de pic de croissance pubertaire est plus précoce et la taille adulte est atteinte plus tôt également.
Facteurs de taille
Si à 2 ans, la majeure partie de l'évolution séculaire de la taille est atteinte, essentiellement par l'allongement des jambes, il s'agit de la période postnatale à taux de croissance le plus élevé et donc aussi la plus sensible aux conditions mésologiques néfastes. Le phénomène de taille réduite pour l'âge (stunting) est bien connu dans les pays du tiers-monde et il est le plus souvent observé entre 1 et 2 ans.
Il est généralement admis que des changements observés au niveau de la croissance et du développement sont de bons indicateurs des conditions de vie d'une société, en particulier de la situation nutritionnelle et sanitaire (Susanne, 1985

). Tanner (1992

) a même proposé le terme d'épidémiologie auxologique et sa phrase « la croissance est le miroir des conditions de la société » est devenue célèbre.
Le retard de croissance semble lié à trois causes : la nutrition, les infections et l'interaction mère-enfant (Waterlow, 1994

). La génétique jouerait un rôle peu important dans le processus d'évolution séculaire puisque des enfants de milieu favorisé dans le tiers-monde croissent de manière assez semblable à ceux de populations de pays développés (Hauspie et coll., 1980

; Bhandari et coll., 2002

). Les différences observées entre populations différentes mais de niveau socioéconomique élevé sont relativement moins élevées que celles observées entre les niveaux socioéconomiques différents au sein de populations identiques.
Au niveau prénatal, des indicateurs d'influence sur la croissance sont le poids à la naissance et le tabagisme maternel ; au niveau postnatal, ces indicateurs sont notamment la grandeur de la famille, le statut socioéconomique, l'éducation parentale, les conditions de logement, le stress psychosocial et l'âge maternel à la naissance.
Facteurs socioéconomiques
Déjà en 1829, Louis-René Villermé avait noté que les personnes plus riches étaient plus grandes, de même si elles avaient une meilleure nutrition et de meilleures conditions de logement (Tanner, 1981

). Quételet avait fait des observations identiques à Bruxelles ainsi que l'effet délétère du travail infantile sur la taille finale.
L'évolution séculaire traduit donc les conditions de santé d'une population et elle met aussi en évidence des inégalités de santé au sein d'une même population.
Il semble établi également que des facteurs socioéconomiques peuvent aussi influencer les processus séculaires, ainsi les changements séculaires sont plus rapides dans les groupes sociaux défavorisés (Susanne et Heyne, 1972

; Salzer, 1975

; Lindgren, 1976

; Smith et coll., 1980

; Rona et Chinn, 1986

; Vercauteren, 1993

; Weber et coll., 1995

; Hauspie et coll., 1996

et 1997

; Vercauteren et coll., 1998

). Ainsi, en Pologne, l'amplitude des inégalités sociales en terme de moyenne de taille a décliné par une évolution séculaire plus élevée des groupes sociaux les moins favorisés (Bielicki et coll., 1992

et 1998

) (figure 1.19

).
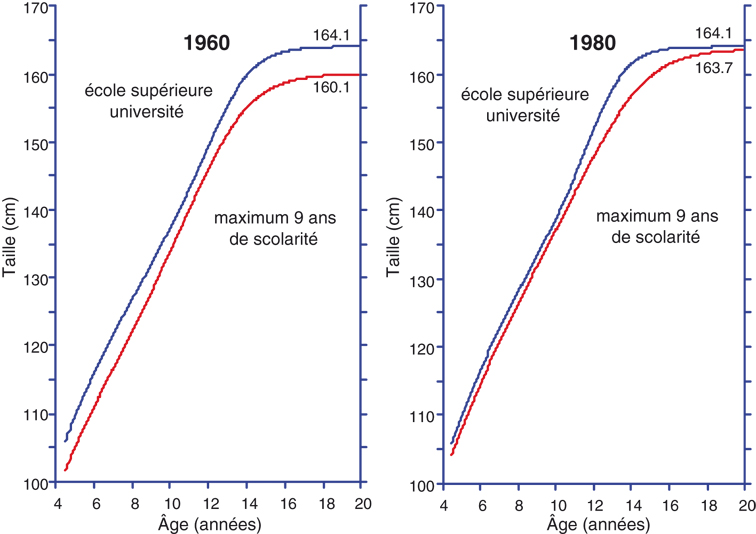
Vercauteren (1993

) démontre également que des enfants belges dont le père a un haut niveau d'éducation (universitaire ou école supérieure) n'ont pas subi une évolution séculaire de taille finale entre 1960 et 1980 alors que ceux dont le père a un niveau d'éducation plus faible (maximum 9 ans de scolarité) subissent une évolution positive de 3,6 cm (figure 1.20

).
Ce phénomène de « récupération » plus importante des groupes socialement défavorisés pourrait s'accompagner d'une évolution séculaire positive plus importante des percentiles peu élevés par rapport aux percentiles élevés. Cette estimation des percentiles peu élevés reste donc importante puisqu'elle détermine le caractère « normal » ou « abnormal » de la croissance (Hauspie et coll., 1996

).
L'influence des facteurs socioéconomiques sur l'évolution séculaire est donc abondamment documentée, comme en ce qui concerne la classe sociale (Kuh et coll., 1991

; Bielicki et coll., 1992

; Bielicki et Szklarska, 1999

; Li et coll., 2004

; Gyenis et coll., 2004

), les revenus et l'éducation (Meyer et Selmer, 1999

), la grandeur de la famille (Chinn et coll., 1989

), les différences ville-campagne (Weber et coll., 1995

; Padez et Johnston, 1999

), la surpopulation de l'habitation (Foster et coll., 1983

).
Tous ces facteurs affectent plus ou moins directement la santé des enfants en croissance par l'intermédiaire du confort environnemental et de l'hygiène.
Les changements séculaires en Europe sont clairement en relation avec l'industrialisation et les changements associés des modes de vie (Vercauteren et Susanne, 1997

) : cela explique que les changements séculaires n'ont pas débuté à la même époque dans les différents pays européens, débutant au XIX
e siècle en Angleterre, après dans des pays comme la Belgique (Vercauteren et coll., 1998

) et les pays scandinaves, seulement au début du XX
e siècle en France (Demoulin, 1998

) et même après en Espagne (Rebato, 1998

).
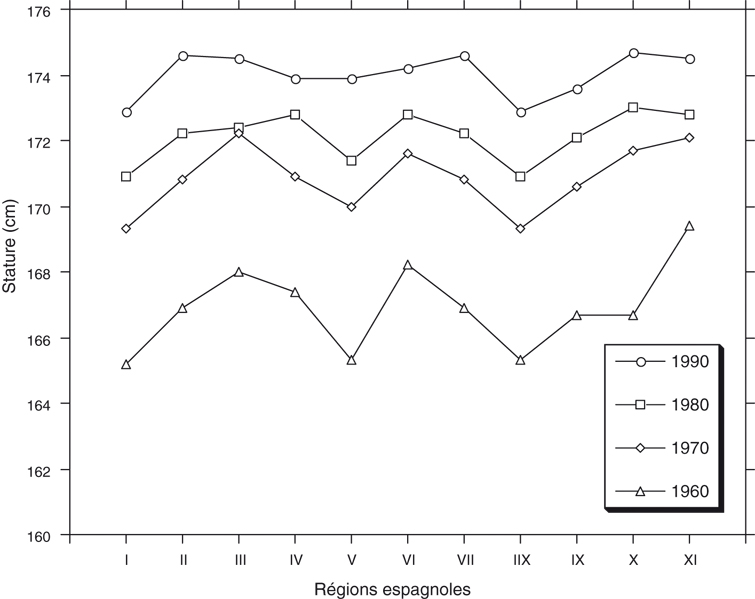
Ces évolutions différentielles amènent également des fluctuations au niveau géographique. Ainsi en Espagne, l'industrialisation a débuté tardivement, essentiellement dans les années 1960 et ceci principalement à Barcelone, Madrid et au Pays Basque donnant lieu à des différences géographiques élevées de moyenne de taille (Rebato, 1998

). L'évolution séculaire fut aussi non uniforme et plus élevée pendant la période 1970-1985. De plus, la variabilité inter-régionale de taille et d'âge à la ménarche diminue régulièrement de 1960 à 1990 (Rebato, 1998

), le taux le plus élevé d'évolution séculaire étant observé pour les régions au départ les plus défavorisées (figure 1.21

).
Dans d'autres cas, une diminution de variabilité inter-régionale a été aussi observée, comme au nord et centre de l'Italie
versus le sud (Floris et Sanna, 1998

) et les différents départements français (Demoulin, 1998

), où l'augmentation de taille a été plus grande dans les régions où au départ les tailles moyennes étaient moins élevées.
Facteurs nutritionnels
Ces changements séculaires de croissance et de développement vont de pair avec des changements de nutrition et d'habitudes alimentaires observés dans une perspective historique, illustrés par van Otterloo (1990

) pour les Pays-Bas, par Facchini et coll. (1982

), Ulizzi et Terrenato (1982

) pour l'Italie, par Ochoa Zamora et coll. (1981

), Tojo et coll. (1987

), Rebato (1998

) pour l'Espagne, et par Bielicki (1986

), Bielicki et coll. (1997) pour la Pologne.
Au niveau pré-industriel, la majorité des habitants vivent de féculents, tels que pommes de terre ou riz. L'apport alimentaire est limité, fluctue en fonction des saisons, ne peut être transporté efficacement et préservé, et des périodes de famine existent. La situation était souvent meilleure en milieu rural qu'urbain. Avec l'industrialisation, la distribution alimentaire devient graduellement meilleure grâce à une amélioration des conditions de transport. La consommation de viande et de graisse augmente lentement, bien que ces aliments étaient trop chers pour les ouvriers, qui dépensaient au moins 2/3 de leur salaire à l'alimentation. La société devient de plus en plus consciente de l'influence de la qualité alimentaire et de l'hygiène sur la santé et la croissance des enfants.
En Europe, après 1900, cette conscience résulte en une attention politique et en certains contrôles gouvernementaux en terme de distribution alimentaire et d'éducation. Les populations urbaines commencent à avoir un meilleur pronostic de croissance que les populations rurales, mais les groupes économiquement pauvres restent extrêmement sensibles. La vulnérabilité de ces groupes socioéconomiques peu favorisés est évidente durant la crise économique des années 1930 et durant les deux guerres mondiales. L'augmentation de richesse ne deviendra évidente qu'à partir des années 1955. Aujourd'hui, les problèmes d'approvisionnement, de transport, de conservation, de distribution ont été résolus. Les aliments de l'ensemble du monde sont disponibles et circulent largement, les fluctuations saisonnières ont disparu, les préparations alimentaires sont plus hygiéniques et seuls environ 15 % des revenus sont consacrés en moyenne à l'alimentation.
La nutrition est clairement un facteur critique. Cependant, en Europe, l'apport nutritionnel n'est probablement plus un facteur limitant. La qualité, plutôt que la quantité, de l'apport nutritionnel est suffisante, à savoir les protéines animales, les micronutriments et les vitamines (Allen et Uauy, 1994

).
À l'appui de cette hypothèse, figurent différentes observations en Europe et au Japon. Les changements nutritionnels ont été conséquents en Europe pendant les dernières décennies. Dans les régions européennes de l'OCDE (1985), des modifications significatives de consommation ont été observées de 1955 à 1988 (Susanne et coll., 1987

; Susanne et Lepage, 1990

et 1992

). Ainsi, la consommation de protéines essentiellement animales a augmenté, ainsi que la consommation de graisse d'origine animale et végétale. L'évolution de la consommation de sucre est plus contrastée ; elle augmente essentiellement dans les pays du sud (Espagne, Italie, Portugal) où elle partait en 1955 de valeur très basse, mais diminue dans les pays nordiques où la valeur de 1955 était élevée. Comparant les changements séculaires de la taille avec la consommation nutritionnelle, certains parallélismes semblent apparaître pour les pays européens (Susanne et coll., 2001

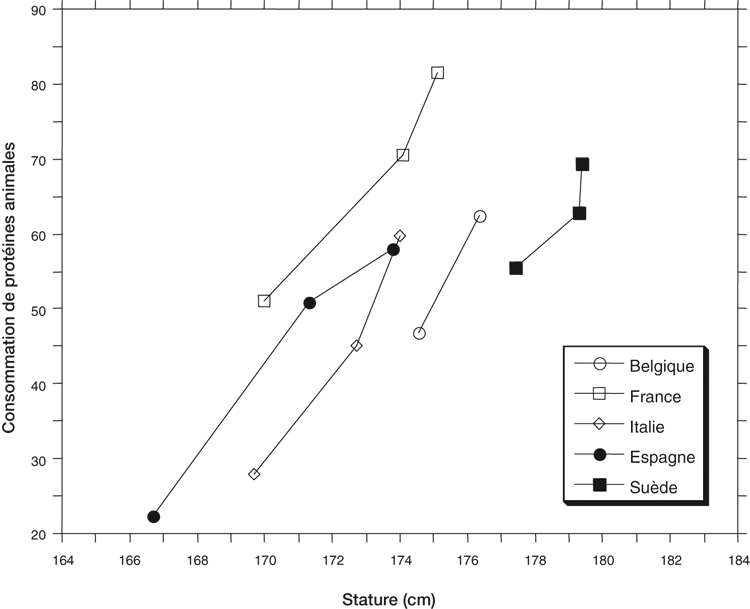
) en termes de consommation de protéines animales (figure 1.22

) mais la relation est moins nette pour les graisses et absente pour le sucre. Aussi, en Galicie (nord-ouest de l'Espagne), des changements très significatifs sont apparus entre 1970 et 1985 avec essentiellement un accroissement de consommation de protéines animales, correspondant aussi à une intensification de l'évolution séculaire (Tojo et coll., 1987

; Rebato, 1998

).
Les différences sociales de consommation nutritionnelle apparaissent également comme en Pologne (Bielicki et coll., 1981

) : en fonction du niveau salarial plus élevé, la consommation de viande, d'œufs, de fromage, de fruits et de légumes augmente. Cette consommation est aussi plus faible dans des familles nombreuses par rapport à des familles de taille plus réduite (Bielicki et coll., 1992

).
Entre l'évolution séculaire de la taille et la consommation nutritionnelle, certains parallélismes semblent donc apparaître :
• pour la Pologne (Bielicki et coll., 1997 ; Sekula et coll., 1997

) en termes de consommation de viande, de graisse et de sucre ;
• pour la Pologne, le lien n'est pas net pour le total de protéines et il est absent pour la pomme de terre ;
• pour d'autres pays européens (OCDE, 1985) en termes de consommation de protéines animales ;
• pour ces mêmes pays, la relation est moins nette pour les graisses et elle est absente pour le sucre.
Au Japon, Takahashi (1984

) lie l'évolution séculaire à la forte augmentation de consommation de lait après la 2
e guerre mondiale.
Les infections interagissent avec la nutrition également par des dommages gastro-intestinaux, de la malabsorption en particulier de micronutriments.
L'appétit est un autre facteur indirect de nutrition par la préparation de la nourriture, l'attention accordée à l'enfant pendant les repas. L'état de santé joue à nouveau un rôle par des réductions d'appétit que la maladie peut provoquer.
L'obésité qui a commencé à apparaître dans les années 1980 chez les enfants et adolescents, est un phénomène lié à l'apport et à l'utilisation d'énergie ; l'alimentation et l'exercice étant donc tous deux impliqués. Lorsque l'utilisation d'énergie diminue (la télévision et la vie sédentaire en sont des facteurs), la possibilité de réguler l'apport nutritionnel est rompue et la réserve de graisse s'accumule.
En conclusion,
l'évolution séculaire ayant trait à des caractères multifactoriels sous contrôle à la fois génétique et mésologique, l'effet de l'hétérosis
1
L'effet d'hétérosis désigne en génétique l'accroissement particulièrement prononcé de la performance des individus hybrides ou métis.
a parfois été postulé (Hulse, 1957

; Wolanski, 1974

). Cette hypothèse trouve son origine dans la mobilité croissante des populations, mobilité à la fois externe et interne, engendrant un plus haut degré d'exogamie. Aucune étude ne met cependant en évidence un lien avec la croissance.
Au niveau génétique, les populations humaines changent continuellement par l'intermédiaire des migrations. Comment considérer ces nouvelles populations ? Pour les études futures de changements séculaires, une solution pourrait être de considérer uniquement les enfants issus de parents autochtones. Cela faciliterait la comparaison avec les données plus anciennes, mais ce ne serait pas tenir compte du devenir d'une population, qui intégrerait les enfants issus de mariages mixtes ou même d'enfants de couples nouvellement nationalisés.
Mais, même dans des populations considérées comme homogènes, l'influence de migrations internes n'est peut-être pas négligeable. Des migrations sélectives, bien que jamais démontrées dans des populations humaines, ne peuvent être exclues. Dans des populations plus hétérogènes, telles qu'en Espagne, France, Italie, la présence de sous-populations doit être considérée.
Il est généralement accepté que les changements de conditions environnementales, et surtout de nutrition, forment les causes principales des changements séculaires (Susanne, 1984

; van Wieringen, 1986). Les facteurs mésologiques, de santé et de nutrition, semblent, en effet, essentiels. Des parallélismes existent entre des changements séculaires et les revenus moyens ou le produit national brut, mais ils existent également pour les facteurs nutritionnels en termes quantitatifs, de consommation de protéines, de graisse et/ou de sucre. Les éléments les plus significatifs semblent être la consommation de viande ou de protéines animales. Des facteurs qualitatifs peuvent aussi avoir une influence, telles qu'une quantité plus importante de protéines animales par rapport à des protéines végétales, des graisses animales par rapport à des graisses végétales, des produits laitiers améliorés en vitamines, du calcium et du phosphore, des changements nutritionnels chez les nouveau-nés.
Les changements positifs doivent donc être interprétés en fonction de l'ensemble de ces facteurs, aussi lorsqu'ils sont négatifs pendant les périodes de crise.
Les changements séculaires doivent être interprétés en fonction de l'ensemble des facteurs socioéconomiques et nutritionnels. L'arrêt de changements observés actuellement dans certains pays européens doit aussi en tenir compte. Y a-t-il arrêt d'amélioration des conditions de vie ? Voire même une situation mésologique moins favorable ? Ou, les conditions ont-elles atteint une qualité telle que le potentiel génétique s'exprime de manière idéale ?
Des évaluations régulières du statut de croissance dans une population restent donc importantes puisqu'elles sont un outil sensible en santé publique.
Bibliographie
[1] alberman e. Are our babies becoming bigger ?.
J Roy Soc Med. 1991;
84:257
-260

[2] allen lh,
uauy r. Guidelines for the study of mechanisms involved in the prevention or reversal of linear growth retardation in developing countries.
Eur J Clin Nutr. 1994;
48:S212
-216

[3] beunen g,
malina r,
lefevre j,
claessens a,
renson r. Size, fatness and relative fat distribution of males contrasting maturity status during adolescence and as adults.
Int J Obesity. 1994;
18:670
-678

[4] bhandari n,
bahl r,
taneja s,
de onis m,
bhan mk. Les enfants indiens de familles aisées ont une croissance comparable à celle des enfants des pays développés.
B WHO. 2002;
80:189
-195

[5] bielicki t. Physical growth as a measure of the economic well-being of populations: the twentieth century. In: Methodology, Ecological, Genetic, and Nutritional Effects on Growth. Volume 3.
In: falkner f, tanner jm, editors.
.
New York et Londres:Plenum Press;
1986.
p. 283
-305

[6] bielicki t,
waliszko h. Stature, upward social mobility and the nature of statural differences between social classes.
Ann Hum Biology. 1992;
19:589
-593

[7] bielicki t,
hauspie rc. On the independence of adult stature from the timing of the adolescent growth spurt.
Am J Hum Biol. 1994;
6:245
-247

[8] bielicki t,
hulanicka b. Secular trends in stature and menarcheal age in Poland.
In: bodzsar e, susanne c, editors.
Secular growth changes in Europe..
Budapest:Budepast: Eòtvòs Lorand Univ;
1998.
p.
-

[9] bielicki t,
szklarska a. Secular trends in stature in Poland : national and social class-specific.
Ann Hum Biol. 1999;
26:251
-258

[10] bielicki t,
szczotka h,
charzewski j. The influence of three socio-economic factors on body height in Polish military conscripts.
Hum Biol. 1981;
153:543
-555

[11] bielicki t,
malina rm,
waliszko h. Monitoring the dynamic of social stratification: statural variation among Polish conscripts in 1976 and 1986.
Am J Hum Biol. 1992;
4:345
-352

[12] bielicki t,
szklarska a,
welon z,
malina rm. Variation in the body mass index among young adult Polish males between 1965 and 1995.
Int J Obesity. 2000;
24:658
-662

[13] bock rd,
thissen dm. Statistical problems of fitting individual growth curves.
In: johnston fe, roche af, susanne c, editors.
Human Physical Growth and Maturation..
New York et Londres:Plenum Press;
1980.
p. 265
-290

[14] bodzsar e,
susanne c. Secular growth changes in Europe: do we observe similar trends? Considerations for future research.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Budapest: Eòtvòs Lorand Univ;
1998.
p.
-

[15] bogin b. Patterns of Human Growth.
New York:Cambridge University Press;
1988.
267pp.

[16] bogin b,
mcvean rb. Growth status of non-agrarian, semiurban living Indians in Guatemala.
Hum Biol. 1984;
56:527
-538

[17] bundred p,
kitchiner d,
buchan i. Prevalence of overweight and obese children between 1989 and 1998: population based series of cross-sectional studies.
Br Med J. 2001;
322:326
-328

[18] butler ge,
mckie m,
ratcliffe sg. An analysis of the phases of mid-childhood growth by synchronisation of growth spurts.
In: tanner jm, editors.
Auxology 88, Perspectives in the Science of Growth and Development..
Londres:Smith-Gordon et Comp. Ltd.;
1989.
p. 77
-84

[19] byard pj,
guo s,
roche af. Family resemblance for Preece-Baines growth curve parameters in the Fels Longitudinal Growth Study.
Am J Hum Biol. 1993;
5:151
-157

[20] cameron n,
tanner jm,
whitehouse rh. A longitudinal analysis of the growth of limb segments in adolescence.
Ann Hum Biol. 1982;
9:211
-220

[21] cernerud l. Height and body mass index of seven-year-old Stockholm schoolchildren from 1940-1990.
Paediatr. 1993;
82:304
-305

[22] chinn s,
rona rj,
price ce. The secular trend in height of primary school children in England and Scotland 1972-79 and 1979-86.
Ann Hum Biol. 1989;
16:387
-396

[23] cole tj. The secular trend in human physical growth: a biological view.
Econ Hum Biol. 2003;
1:161
-168

[24] deheeger m,
rolland-cachera mf,
labadie m,
rossignol c. Étude longitudinale de la croissance et de l’alimentation d’enfants examinés de l’âge de 10 mois à 8 ans.
Cah Nutr Diet. 1994;
39:16
-23

[25] deheeger m,
rolland-cachera mf. Étude longitudinale de la croissance d’enfants parisiens suivis de l’âge de 10 mois à 18 ans.
Archives de pédiatrie. 2004;
11:1139
-1144

[26] demoulin e. The studies on secular trend in Spain: a review.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[27] demoulin f. Croissance fœtale humaine.
In: susanne c, rebato e, chiarelli b, editors.
Anthropologie biologique. Évolution et biologie humaine..
Bruxelles:De Boeck Université;
2003.
p. 487
-501

[28] eiben og. Secular trend in Hungary.
Humanbiologia Budapestinensis. 1989;
19:161
-168

[29] eveleth pb,
tanner jm. Worldwide variation in human growth. 2d edition.
Cambridge:Cambridge University Press;
1990.
397pp.

[30] eveleth pb,
salzano fm,
de lima pe. Child growth and adult physique in Brazilian Xingu Indians.
Am J Phys Anthropol. 1974;
41:95
-102

[31] facchini f,
gualdi russo e. Secular anthropometric changes in a sample in Italian adults.
J Hum Evol. 1982;
11:703
-710

[32] floris g,
sanna e. Some aspects of the secular trends in Italy.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[33] floud r,
wachter k,
gregory a. Height, health and history. Nutritional status in the United Kingdom, 1750-1980.
:Cambridge University Press;
1990.
378pp.

[34] foster jm,
chinn s,
rona rj. The relation of the height of primary school children to population density.
Int J Epid. 1983;
12:199
-204

[35] froment a. Croissance.
In: ferembach d, susanne c, chamla mc, editors.
L’homme, son évolution, sa diversité – Manuel d’anthropologie physique..
Paris:Doin Editeurs;
1986.
p. 359
-368

[36] garn sm. The secular trend in size and maturational timing and its implications for nutritional assessment.
J Nutr. 1987;
117:817
-823

[37] gasser t,
köhler w,
müller hg,
kneip a,
largo r. Velocity and acceleration of height growth using kernel estimation.
Ann Hum Biol. 1984;
11:397
-411

[38] gasser t,
sheehy a,
molinari l,
largo r. Growth of early and late maturers.
Ann Hum Biol. 2001;
28:328
-336

[39] golden mhn. Catch-up growth in height.
In: ulijaszek sj, johnston fe, preece ma, editors.
The Cambridge Encyclopedia of Human Growth and Development..
Cambridge:Cambridge University Press;
1998.
p. 346
-347

[40] gyenis g. Rapid change of head and face measurements in university students in Hungary.
Anth Anz. 1994;
52:149
-158

[41] gyenis g,
joubert k. Socioeconomic determinants of anthropmetric trends among Hungarian youth.
Econ Hum Biol. 2004;
2:321
-333

[42] hansen jdl,
freesemann c,
moodie ad,
evans de. What does nutritional growth retardation imply?.
Pediatr. 1971;
47:299
-313

[43] hauspie r. Adolescent Growth.
In: johnston fe, roche af, susanne c, editors.
Human Physical Growth and Maturation: Methodologies and Factors..
New York et Londres:Plenum Press;
1980.
p. 161
-175

[44] hauspie r. Aspects nutritionnels de l’anthropologie.
In: ferembach d, susanne c, chamla mc, editors.
L’homme, son évolution, sa diversité – Manuel d’anthropologie physique..
Paris:Doin Editeurs;
1986.
p. 347
-357

[45] hauspie rc. Mathematical models for the study of individual growth patterns.
Rev Epidemiol Sante. 1989;
37:461
-476

[46] hauspie rc. Curve fitting.
In: ulijaszek sj, johnston fe, preece ma, editors.
The Cambridge Encyclopedia of Human Growth and Development..
Cambridge:Cambridge University Press;
1998a.
p. 114
-115

[47] hauspie rc. The genetics of child growth.
In: ulijaszek sj, johnston fe, preece ma, editors.
The Cambridge Encyclopedia of Human Growth and Development..
Cambridge:Cambridge University Press;
1998b.
p. 124
-128

[48] hauspie r. Croissance et développement.
In: susanne c, rebato e, chiarelli b, editors.
Anthropologie biologique. Évolution et biologie humaine..
Bruxelles:De Boeck Université;
2003.
p. 475
-486

[49] hauspie r. Courbes de croissance de la population flamande (Belgique). http//www.vub.ac.be/groeicurven.
:;
2005.

[50] hauspie rc,
wachholder a. Clinical standards for growth velocity in height of Belgian boys and girls, aged 2 to 18 years.
Int J Anthropol. 1986;
1:327
-338

[51] hauspie rc,
chrzastek-spruch h. The analysis of individual and average growth curves: some methodological aspects.
In: duquet w, day jap, editors.
Kinanthropometry IV..
Londres:E & FN Spon;
1993.
p. 68
-83

[52] hauspie r,
chrzastek-spruch h. Growth models: possibilities and limitations.
In: johnston fe, zemel b, eveleth pb, editors.
Human Growth in Context..
Londres:Smith-Gordon;
1999.
p. 15
-24

[53] hauspie r,
vercauteren m. Secular trend.
In: nicoletti i, benso l, gilli g, editors.
Physiological and pathological auxology..
Italie:Centro Studi Auxologici;
2004.
p.
-

[54] hauspie r,
susanne c,
alexander f. Maturational delay and temporal growth retardation in asthmatic boys.
J Allergy Clin Immun. 1977;
59:200
-206

[55] hauspie r,
gyenis g,
alexander f,
simon g,
susanne c,
madach a. Heights and weights of Hungarian and Belgian asthmatic boys.
Hum Biol. 1979;
51:507
-521

[56] hauspie rc,
das sr,
preece ma,
tanner jm. A longitudinal study of the growth in height of boys and girls of West Bengal (India) aged six months to 20 years.
Ann Hum Biol. 1980;
7:429
-441

[57] hauspie rc,
das sr,
preece ma,
tanner jm. Degree of resemblance of the pattern of growth among sibs in families of West Bengal (India).
Ann Hum Biol. 1982;
9:171
-174

[58] hauspie r,
das sr,
preece ma,
tanner jm,
susanne c. Decomposition of sexual dimorphism in adult size of height, sitting height, shoulder width and hip width in a British and West Bengal sample.
In: ghesquire j, martin rd, newcombe f, editors.
Human Sexual Dimorphism..
Londres et Philadelphie:Taylor & Francis;
1985.
p. 207
-215

[59] hauspie rc,
lindgren g,
tanner jm,
chrzastek-spruch h. Modelling individual and average human growth data form childhood to adulthood.
In: magnusson d, bergman lr, törestad b, editors.
Problems and Methods in Longitudinal Research - Stability and Change..
Cambridge:Cambridge University Press;
1991.
p. 28
-46

[60] hauspie rc,
bergman p,
bielicki t,
susanne c. Genetic variance in the pattern of the growth curve for height: a longitudinal analysis of male twins.
Ann Hum Biol. 1994;
21:347
-362

[61] hauspie r,
vercauteren m,
susanne c. Secular changes in growth.
Horm Res. 1996;
45:817

[62] hauspie r,
vercauteren m,
susanne c. Secular changes in growth and maturation: an update.
Acta Paediatr Suppl. 1997;
423:20
-27

[63] hermanussen m. The analysis of short-term growth.
Hormone Research. 1998;
49:53
-64

[64] himes jh. Secular changes in body proportions and composition. In : Secular trends in human growth, maturation and development.
roche af (ed).
Mon Soc Res Child Dev. 1979;
44:28
-58

[65] hulanicka b,
waliszko a. Deceleration of age at menarche in Poland.
Ann Hum Biol. 1991;
18:507
-513

[66] hulse fs. Exogamie et heterosis.
Archives Suisses d’Anthropologie et de Génétique. 1957;
22:103
-125

[67] jaeger u. Secular trend in Germany.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[68] jolicoeur p,
pontier j,
abidi h. Asymptotic models for the longitudinal growth of human stature.
Am J Hum Biol. 1992;
4:461
-468

[69] kiess w,
gausche r,
keller a,
burmeister j,
willgerodt h,
keller e. Computer-guided, population-based screening system for growth disorders (CrescNet) and on-line generation of normative data for growth and development.
Horm Res. 2001;
56 suppl 1:59
-66

[70] komlos j. Stature and nutrition in the Habsburg monarchy: the standard of living and economic development.
Am Hist Rev. 1985;
90:1149
-1161

[71] koziel sk,
hauspie rc,
susanne c. Sex differences in height and sitting height in the Belgian population.
Int J Anthropol. 1995;
10:241
-247

[72] kuh dl,
power c,
rogers b. Secular trends in social class and sex differences in adult height.
Int J Epidemiol. 1991;
20:1001
-1009

[73] lampl m. Saltation and stasis in human growth: Evidence, methods and theory.
Nishimura:Smith-Gordon;
1999.
148pp.

[74] largo rh,
gasser th,
prader a,
stützle w,
huber pj. Analysis of the adolescent growth spurt using smoothing spline functions.
Ann Hum Biol. 1978;
5:421
-434

[75] li l,
manor o,
power c. Are inequalities in height narrowing? Comparing effects of social class on height in two generations.
Arch Dis Child. 2004;
89:1018
-1023

[76] liestol k,
rosenberg m. Height, weight and menarcheal age of schoolgirls in Oslo - an update.
Ann Hum Biol. 1995;
22:199
-205

[77] lindgren g. Height, weight and menarche in Swedish urban school children in relation to socio-economic and regional factors.
Ann Hum Biol. 1976;
3:501
-528

[78] lindgren g. Secular growth changes in Sweden.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[79] loesch dz,
hopper jl,
rogucka e,
ruggins r. Timing and genetic rapport between growth in skeletal maturity and height around puberty: similarities and differences betwwen girls and boys.
Am J Hum Genet. 1995;
56:753
-759

[80] malik sl,
hauspie r. Age at menarche among high altitude Bods of Ladakh (India).
Hum Biol. 1986;
58:541
-548

[81] malina rm,
bouchard c. Growth, maturation and physical activity.
In: , editors.
.
Champaign, IL:Human Kinetics;
1991.
p.
-

[82] marshall wa,
tanner jm. Puberty.
In: falkner f, tanner jm, editors.
Human Growth..
Vol. 2.
New York:Plenum Press;
1986.
p. 171
-209

[83] marubini e,
milani s. Approaches to the analysis of longitudinal data.
In: falkner f, tanner jm, editors.
Human Growth - A comprehensive treatise..
2
nd ed.
New York et Londres:Plenum Press;
1986.
p. 79
-94

[84] mccullough jm. Secular trend for stature in adult male Yucatec maya to 1968.
Am J Phys Anthropol. 1982;
58:221
-225

[85] meyer he,
selmer r. Income, educational level and body height.
Ann Hum Biol. 1999;
26:219
-227

[86] mueller wh. The genetics of size and shape in children and adults.
In: falkner f, tanner jm, editors.
Human Growth. Vol. 3 - Methodology, Ecological, Genetic, and Nutritional Effects on Growth..
New York et Londres:Plenum Press;
1986.
p. 145
-168

[87] ochoa zamora f,
pérez díaz c,
canadilla v. Variabilidad geográfica de los cambios seculares en escolares españoles.
Revista mexicana de estudios antropológicos. 1981;
27:221
-231

[88]oecd (organisation for economic cooperation and development). Food consumption’s statistics 1955-1974; 1973-1982.
Paris:Organisation for Cooperation and Development;
1985.

[89] otterloo ah van. Eten en eetlust in Nederland 1940 - 1990: een historisch - sociologische studie.
Amsterdam:Bert Bakker;
1990.
87pp.

[90] padez c,
johnston f. Secular trends in male adult height 1904-1996 in relation to place of residence and parent’s educational level in Portugal.
Ann Hum Biol. 1999;
26:387
-298

[91] pineau jc. La stature en France depuis un siècle: évolution générale et régionale.
B Mém Soc Anthr Paris. 1993;
5:257
-268

[92] powell gf,
brasel ja,
blizzard rm. Emotional deprivation and growth retardation simulating idiopathic hypopituitarism.
New Engl J Med. 1967;
276:1271
-1283

[93] preece ma,
baines mk. A new family of mathematical models describing the human growth curve.
Ann Hum Biol. 1978;
5:1
-24

[94] qin t,
shohoji t,
sumiya t. Relationship between adult stature and timing of the pubertal growth spurt.
Am J Hum Biol. 1996;
8:417
-426

[95] rebato e. The studies on secular trend in Spain: a review.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Budapest: Eòtvòs Lorand Univ;
1998.
p.
-

[96] rebato e. Obésité.
In: susanne c, rebato e, chiarelli b, editors.
Anthropologie biologique. Évolution et biologie humaine..
Bruxelles:De Boeck Université;
2003.
p. 609
-616

[97] rolland-cachera mf,
cole t,
sempé m,
tichet j,
rossignol c,
charraud a. Body mass index variations, centiles from birth to 87 years.
Eur J Clin Nutr. 1991;
45:13
-21

[98] rolland-cachera mf,
deheeger m,
maillot m,
bellisle f. Early adiposity rebound : causes and consequences for obesity inchildren and adults.
Int J Obesity. 2006;
30:S11
-S17

[99] rona rj. Secular trend of stature and body mass index (BMI) in Britain in the 20th century.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Budapest: Eòtvòs Lorand Univ;
1998.
p.
-

[100] rona rj,
chinn s. National study of health and growth: social and biological factors associated with height of children from ethnic groups living in England.
Ann Hum Biol. 1986;
5:453
-471

[101] rosenberg m. Birth weight in three Norwegian cities 1860-1984. Secular trends and influencing factors.
Ann Hum Biol. 1988;
15:275
-288

[102] salzer a. Die Akzeleration - ein gesellschaftlich und biologisch gesteuerter Prozess.
Anthropologiai Közlemények. 1975;
19:195
-200

[103] sekula w,
niedzialek z,
figurska k,
boruc t. Spozycie zywnosci w Polsce w latach 1950-1996 w przeliczeniu na energie i skladniki odzywcze; Prace Instytutu Zywnosci i Zywienia 84, Warszawa 1997 (Food consumption in Poland in 1950-1996. Energy and components).
:;
.

[104] sempé m,
pédron g,
roy-pernod m. Auxologie. Méthode et séquences.
Paris:Thérapix;
1979.
205pp.

[105] sethi hk,
sidhu ls,
singal p. Estimates of ageing and secular changes using total arm length.
Am J Hum Biol. 1995;
7:363
-368

[106] sharma jc. The genetic contribution to pubertal growth and development studies by longitudinal growth data on twins.
Ann Hum Biol. 1983;
10:163
-171

[107] shatrugna v,
rao kv. Secular trends in the heights of women from theurban poor community of Hyderabad.
Ann Hum Biol. 1987;
14:375
-377

[108] siegel s. Nonparametric statistics for the behavioral sciences.
Londres:McGraw-Hill, Ltd;
1956.

[109] skuse dh. Growth and psychosocial stress.
In: ulijaszek sj, johnston fe, preece ma, editors.
The Cambridge Encyclopedia of Human Growth and Development..
Cambridge:Cambridge University Press;
1998.
p. 341
-342

[110] smith am,
chinn s,
rona rj. Social factors and height gain of primary schoolchildren in England and Scotland.
Ann Hum Genet. 1980;
7:115
-124

[111] sorensen ti,
price ra. Secular trends in body mass index among Danish young men.
Int J Obesity. 1990;
14:411
-419

[112] stefanic m,
tomazo-ravnik t. Fifty two years of secular trend in Ljubljiana school children.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[113] stoev r,
yordanov j. Secular trend in Bulgaria.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[114] susanne c. Biological differences between migration and nonmigration.
In: boyce t, editors.
Migration and Mobility..
London:Taylor and Francis;
1984.
p. 174
-193

[115] susanne c. Living conditions and secular trend.
J Hum Evol. 1985;
14:357
-370

[116] susanne c. Croissance et nutrition.
B Mem Soc Anthropol Paris. 1993;
5:69
-83

[117] susanne c,
heyne d. Stature, poids et capacité vitale des étudiants et étudiantes de l’Université Libre de Bruxelles.
B Soc R Belg Anthrop Prehist. 1972;
83:101
-105

[118] susanne c,
lepage y. Fats, sugar, animal proteins: a new way of life.
J Hum Ecol. 1990;
1:49
-61

[119] susanne c,
lepage y. Evolution of nutritional factors and of growth in Belgium.
Ecol Food Nutr. 1992;
27:291
-306

[120] susanne c,
vercauteren m. Focus on physical and sexual maturation: the case of Belgium.
Acta Biol Szeged. 1997;
42:287
-297

[121] susanne c,
bodzsar e. Patterns of secular change of growth and development.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[122] susanne c,
hauspie r,
lepage y,
vercauteren m. Nutrition and growth.
World Rev Nutr Diet. 1987;
643:69
-170

[123] susanne c,
vercauteren m,
krasnicanova h,
jaeger u,
hauspie r,
bruzek j. Évolution séculaire des dimensions céphaliques.
B Mem Soc Anthropol Paris. 1988;
5:151
-162

[124] susanne c,
bodzsar e,
bielicki t,
hauspie r,
hulanicka b. Changements séculaires de la croissance et du développement en Europe. www.didac.ehu.es/antropo.
:;
2001.

[125] susanne c,
rebato e,
chiarelli b. Anthropologie biologique. Évolution et biologie humaine.
Bruxelles:De Boeck Université;
2003.
763pp.

[126] takahashi e. Secular trend in milk consumption and growth in Japan.
Hum Biol. 1984;
56:427
-437

[127] takaishi m. Growth standards for Japanese children - an overview with special reference to secular change in growth.
In: hauspie r, lindgren g, falkner f, editors.
Essays on Auxology Presented to James Mourilyan Tanner by Former Colleagues and Fellows..
Welwyn Garden City, Herts:Castlemead publications;
1995.
p. 302
-311

[128] tanner jm. A History of the Study of Human Growth.
Cambridge:Cambridge University Press;
1981.

[129] tanner jm. Growth as a target-seeking function - catch-up and catch-down growth in Man. Vol 1.
In: falkner f, tanner jm, editors.
Developmental Biology, Prenatal Growth.
New York et Londres:Plenum Press;
1986.
p. 167
--179

[130] tanner jm. Growth as a mirror of conditions in society.
In: lindgren g, editors.
Growth as a mirror of conditions in society..
Stockholm:Stockholm Instit, Education Press;
1990.
p. 9
-70

[131] tanner jm. Growth as a measure of nutritional and hygienic status of a population.
Horm Res. 1992;
38:106
-115

[132] tanner jm,
whitehouse rh,
marubini e,
resele lf. The adolescent growth spurt of boys and girls of the Harpenden study.
Ann Hum Biol. 1976;
3:109
-126

[133] tanner jm,
hayashi t,
preece ma,
cameron n. Increase in length of leg relative to the trunk in Japanese children and adults from 1975 to 1977: comparison with British and with Japanese Americans.
Ann Hum Biol. 1982;
9:411
-423

[134] tanner jm,
whitehouse rh,
takaishi m. Standards from birth to maturity for height, weight, height velocity, and weight velocity: British children, 1965. Part I.
Arch Dis Child. 1966a;
41:454
-471

[135] tanner jm,
whitehouse rh,
takaishi m. Standards from birth to maturity for height, weight, height velocity, and weight velocity: British children, 1965. Part II.
Arch Dis Child. 1966b;
41:613
-635

[136] tojo r,
iglesies c,
castro j,
alonso b,
segada r,
mores a. Secular trend in Galicicia 1900-1985. Evolución del crecimiento, maduración y desarrollo humano.
Bol Soc Cast Ast Leon de Pediatria. 1987;
28:289
-300

[137] ulizzi l,
terrenato l. A comparison between the secular trends of stature and of some socio-economic factors in Italy.
J Hum Evol. 1982;
11:715
-722

[138] van wieringen jc. Secular growth changes.
In: falkner f, tanner jm, editors.
Human Growth: a Comprehensive Treatise. Vol 3, 2
nd edition..
New York:Plenum Press;
1986.
p. 307
-331

[139] vercauteren m. Croissance, facteurs socio-familiaux et évolution séculaire.
B Mem Soc Anthropol Paris. 1993;
5:85
-92

[140] vercauteren m. Évolution séculaire au 20
e siècle.
In: susanne c, rebato e, chiarelli b, editors.
Anthropologie biologique. Évolution et biologie humaine..
Bruxelles:De Boeck Université;
2003.
p. 539
-548

[141] vercauteren m,
susanne c. Secular changes in growth and maturation: an update.
Acta Paediatr Suppl. 1997;
423:20
-27

[142] vercauteren m,
susanne c,
orban r. Évolution séculaire des dimensions céphaliques chez les enfants belges, entre 1960-1980.
B Mem Soc Anthropol Paris. 1983;
10:13
-24

[143] vercauteren m,
hauspie r,
susanne c. Biometry of Belgian boys and girls: changes since Quételet.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Budapest: Eòtvòs Lorand Univ;
1998.
p.
-

[144] vignerova j,
blaha p. The growth of the Czech child during the 40 years.
In: bodzsar e, susanne c, editors.
Secular growth change in Europe..
Budapest:Eòtvòs Lorand Univ;
1998.
p.
-

[145] wachholder a,
hauspie rc. Clinical standards for growth in height of Belgian boys and girls aged 2 to 18 years.
Int J Anthropol. 1986;
1:339
-348

[146] ward wp,
ward pc. Infant birth weight and nutrition in industrialising Montreal.
Am Hist Rev. 1984;
89:324
-345

[147] waterlow jc. Summary of causes and mechanisms of linear growth retardation.
Eur J Clin Nutr. 1994;
48 Suppl 1:S210
-

[148] weber g,
seidler h,
wilfing h,
hauser g. Secular change in height in Austria: an effect of population stratification?.
Ann Hum Biol. 1995;
22:277
-288

[149] widdowson em. Mental contentment and physical growth.
Lancet. 1951;
1:1316
-1318

[150] wolanski n. The problem of heterosis in man.
In: , editors.
Bevölkerungsbiologie. Bernhard et kandkler (eds)..
:Fischer Verlag;
1974.
p. 16
-30

[151] zacharias l,
rand wm. Adolescent growth in height and its relation to menarche in contemporary American girls.
Ann Hum Biol. 1983;
10:209
-222

[152] zellner k,
jaeger u,
kromeyer-hauschild k. Height, weight and BMI of schoolchildren in Jena, Germany - are the secular changes levelling off?.
Econ Hum Biol. 2004;
2:281
-294

→ Aller vers SYNTHESE
 ).
). ).
). illustre à partir d'un exemple les trois types principaux de courbes de croissance de dimensions corporelles : la courbe de croissance staturale typique des longueurs (longueur des jambes par exemple) et de certaines largeurs (comme la largeur des épaules et des hanches) ; la courbe de croissance pondérale et la courbe de croissance du périmètre céphalique. Dans ce dernier cas, à la naissance, l'enfant a déjà atteint une large part de la dimension finale ; cette courbe est similaire pour toutes les dimensions crâniennes ainsi que pour les dimensions du visage.
illustre à partir d'un exemple les trois types principaux de courbes de croissance de dimensions corporelles : la courbe de croissance staturale typique des longueurs (longueur des jambes par exemple) et de certaines largeurs (comme la largeur des épaules et des hanches) ; la courbe de croissance pondérale et la courbe de croissance du périmètre céphalique. Dans ce dernier cas, à la naissance, l'enfant a déjà atteint une large part de la dimension finale ; cette courbe est similaire pour toutes les dimensions crâniennes ainsi que pour les dimensions du visage. montre que la vitesse de croissance staturale est caractérisée par une période d'accroissement rapide, mais néanmoins décélérante, durant les deux premières années de la croissance postnatale ; elle est suivie d'une période de vitesse de croissance staturale plus ou moins constante, parfois interrompue par un ou plusieurs petits pics de croissance pré-pubertaires (Butler et coll., 1989
montre que la vitesse de croissance staturale est caractérisée par une période d'accroissement rapide, mais néanmoins décélérante, durant les deux premières années de la croissance postnatale ; elle est suivie d'une période de vitesse de croissance staturale plus ou moins constante, parfois interrompue par un ou plusieurs petits pics de croissance pré-pubertaires (Butler et coll., 1989 ; Hauspie et Chrzastek-Spruch, 1993
; Hauspie et Chrzastek-Spruch, 1993 ). Cette période est suivie par la période pubertaire ou l'adolescence, caractérisée par la présence d'un pic de croissance pubertaire.
). Cette période est suivie par la période pubertaire ou l'adolescence, caractérisée par la présence d'un pic de croissance pubertaire. ) (Tanner et coll., 1966a
) (Tanner et coll., 1966a ), après lequel la vitesse augmente graduellement. La courbe de vitesse de croissance du périmètre crânien est caractérisée par une vitesse rapide mais fortement décélérante durant la première année postnatale (figure 1.2 C
), après lequel la vitesse augmente graduellement. La courbe de vitesse de croissance du périmètre crânien est caractérisée par une vitesse rapide mais fortement décélérante durant la première année postnatale (figure 1.2 C ). Vers l'âge de 2 ans, la vitesse de croissance chute en dessous de 1 cm/an, et cela pour le reste de la période de croissance. Les dimensions de la tête et du visage ne montrent pas de pic de croissance pubertaire.
). Vers l'âge de 2 ans, la vitesse de croissance chute en dessous de 1 cm/an, et cela pour le reste de la période de croissance. Les dimensions de la tête et du visage ne montrent pas de pic de croissance pubertaire. illustre cette vitesse calculée comme la première dérivée d'un exemple de courbe lissée de croissance de la taille par rapport à l'âge. La figure 1.3
illustre cette vitesse calculée comme la première dérivée d'un exemple de courbe lissée de croissance de la taille par rapport à l'âge. La figure 1.3 illustre donc le fait que la taille, caractérisée par une période d'accroissement rapide à la naissance, décélère durant les deux premières années (la petite enfance) ; cette période est suivie par une période de vitesse plus stable (légèrement décélérante ou constante) pendant l'enfance, caractérisée parfois par un ou plusieurs petits pics de croissance pré-pubertaires. Cette période de l'enfance est de durée variable selon le sexe et la vitesse de maturation de l'enfant. Cette période est suivie par la période pubertaire ou l'adolescence, caractérisée par une accélération de la croissance staturale et un pic de croissance pubertaire. Après ce pic, la vitesse de croissance staturale diminue rapidement et la croissance se termine à l'âge adulte, atteint actuellement vers 16-17 ans chez les filles et 18-19 ans chez les garçons. Naturellement, les facteurs de variation sont multiples, entre populations, entre individus et entre les deux sexes ; cette variation concerne aussi bien le timing de développement que la taille elle-même à chaque âge.
illustre donc le fait que la taille, caractérisée par une période d'accroissement rapide à la naissance, décélère durant les deux premières années (la petite enfance) ; cette période est suivie par une période de vitesse plus stable (légèrement décélérante ou constante) pendant l'enfance, caractérisée parfois par un ou plusieurs petits pics de croissance pré-pubertaires. Cette période de l'enfance est de durée variable selon le sexe et la vitesse de maturation de l'enfant. Cette période est suivie par la période pubertaire ou l'adolescence, caractérisée par une accélération de la croissance staturale et un pic de croissance pubertaire. Après ce pic, la vitesse de croissance staturale diminue rapidement et la croissance se termine à l'âge adulte, atteint actuellement vers 16-17 ans chez les filles et 18-19 ans chez les garçons. Naturellement, les facteurs de variation sont multiples, entre populations, entre individus et entre les deux sexes ; cette variation concerne aussi bien le timing de développement que la taille elle-même à chaque âge. ; Lampl, 1999
; Lampl, 1999 ).
). ; Bogin, 1988
; Bogin, 1988 ; Hauspie, 1989
; Hauspie, 1989 et 1998a
et 1998a ). Les avantages et désavantages des modèles les plus utilisés ont été envisagés par Hauspie et coll. (1991
). Les avantages et désavantages des modèles les plus utilisés ont été envisagés par Hauspie et coll. (1991 ) et par Hauspie et Chrzastek-Spruch (1999
) et par Hauspie et Chrzastek-Spruch (1999 ). Le modèle I de Preece et Baines (PB1) est très couramment utilisé pour décrire la croissance de la taille et des dimensions post-crâniennes entre l'âge de 2-5 ans et l'âge adulte (Preece et Baines, 1978
). Le modèle I de Preece et Baines (PB1) est très couramment utilisé pour décrire la croissance de la taille et des dimensions post-crâniennes entre l'âge de 2-5 ans et l'âge adulte (Preece et Baines, 1978 ) ; la fonction logistique triple (Bock et Thissen, 1980
) ; la fonction logistique triple (Bock et Thissen, 1980 ) et le modèle JPA-2 (Jolicoeur et coll., 1992
) et le modèle JPA-2 (Jolicoeur et coll., 1992 ) le sont lorsque la courbe est étudiée à partir de la naissance.
) le sont lorsque la courbe est étudiée à partir de la naissance.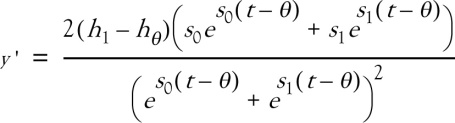
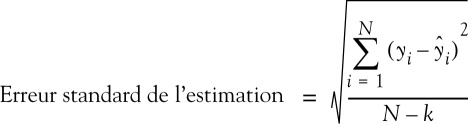
 illustre l'ajustement du modèle PB1 et les accroissements annuels ainsi que la courbe de vitesse de croissance instantanée. Les valeurs des paramètres du modèle PB1 figurent dans le tableau 1.I
illustre l'ajustement du modèle PB1 et les accroissements annuels ainsi que la courbe de vitesse de croissance instantanée. Les valeurs des paramètres du modèle PB1 figurent dans le tableau 1.I . L'erreur standard de l'estimation, qui correspond à la racine carrée de la variance résiduelle, est souvent utilisée comme une mesure de la qualité de l'ajustement.
. L'erreur standard de l'estimation, qui correspond à la racine carrée de la variance résiduelle, est souvent utilisée comme une mesure de la qualité de l'ajustement.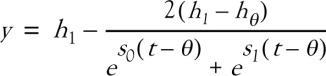 avec yi la taille à l'âge xi,
avec yi la taille à l'âge xi,  la valeur de la courbe ajustée à l'âge xi, N le nombre de mesures de la taille, et k le nombre de paramètres dans le modèle (5 dans le cas du modèle PB1).
la valeur de la courbe ajustée à l'âge xi, N le nombre de mesures de la taille, et k le nombre de paramètres dans le modèle (5 dans le cas du modèle PB1). ) » (Hauspie, 2003
) » (Hauspie, 2003 ).
). ; Gasser et coll., 1984
; Gasser et coll., 1984 ).
). illustre un exemple théorique soulignant les effets principaux de la variation du rythme de croissance sur la forme de la courbe de croissance. Le graphique montre la taille atteinte, ainsi que la vitesse de croissance de la taille, pour des enfants à maturation avancée, moyenne et tardive, ayant la même taille à la naissance et à l'âge adulte. Ces trois sujets théoriques ont le même potentiel pour atteindre une certaine taille finale, mais ils diffèrent considérablement en ce qui concerne le temps nécessaire pour arriver à cette maturation complète. Par conséquent, on observe des différences considérables de la taille et de la forme de la courbe de croissance entre ces trois degrés de rythme de croissance tout au long de la période de l'enfance et surtout à l'adolescence. L'effet de différences de rythme de croissance sur la taille atteinte est d'autant plus grand que l'enfant devient plus âgé et que la pente de la courbe de croissance est plus aiguë, ce qui explique que l'effet de différences de rythme de croissance sur la taille atteinte est plus prononcé lors du pic de croissance pubertaire (Hauspie, 2003
illustre un exemple théorique soulignant les effets principaux de la variation du rythme de croissance sur la forme de la courbe de croissance. Le graphique montre la taille atteinte, ainsi que la vitesse de croissance de la taille, pour des enfants à maturation avancée, moyenne et tardive, ayant la même taille à la naissance et à l'âge adulte. Ces trois sujets théoriques ont le même potentiel pour atteindre une certaine taille finale, mais ils diffèrent considérablement en ce qui concerne le temps nécessaire pour arriver à cette maturation complète. Par conséquent, on observe des différences considérables de la taille et de la forme de la courbe de croissance entre ces trois degrés de rythme de croissance tout au long de la période de l'enfance et surtout à l'adolescence. L'effet de différences de rythme de croissance sur la taille atteinte est d'autant plus grand que l'enfant devient plus âgé et que la pente de la courbe de croissance est plus aiguë, ce qui explique que l'effet de différences de rythme de croissance sur la taille atteinte est plus prononcé lors du pic de croissance pubertaire (Hauspie, 2003 ).
).
 ; Cameron et coll., 1982
; Cameron et coll., 1982 ; Zacharias et Rand, 1983
; Zacharias et Rand, 1983 ; Marshall et Tanner 1986
; Marshall et Tanner 1986 ; Malina et Bouchard, 1991
; Malina et Bouchard, 1991 ; Beunen et coll., 1994
; Beunen et coll., 1994 ; Bielicki et Hauspie, 1994
; Bielicki et Hauspie, 1994 ; Qin et coll., 1996
; Qin et coll., 1996 ; Gasser et coll., 2001
; Gasser et coll., 2001 ). Ainsi par exemple, les enfants à maturation avancée ont une période de croissance moins longue mais une vitesse de croissance plus élevée pendant l'enfance et, surtout au moment du pic de croissance pubertaire. Au contraire, des enfants à maturation tardive auront une période de croissance plus longue mais le pic de croissance pubertaire sera moins élevé. Il existe donc une corrélation négative entre la vitesse maximale lors du pic de croissance pubertaire et l'âge auquel cette vitesse maximale est atteinte : ceci est le cas pour la taille et bien d'autres caractères (Tanner et coll., 1976
). Ainsi par exemple, les enfants à maturation avancée ont une période de croissance moins longue mais une vitesse de croissance plus élevée pendant l'enfance et, surtout au moment du pic de croissance pubertaire. Au contraire, des enfants à maturation tardive auront une période de croissance plus longue mais le pic de croissance pubertaire sera moins élevé. Il existe donc une corrélation négative entre la vitesse maximale lors du pic de croissance pubertaire et l'âge auquel cette vitesse maximale est atteinte : ceci est le cas pour la taille et bien d'autres caractères (Tanner et coll., 1976 ; Largo et coll., 1978
; Largo et coll., 1978 ; Hauspie, 1980
; Hauspie, 1980 ).
). ) et pour l'IMC (figure 1.6
) et pour l'IMC (figure 1.6 ) (Hauspie, 2005
) (Hauspie, 2005 ).
).

 illustre ces courbes d'accroissement des moyennes pour la même population que la figure 1.5
illustre ces courbes d'accroissement des moyennes pour la même population que la figure 1.5 . L'allure d'une courbe moyenne d'une étude transversale diffère nettement de celle de courbes individuelles longitudinales. Pendant la puberté, la courbe de croissance d'un enfant ne suit pas une des lignes percentilées des normes de croissance transversale et ces lignes percentilées ne permettent pas d'évaluer la normalité de l'évolution de la croissance dans le temps. Cependant, on peut tenir compte dans des courbes de référence de ces différences de rythme de croissance (Tanner et coll., 1966a
. L'allure d'une courbe moyenne d'une étude transversale diffère nettement de celle de courbes individuelles longitudinales. Pendant la puberté, la courbe de croissance d'un enfant ne suit pas une des lignes percentilées des normes de croissance transversale et ces lignes percentilées ne permettent pas d'évaluer la normalité de l'évolution de la croissance dans le temps. Cependant, on peut tenir compte dans des courbes de référence de ces différences de rythme de croissance (Tanner et coll., 1966a et b
et b ). Wachholder et Hauspie (1986
). Wachholder et Hauspie (1986 ) et Hauspie et Wachholder (1986
) et Hauspie et Wachholder (1986 ) ont par exemple utilisé des courbes de « constantes-moyennes » pour estimer l'allure typiquement moyenne (Hauspie, 1989
) ont par exemple utilisé des courbes de « constantes-moyennes » pour estimer l'allure typiquement moyenne (Hauspie, 1989 ), alors que les courbes de référence pour les enfants à maturation avancée ou tardive étaient obtenues par une analyse de régression des paramètres du modèle Preece et Baines (PB1) sur l'âge à la vitesse maximale lors de la puberté (Wachholder et Hauspie, 1986
), alors que les courbes de référence pour les enfants à maturation avancée ou tardive étaient obtenues par une analyse de régression des paramètres du modèle Preece et Baines (PB1) sur l'âge à la vitesse maximale lors de la puberté (Wachholder et Hauspie, 1986 ; Hauspie et Wachholder, 1986
; Hauspie et Wachholder, 1986 ). La figure 1.7
). La figure 1.7 illustre de telles courbes pour la population de Sarsuna-Barisha (Hauspie et coll., 1980
illustre de telles courbes pour la population de Sarsuna-Barisha (Hauspie et coll., 1980 ).
). ; Hauspie et coll., 1985
; Hauspie et coll., 1985 ; Hauspie, 1986
; Hauspie, 1986 ; Koziel et coll., 1995
; Koziel et coll., 1995 ). En effet, en comparant les courbes de constantes moyennes des garçons et des filles, obtenues après ajustement d'un modèle mathématique aux sujets individuels de l'échantillon, on peut décomposer le dimorphisme sexuel de la taille adulte en trois parties :
). En effet, en comparant les courbes de constantes moyennes des garçons et des filles, obtenues après ajustement d'un modèle mathématique aux sujets individuels de l'échantillon, on peut décomposer le dimorphisme sexuel de la taille adulte en trois parties : montre les courbes de constantes moyennes pour la population belge. Le début de la poussée de croissance pubertaire est indiqué par les points noirs, alors que l'accroissement pubertaire est la croissance acquise depuis le début de la poussée de croissance pubertaire jusqu'à la taille finale.
montre les courbes de constantes moyennes pour la population belge. Le début de la poussée de croissance pubertaire est indiqué par les points noirs, alors que l'accroissement pubertaire est la croissance acquise depuis le début de la poussée de croissance pubertaire jusqu'à la taille finale. montre les résultats d'une telle analyse pour la population belge en ce qui concerne la taille et la taille assis (Hauspie, 2003
montre les résultats d'une telle analyse pour la population belge en ce qui concerne la taille et la taille assis (Hauspie, 2003 ).
). indique que le dimorphisme sexuel de la taille adulte était de 13,5 cm dans la population belge, décomposé en 0,4 cm de différences pré-pubertaires de taille, 4,9 cm de pic pubertaire plus élevé chez les garçons et surtout 8,2 cm dû au retard dans le timing de la poussée de croissance pubertaire chez les garçons.
indique que le dimorphisme sexuel de la taille adulte était de 13,5 cm dans la population belge, décomposé en 0,4 cm de différences pré-pubertaires de taille, 4,9 cm de pic pubertaire plus élevé chez les garçons et surtout 8,2 cm dû au retard dans le timing de la poussée de croissance pubertaire chez les garçons. ) ont suggéré que le début plus précoce de la puberté chez les filles est associé à une sécrétion plus précoce d'œstrogènes, qui accélère plus la maturation squelettique que la croissance en taille, et réduit donc le gain en taille pendant la période pubertaire. Chez les garçons, la testostérone stimule la croissance en taille et accélère la maturation squelettique.
) ont suggéré que le début plus précoce de la puberté chez les filles est associé à une sécrétion plus précoce d'œstrogènes, qui accélère plus la maturation squelettique que la croissance en taille, et réduit donc le gain en taille pendant la période pubertaire. Chez les garçons, la testostérone stimule la croissance en taille et accélère la maturation squelettique. ).
). ; Sharma, 1983
; Sharma, 1983 ; Mueller, 1986
; Mueller, 1986 ; Byard et coll., 1993
; Byard et coll., 1993 ; Hauspie, 1998b
; Hauspie, 1998b ). Ainsi, une étude de Hauspie et coll. (1994
). Ainsi, une étude de Hauspie et coll. (1994 ) sur des jumeaux monozygotes et dizygotes montre une composante génétique importante, en particulier dans la variation de l'âge au pic de croissance pubertaire. L'influence génétique peut être évaluée par un cœfficient d'héritabilité, défini comme la proportion de la variation due aux facteurs génétiques par rapport à la variation totale. Cependant, dans l'examen des relations familiales, à la composante génétique s'ajoute la transmissibilité culturelle et mésologique.
) sur des jumeaux monozygotes et dizygotes montre une composante génétique importante, en particulier dans la variation de l'âge au pic de croissance pubertaire. L'influence génétique peut être évaluée par un cœfficient d'héritabilité, défini comme la proportion de la variation due aux facteurs génétiques par rapport à la variation totale. Cependant, dans l'examen des relations familiales, à la composante génétique s'ajoute la transmissibilité culturelle et mésologique. ; Golden, 1998
; Golden, 1998 ). Mais si la période de stress dure trop longtemps, la croissance répondra à un modèle de maturation tardive. Les exemples sont nombreux, que ce soit pour des raisons de malnutrition chronique mais légère (Hansen et coll., 1971
). Mais si la période de stress dure trop longtemps, la croissance répondra à un modèle de maturation tardive. Les exemples sont nombreux, que ce soit pour des raisons de malnutrition chronique mais légère (Hansen et coll., 1971 ), des raisons médicales de maladies chroniques comme l'asthme (Hauspie et coll., 1977
), des raisons médicales de maladies chroniques comme l'asthme (Hauspie et coll., 1977 et 1979
et 1979 ), des raisons de stress psychosocial (Widdowson, 1951
), des raisons de stress psychosocial (Widdowson, 1951 ; Powell et coll., 1967
; Powell et coll., 1967 ; Skuse, 1998
; Skuse, 1998 ), des raisons de milieu familial socialement défavorisé (Bielicki, 1986
), des raisons de milieu familial socialement défavorisé (Bielicki, 1986 ), ou encore chez des enfants vivant à haute altitude (Malik et Hauspie, 1986
), ou encore chez des enfants vivant à haute altitude (Malik et Hauspie, 1986 ). « Tous ces enfants sont légèrement en retard pour atteindre leur poussée de croissance pubertaire, la maturation sexuelle et la taille finale. Au contraire, la taille finale n'est, en moyenne, pas réduite (c'est-à-dire conforme à la moyenne de la population), sauf si les conditions contraignantes sont trop sévères (Froment, 1986
). « Tous ces enfants sont légèrement en retard pour atteindre leur poussée de croissance pubertaire, la maturation sexuelle et la taille finale. Au contraire, la taille finale n'est, en moyenne, pas réduite (c'est-à-dire conforme à la moyenne de la population), sauf si les conditions contraignantes sont trop sévères (Froment, 1986 ; Tanner, 1986
; Tanner, 1986 ) » (Hauspie, 2003
) » (Hauspie, 2003 ).
). ; Susanne et coll., 2001
; Susanne et coll., 2001 ) (figures 1.9
) (figures 1.9 et 1.10
et 1.10 ).
). ) ont montré que l'évolution séculaire de la taille continue à être observée dans la plupart des régions européennes (figure 1.11
) ont montré que l'évolution séculaire de la taille continue à être observée dans la plupart des régions européennes (figure 1.11 ) : elle est plus faible dans les pays nordiques comme la Suède et la Norvège (de l'ordre de 0,3 cm par décennie) et plus élevée dans les pays de l'est et du sud (2,5 cm par décennie en Pologne, Espagne, Bulgarie, Italie et 3,5 cm par décennie en Grèce). En Europe occidentale, elle reste de l'ordre de 1 cm par décennie (Hauspie et coll., 1997
) : elle est plus faible dans les pays nordiques comme la Suède et la Norvège (de l'ordre de 0,3 cm par décennie) et plus élevée dans les pays de l'est et du sud (2,5 cm par décennie en Pologne, Espagne, Bulgarie, Italie et 3,5 cm par décennie en Grèce). En Europe occidentale, elle reste de l'ordre de 1 cm par décennie (Hauspie et coll., 1997 ).
).

 ).
). ; Garn, 1987
; Garn, 1987 ; Rosenberg, 1988
; Rosenberg, 1988 ). Ils prennent place cependant dès les premières années de vie, mais l'évolution séculaire de la taille est souvent plus élevée durant la période pubertaire : Eveleth et Tanner (1990
). Ils prennent place cependant dès les premières années de vie, mais l'évolution séculaire de la taille est souvent plus élevée durant la période pubertaire : Eveleth et Tanner (1990 ) évaluent, pour la période 1880-1980, les changements à 1,5 cm par décennie pendant l'enfance, 2,5 cm par décennie pendant la puberté et à 1 cm par décennie à l'âge adulte. En fait, cette observation est liée au développement pubertaire progressivement plus précoce. Ainsi, la figure 1.13
) évaluent, pour la période 1880-1980, les changements à 1,5 cm par décennie pendant l'enfance, 2,5 cm par décennie pendant la puberté et à 1 cm par décennie à l'âge adulte. En fait, cette observation est liée au développement pubertaire progressivement plus précoce. Ainsi, la figure 1.13 relative à l'évolution séculaire en Belgique montrant les différences entre les données de 1980 avec celles de 1960, 1930 et 1830, met en évidence des différences plus élevées pendant l'âge de la puberté mais uniquement par rapport à 1930 et 1830 où l'augmentation est due à l'accroissement de taille mais aussi à une accélération de tempo. Au contraire, par rapport à 1960, les différences observées sont du même ordre de grandeur : dans ce cas, les différences ne sont plus dues qu'à l'accroissement de taille.
relative à l'évolution séculaire en Belgique montrant les différences entre les données de 1980 avec celles de 1960, 1930 et 1830, met en évidence des différences plus élevées pendant l'âge de la puberté mais uniquement par rapport à 1930 et 1830 où l'augmentation est due à l'accroissement de taille mais aussi à une accélération de tempo. Au contraire, par rapport à 1960, les différences observées sont du même ordre de grandeur : dans ce cas, les différences ne sont plus dues qu'à l'accroissement de taille.
 ).
). ; Vercauteren, 2003
; Vercauteren, 2003 ).
). ; Hauspie et Vercauteren, 2004
; Hauspie et Vercauteren, 2004 ).
). ; Tanner et coll., 1982
; Tanner et coll., 1982 ; Vercauteren et coll., 1983
; Vercauteren et coll., 1983 ; Tanner, 1990
; Tanner, 1990 ; Susanne, 1993
; Susanne, 1993 ; Takaishi, 1995
; Takaishi, 1995 ).
). ; Kuh et coll., 1991
; Kuh et coll., 1991 ) mentionnent une plus grande plasticité des garçons, c'est-à-dire que les garçons seraient plus plastiques aux changements mésologiques, seraient plus affectés par de mauvaises conditions et croîtraient plus rapidement lorsque les conditions sont favorables.
) mentionnent une plus grande plasticité des garçons, c'est-à-dire que les garçons seraient plus plastiques aux changements mésologiques, seraient plus affectés par de mauvaises conditions et croîtraient plus rapidement lorsque les conditions sont favorables. ; Susanne et coll., 2001
; Susanne et coll., 2001 ) mais indique souvent un type de silhouette plus longiligne, comme en Belgique (Susanne, 1993
) mais indique souvent un type de silhouette plus longiligne, comme en Belgique (Susanne, 1993 ; Vercauteren et coll., 1998
; Vercauteren et coll., 1998 ), Suède (Lindgren, 1998
), Suède (Lindgren, 1998 ) et Allemagne (Jaeger, 1998
) et Allemagne (Jaeger, 1998 ) (figure 1.14
) (figure 1.14 ), bien que des différences régionales et socioéconomiques existent.
), bien que des différences régionales et socioéconomiques existent.
 ; Susanne et coll., 1988
; Susanne et coll., 1988 ; Vercauteren et coll., 1998
; Vercauteren et coll., 1998 ), la Bulgarie (Stoev et Yordanov, 1998
), la Bulgarie (Stoev et Yordanov, 1998 ), la France (Demoulin, 1998
), la France (Demoulin, 1998 ), l'Allemagne (Jaeger, 1998
), l'Allemagne (Jaeger, 1998 ), la Hongrie (Gyenis, 1994
), la Hongrie (Gyenis, 1994 ) et la République tchèque (Vignerova et Blaha, 1998
) et la République tchèque (Vignerova et Blaha, 1998 ) (figure 1.15
) (figure 1.15 ).
).
 ; Susanne et coll., 2001
; Susanne et coll., 2001 ).
). , pour les filles de plus de 15 ans), en Slovénie (Stefancic et Tomazo-Ravnik, 1998, à partir de 13 ans), en Belgique (Susanne, 1993
, pour les filles de plus de 15 ans), en Slovénie (Stefancic et Tomazo-Ravnik, 1998, à partir de 13 ans), en Belgique (Susanne, 1993 ; Hauspie et coll., 1997
; Hauspie et coll., 1997 , à partir de 13 ans) et à Jena (Jaeger, 1998
, à partir de 13 ans) et à Jena (Jaeger, 1998 , aux tailles supérieures à 150 cm).
, aux tailles supérieures à 150 cm). ) et Lindgren (1998
) et Lindgren (1998 ) pour la Suède, Liestol et Rosenberg (1995
) pour la Suède, Liestol et Rosenberg (1995 ) pour la Norvège, Rona (1998
) pour la Norvège, Rona (1998 ) pour l'Angleterre, Sorensen et Price (1990
) pour l'Angleterre, Sorensen et Price (1990 ) pour le Danemark, Kiess et coll. (2001
) pour le Danemark, Kiess et coll. (2001 ) pour l'Allemagne (ces auteurs observent une augmentation du 97e percentile alors que le 3e percentile reste constant) ainsi que Zellner et coll. (2004
) pour l'Allemagne (ces auteurs observent une augmentation du 97e percentile alors que le 3e percentile reste constant) ainsi que Zellner et coll. (2004 ) pour l'Allemagne (figure 1.16
) pour l'Allemagne (figure 1.16 ).
). ). L'obésité est actuellement observée à des âges de plus en plus jeunes (Bundred et coll., 2001
). L'obésité est actuellement observée à des âges de plus en plus jeunes (Bundred et coll., 2001 ; Zellner et coll., 2004
; Zellner et coll., 2004 ).
). ; Rosenberg, 1988
; Rosenberg, 1988 ). Au XXe siècle, il est resté stable mais il existe des signes récents aux États-Unis d'une augmentation, liée probablement à l'obésité maternelle (Alberman, 1991
). Au XXe siècle, il est resté stable mais il existe des signes récents aux États-Unis d'une augmentation, liée probablement à l'obésité maternelle (Alberman, 1991 ) et à une augmentation de diabète gestationnel.
) et à une augmentation de diabète gestationnel. ), les Khatris en Inde (Sethi et coll., 1995
), les Khatris en Inde (Sethi et coll., 1995 ), les Indiens Xingu au Brésil (Eveleth et coll., 1974
), les Indiens Xingu au Brésil (Eveleth et coll., 1974 ), à Hyderabab en Inde (Shatrugna et Rao, 1987
), à Hyderabab en Inde (Shatrugna et Rao, 1987 ).
). ) (figure 1.17
) (figure 1.17 ) ; c'est aussi le cas en Europe au début du XIXe siècle pour la taille sous l'effet de la révolution industrielle, et de faibles récoltes (Komlos, 1985
) ; c'est aussi le cas en Europe au début du XIXe siècle pour la taille sous l'effet de la révolution industrielle, et de faibles récoltes (Komlos, 1985 ; Floud et coll., 1990
; Floud et coll., 1990 ), et également durant les deux guerres mondiales (Eiben, 1989
), et également durant les deux guerres mondiales (Eiben, 1989 ).
). ). Cette observation d'évolution séculaire est essentiellement basée sur des tailles masculines adultes, à savoir des conscrits de 18-20 ans qui cependant n'ont pas atteint nécessairement leur taille définitive. L'évolution séculaire y est de 0,7 cm par décennie entre 1900 et 1960 et de 1 à 2 cm par décennie entre 1960 et 1990.
). Cette observation d'évolution séculaire est essentiellement basée sur des tailles masculines adultes, à savoir des conscrits de 18-20 ans qui cependant n'ont pas atteint nécessairement leur taille définitive. L'évolution séculaire y est de 0,7 cm par décennie entre 1900 et 1960 et de 1 à 2 cm par décennie entre 1960 et 1990. ) a montré que les enfants actuels sont plus grands et ont un poids plus élevé. Elle montre également un avancement du rebond d'adiposité et une vitesse augmentée de la croissance au début de la vie (Deheeger et Rolland-Cachera, 2004
) a montré que les enfants actuels sont plus grands et ont un poids plus élevé. Elle montre également un avancement du rebond d'adiposité et une vitesse augmentée de la croissance au début de la vie (Deheeger et Rolland-Cachera, 2004 ; Rolland-Cachera et coll., 2006
; Rolland-Cachera et coll., 2006 ).
). ). À titre d'exemple, la figure 1.18
). À titre d'exemple, la figure 1.18 illustre la situation en 1989, où un gradient nord-est vers sud-ouest est observé, des tailles les plus élevées au nord et nord-est vers les moins élevées au sud et sud-ouest.
illustre la situation en 1989, où un gradient nord-est vers sud-ouest est observé, des tailles les plus élevées au nord et nord-est vers les moins élevées au sud et sud-ouest.  ; Rolland-Cachera et coll., 1991
; Rolland-Cachera et coll., 1991 ).
). ) et Rolland-Cachera et coll. (1991
) et Rolland-Cachera et coll. (1991 ) (voir en annexe 2).
) (voir en annexe 2). ). Tanner (1992
). Tanner (1992 ) a même proposé le terme d'épidémiologie auxologique et sa phrase « la croissance est le miroir des conditions de la société » est devenue célèbre.
) a même proposé le terme d'épidémiologie auxologique et sa phrase « la croissance est le miroir des conditions de la société » est devenue célèbre. ). La génétique jouerait un rôle peu important dans le processus d'évolution séculaire puisque des enfants de milieu favorisé dans le tiers-monde croissent de manière assez semblable à ceux de populations de pays développés (Hauspie et coll., 1980
). La génétique jouerait un rôle peu important dans le processus d'évolution séculaire puisque des enfants de milieu favorisé dans le tiers-monde croissent de manière assez semblable à ceux de populations de pays développés (Hauspie et coll., 1980 ; Bhandari et coll., 2002
; Bhandari et coll., 2002 ). Les différences observées entre populations différentes mais de niveau socioéconomique élevé sont relativement moins élevées que celles observées entre les niveaux socioéconomiques différents au sein de populations identiques.
). Les différences observées entre populations différentes mais de niveau socioéconomique élevé sont relativement moins élevées que celles observées entre les niveaux socioéconomiques différents au sein de populations identiques. ). Quételet avait fait des observations identiques à Bruxelles ainsi que l'effet délétère du travail infantile sur la taille finale.
). Quételet avait fait des observations identiques à Bruxelles ainsi que l'effet délétère du travail infantile sur la taille finale. ; Salzer, 1975
; Salzer, 1975 ; Lindgren, 1976
; Lindgren, 1976 ; Smith et coll., 1980
; Smith et coll., 1980 ; Rona et Chinn, 1986
; Rona et Chinn, 1986 ; Vercauteren, 1993
; Vercauteren, 1993 ; Weber et coll., 1995
; Weber et coll., 1995 ; Hauspie et coll., 1996
; Hauspie et coll., 1996 et 1997
et 1997 ; Vercauteren et coll., 1998
; Vercauteren et coll., 1998 ). Ainsi, en Pologne, l'amplitude des inégalités sociales en terme de moyenne de taille a décliné par une évolution séculaire plus élevée des groupes sociaux les moins favorisés (Bielicki et coll., 1992
). Ainsi, en Pologne, l'amplitude des inégalités sociales en terme de moyenne de taille a décliné par une évolution séculaire plus élevée des groupes sociaux les moins favorisés (Bielicki et coll., 1992 et 1998
et 1998 ) (figure 1.19
) (figure 1.19 ).
). ) démontre également que des enfants belges dont le père a un haut niveau d'éducation (universitaire ou école supérieure) n'ont pas subi une évolution séculaire de taille finale entre 1960 et 1980 alors que ceux dont le père a un niveau d'éducation plus faible (maximum 9 ans de scolarité) subissent une évolution positive de 3,6 cm (figure 1.20
) démontre également que des enfants belges dont le père a un haut niveau d'éducation (universitaire ou école supérieure) n'ont pas subi une évolution séculaire de taille finale entre 1960 et 1980 alors que ceux dont le père a un niveau d'éducation plus faible (maximum 9 ans de scolarité) subissent une évolution positive de 3,6 cm (figure 1.20 ).
).
 ).
). ; Bielicki et coll., 1992
; Bielicki et coll., 1992 ; Bielicki et Szklarska, 1999
; Bielicki et Szklarska, 1999 ; Li et coll., 2004
; Li et coll., 2004 ; Gyenis et coll., 2004
; Gyenis et coll., 2004 ), les revenus et l'éducation (Meyer et Selmer, 1999
), les revenus et l'éducation (Meyer et Selmer, 1999 ), la grandeur de la famille (Chinn et coll., 1989
), la grandeur de la famille (Chinn et coll., 1989 ), les différences ville-campagne (Weber et coll., 1995
), les différences ville-campagne (Weber et coll., 1995 ; Padez et Johnston, 1999
; Padez et Johnston, 1999 ), la surpopulation de l'habitation (Foster et coll., 1983
), la surpopulation de l'habitation (Foster et coll., 1983 ).
). ) : cela explique que les changements séculaires n'ont pas débuté à la même époque dans les différents pays européens, débutant au XIXe siècle en Angleterre, après dans des pays comme la Belgique (Vercauteren et coll., 1998
) : cela explique que les changements séculaires n'ont pas débuté à la même époque dans les différents pays européens, débutant au XIXe siècle en Angleterre, après dans des pays comme la Belgique (Vercauteren et coll., 1998 ) et les pays scandinaves, seulement au début du XXe siècle en France (Demoulin, 1998
) et les pays scandinaves, seulement au début du XXe siècle en France (Demoulin, 1998 ) et même après en Espagne (Rebato, 1998
) et même après en Espagne (Rebato, 1998 ).
). ). L'évolution séculaire fut aussi non uniforme et plus élevée pendant la période 1970-1985. De plus, la variabilité inter-régionale de taille et d'âge à la ménarche diminue régulièrement de 1960 à 1990 (Rebato, 1998
). L'évolution séculaire fut aussi non uniforme et plus élevée pendant la période 1970-1985. De plus, la variabilité inter-régionale de taille et d'âge à la ménarche diminue régulièrement de 1960 à 1990 (Rebato, 1998 ), le taux le plus élevé d'évolution séculaire étant observé pour les régions au départ les plus défavorisées (figure 1.21
), le taux le plus élevé d'évolution séculaire étant observé pour les régions au départ les plus défavorisées (figure 1.21 ).
). ) et les différents départements français (Demoulin, 1998
) et les différents départements français (Demoulin, 1998 ), où l'augmentation de taille a été plus grande dans les régions où au départ les tailles moyennes étaient moins élevées.
), où l'augmentation de taille a été plus grande dans les régions où au départ les tailles moyennes étaient moins élevées. ) pour les Pays-Bas, par Facchini et coll. (1982
) pour les Pays-Bas, par Facchini et coll. (1982 ), Ulizzi et Terrenato (1982
), Ulizzi et Terrenato (1982 ) pour l'Italie, par Ochoa Zamora et coll. (1981
) pour l'Italie, par Ochoa Zamora et coll. (1981 ), Tojo et coll. (1987
), Tojo et coll. (1987 ), Rebato (1998
), Rebato (1998 ) pour l'Espagne, et par Bielicki (1986
) pour l'Espagne, et par Bielicki (1986 ), Bielicki et coll. (1997) pour la Pologne.
), Bielicki et coll. (1997) pour la Pologne. ).
). ; Susanne et Lepage, 1990
; Susanne et Lepage, 1990 et 1992
et 1992 ). Ainsi, la consommation de protéines essentiellement animales a augmenté, ainsi que la consommation de graisse d'origine animale et végétale. L'évolution de la consommation de sucre est plus contrastée ; elle augmente essentiellement dans les pays du sud (Espagne, Italie, Portugal) où elle partait en 1955 de valeur très basse, mais diminue dans les pays nordiques où la valeur de 1955 était élevée. Comparant les changements séculaires de la taille avec la consommation nutritionnelle, certains parallélismes semblent apparaître pour les pays européens (Susanne et coll., 2001
). Ainsi, la consommation de protéines essentiellement animales a augmenté, ainsi que la consommation de graisse d'origine animale et végétale. L'évolution de la consommation de sucre est plus contrastée ; elle augmente essentiellement dans les pays du sud (Espagne, Italie, Portugal) où elle partait en 1955 de valeur très basse, mais diminue dans les pays nordiques où la valeur de 1955 était élevée. Comparant les changements séculaires de la taille avec la consommation nutritionnelle, certains parallélismes semblent apparaître pour les pays européens (Susanne et coll., 2001 ) en termes de consommation de protéines animales (figure 1.22
) en termes de consommation de protéines animales (figure 1.22 ) mais la relation est moins nette pour les graisses et absente pour le sucre. Aussi, en Galicie (nord-ouest de l'Espagne), des changements très significatifs sont apparus entre 1970 et 1985 avec essentiellement un accroissement de consommation de protéines animales, correspondant aussi à une intensification de l'évolution séculaire (Tojo et coll., 1987
) mais la relation est moins nette pour les graisses et absente pour le sucre. Aussi, en Galicie (nord-ouest de l'Espagne), des changements très significatifs sont apparus entre 1970 et 1985 avec essentiellement un accroissement de consommation de protéines animales, correspondant aussi à une intensification de l'évolution séculaire (Tojo et coll., 1987 ; Rebato, 1998
; Rebato, 1998 ).
).
 ) : en fonction du niveau salarial plus élevé, la consommation de viande, d'œufs, de fromage, de fruits et de légumes augmente. Cette consommation est aussi plus faible dans des familles nombreuses par rapport à des familles de taille plus réduite (Bielicki et coll., 1992
) : en fonction du niveau salarial plus élevé, la consommation de viande, d'œufs, de fromage, de fruits et de légumes augmente. Cette consommation est aussi plus faible dans des familles nombreuses par rapport à des familles de taille plus réduite (Bielicki et coll., 1992 ).
). ) en termes de consommation de viande, de graisse et de sucre ;
) en termes de consommation de viande, de graisse et de sucre ; ) lie l'évolution séculaire à la forte augmentation de consommation de lait après la 2e guerre mondiale.
) lie l'évolution séculaire à la forte augmentation de consommation de lait après la 2e guerre mondiale. ; Wolanski, 1974
; Wolanski, 1974 ). Cette hypothèse trouve son origine dans la mobilité croissante des populations, mobilité à la fois externe et interne, engendrant un plus haut degré d'exogamie. Aucune étude ne met cependant en évidence un lien avec la croissance.
). Cette hypothèse trouve son origine dans la mobilité croissante des populations, mobilité à la fois externe et interne, engendrant un plus haut degré d'exogamie. Aucune étude ne met cependant en évidence un lien avec la croissance. ; van Wieringen, 1986). Les facteurs mésologiques, de santé et de nutrition, semblent, en effet, essentiels. Des parallélismes existent entre des changements séculaires et les revenus moyens ou le produit national brut, mais ils existent également pour les facteurs nutritionnels en termes quantitatifs, de consommation de protéines, de graisse et/ou de sucre. Les éléments les plus significatifs semblent être la consommation de viande ou de protéines animales. Des facteurs qualitatifs peuvent aussi avoir une influence, telles qu'une quantité plus importante de protéines animales par rapport à des protéines végétales, des graisses animales par rapport à des graisses végétales, des produits laitiers améliorés en vitamines, du calcium et du phosphore, des changements nutritionnels chez les nouveau-nés.
; van Wieringen, 1986). Les facteurs mésologiques, de santé et de nutrition, semblent, en effet, essentiels. Des parallélismes existent entre des changements séculaires et les revenus moyens ou le produit national brut, mais ils existent également pour les facteurs nutritionnels en termes quantitatifs, de consommation de protéines, de graisse et/ou de sucre. Les éléments les plus significatifs semblent être la consommation de viande ou de protéines animales. Des facteurs qualitatifs peuvent aussi avoir une influence, telles qu'une quantité plus importante de protéines animales par rapport à des protéines végétales, des graisses animales par rapport à des graisses végétales, des produits laitiers améliorés en vitamines, du calcium et du phosphore, des changements nutritionnels chez les nouveau-nés.