| |
| Med Sci (Paris). 36(4): 336–339. doi: 10.1051/medsci/2020046.Le réservoir viral dans l’infection par le VIH-2,
modèle d’une infection rétrovirale atténuée Assia Samri,1*# Charlotte Charpentier,2* Rémi Cheynier,3 Sophie Matheron,4 Françoise Brun-Vézinet,5** Brigitte Autran,6** and groupe d’étude ANRS CO5 IMMUNOVIR-2◊ 1Sorbonne Université, Inserm U1135, Centre d’immunologie et
des maladies infectieuses, Cimi-Paris, F-75013Paris,
France 2Inserm, IAME, UMR 1137, Universités Paris Diderot et Paris
Nord, Sorbonne Paris Cité ; Laboratoire de virologie, Hôpital Bichat,
AP-HP, Paris, France 3Université de Paris, Institut Cochin, Inserm U1016, CNRS
UMR8104, F-75014Paris,
France 4Inserm, IAME, UMR 1137, Universités Paris Diderot et Paris
Nord, Sorbonne Paris Cité, Service des maladies infectieuses et tropicales,
Hôpital Bichat, AP-HP, Paris, France 5Université Paris7 Denis Diderot,
Paris,
France 6Sorbonne Université, Inserm U1135, Centre d’immunologie et
des maladies infectieuses, Cimi-Paris, AP-HP, Hôpital universitaire
Pitié-Salpêtrière, F-75013Paris,
France MeSH keywords: Lymphocytes T CD4+, Infections à VIH, VIH-2 (Virus de l'Immunodéficience Humaine de type 2), Humains, Mémoire immunologique, Activation des lymphocytes, Charge virale, Latence virale, physiologie, virologie, pathogénicité |
Le virus de l’immunodéficience humaine de type 2 (VIH-2) [1] est un lentivirus responsable d’une infection
moins grave que celle induite par le VIH de type 1 (VIH-1). L’infection par le VIH-2 est
caractérisée par un maintien prolongé du nombre de lymphocytes T CD4+ et par
une charge virale plasmatique indétectable [2]. La progression plus lente de la maladie induite par le VIH-2
pourrait indiquer un équilibre hôte-pathogène plus favorable. La faible charge virale
plasmatique, une des principales caractéristiques de l’infection par le VIH-2, a pour
conséquence un taux de transmission réduit, et une concentration de l’infection en
Afrique occidentale, où 1 à 2 millions de personnes pourraient être infectées [3]. Le génome du VIH-2 est proche
de celui du VIH-1 (50 % d’identité de séquence nucléotidique) [4], et est presque identique à celui du virus de
l’immunodéficience simien (VIS) des singes sooty mangabeys (sm) [5]. De plus, le VIH-2, qui utilise les mêmes
co-récepteurs CCR5 (C-C chemokine receptor 5) et CXCR4 (c-x-c
chemokine receptor 4) que le VIH-1 pour infecter les cellules [6], semble utiliser un plus large
spectre de co-récepteurs alternatifs (CCR1 à CCR8, CXCR6, GPR15 [G
protein-coupled receptor 15], GPR1, APJ [putative receptor protein
related to AT1], CX3CR1 (V28), CXCR5 et RDC1/CXCR7) in
vitro [7]. CXCR6
pourrait être un des co-récepteurs alternatifs majeur du VIH-2 car il serait
préférentiellement utilisé chez les patients avirémiques infectés par le VIH-2 [8] ainsi que dans les infections
par les lentivirus simiens non pathogènes [9]. Comme pour le VIH-1, l’infection par le VIH-2 semble aboutir à la constitution d’un
réservoir de cellules infectées. Cependant, les mécanismes physiopathologiques
expliquant les faibles charges virales du VIH-2 restent peu explorés. Le réservoir
latent et inductible du VIH-1, intégré dans le génome cellulaire, est principalement
localisé dans les lymphocytes T CD4+ à mémoire centrale (T central
memory, TCM) au repos [10] et dans quelques monocytes et macrophages
[11, 12]. Inversement, dans l’infection atténuée
par VISsm, la contribution des TCM au réservoir viral est plus faible que
celle des cellules plus différenciées, du fait de leur faible expression du co-récepteur
CCR5 [13]. De même, une
infection plus réduite des TCM a été observée dans l’infection par le VIH-1 des sujets
« non progresseurs à long terme » (long-term non progressors, LTNP),
porteurs des allèles protecteurs HLA (human leukocyte antigen)-B*27 ou
B*57 [14], ou chez les
« contrôleurs » du VIH-1 post-traitement [12]. Afin de mieux définir les caractéristiques du réservoir du VIH-2, nous avons analysé sa
distribution parmi les cellules sanguines périphériques CD4+ provenant
d’individus suivis dans la cohorte française ANRS-VIH-2 CO5 [15]. Nous avons cherché à savoir si les monocytes
étaient infectés in vivo, et avons testé l’hypothèse d’une infection
plus restreinte des TCM. |
Distribution préférentielle du réservoir du VIH-2 dans les lymphocytes
T CD4 + à mémoire transitionnelle (T transitional memory, TTM) et
absence d’infection des monocytes Des sujets infectés par le VIH-2 et n’ayant reçu aucun traitement antirétroviral (12
individus « non progresseurs », et 2 « progresseurs ») ont été inclus dans une étude
prospective [15]. Les monocytes ainsi que des
sous-populations de lymphocytes T CD4+ au repos - naïfs TN (T
naive), à mémoire centrale TCM, à mémoire transitionnelle TTM,
et à mémoire effectrice TEM (T effector memory) - ont été triés à
partir des cellules mononucléées du sang (CMNS). L’ADN du VIH-2 a été quantifié par
PCR (polymerase chain reaction) en temps réel dans chaque
sous-population triée. Nous avons ainsi montré que le réservoir du VIH-2 diffère du
réservoir du VIH-1 par une absence totale d’infection des monocytes [11, 12,
14] et une infection prédominante des TTM
plutôt que des TCM (Figure 1),
confirmant donc l’hypothèse d’une infection réduite des TCM, comme cela est observé
dans le modèle d’infection non pathogène de singes sooty mangabeys par le
VISsm [13], ainsi que chez les
sujets LTNP [14] ou les contrôleurs
post-traitement infectés par le VIH-1 [12].
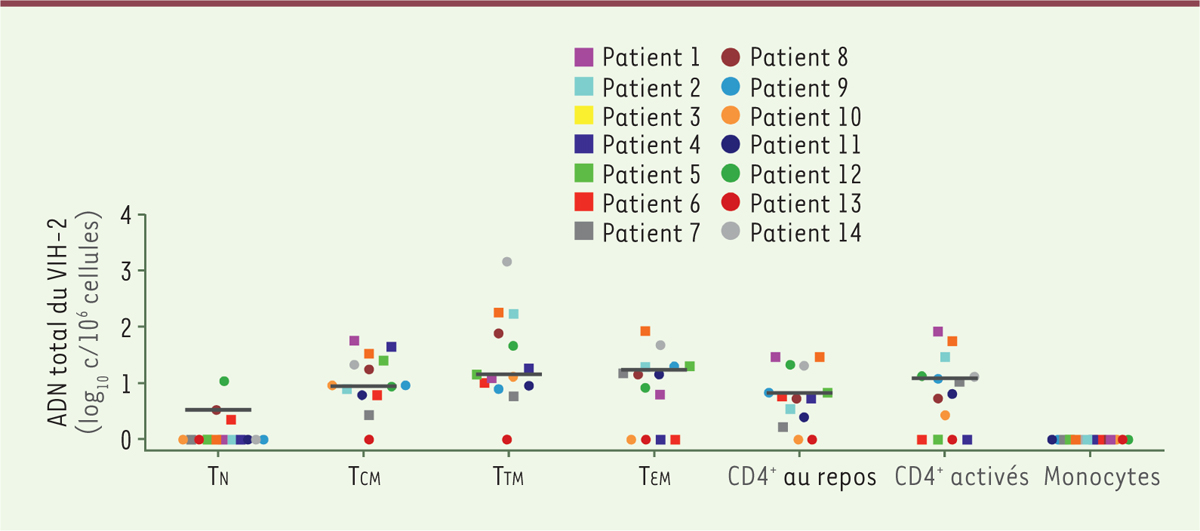
 | Figure 1. Distribution de l’ADN total du VIH-2 dans les monocytes et
différentes sous-populations de lymphocytes T.
L’ADN total du VIH-2 a été quantifié dans différentes populations
cellulaires triées à partir des cellules mononucléées du sang
périphérique (CMNS) chez 14 sujets infectés par le VIH-2. Sept
populations ou sous-populations cellulaires ont été analysées : les
populations de monocytes (CD3- CD4-
CD14+), de lymphocytes T CD4+ activés
(CD25+ CD69+ HLADR+), de
lymphocytes T CD4+ au repos (CD25-
CD69- HLADR-), les sous-populations de lymphocytes T
CD4+ au repos : les lymphocytes T naïfs (TN ;
CD45RA+ CCR7+ CD27+), les
lymphocyte T à mémoire centrale (TCM ; CD45RA-
CCR7+ CD27+), les lymphocytes T à mémoire
transitionnelle (TTM ; CD45RA- CCR7-
CD27+) et les lymphocytes T à mémoire effectrice (TEM ;
CD45RA- CCR7- CD27-). Les résultats sont
exprimés en log10 du nombre de copies (c) d’ADN du VIH-2 par million de
cellules et les valeurs médianes sont indiquées par des barres
horizontales. Chaque symbole représente un sujet. |
|
Faible inductibilité du VIH-2 dans les cellules CD4 +
circulantes Dans notre étude, nous n’avons pu détecter que de faibles niveaux d’ADN du VIH-2 chez
les 14 sujets infectés par le VIH-2 testés, cette infection n’étant quantifiable que
chez 5 d’entre eux. De plus, nous n’avons pu réactiver in vitro la
production virale dans les cellules mononucléées du sang que chez 3 individus,
confirmant la faible productivité, déjà connue, du VIH-2. Bien que ces résultats
puissent refléter les caractéristiques de ces sujets majoritairement « non
progresseurs », des résultats identiques ont été observés chez les 2 sujets
« progresseurs » bien qu’ayant une faible charge virale VIH-2 plasmatique. |
La distribution du réservoir du VIH-2 dans les sous-populations de lymphocytes T
CD4 + mémoires est associée à un déséquilibre de l’expression des
gènes CXCR6 et TRIM5a Afin de mieux comprendre les déterminants de la distribution atypique du réservoir du
VIH-2, nous avons analysé le profil transcriptomique des sous-populations T
CD4+ triées, concernant un total de 96 gènes associés à
l’inflammation, aux cytokines, aux chimiokines, et aux voies de signalisation de
l’interféron, avec un intérêt particulier pour les co-récepteurs alternatifs du VIH
tels que CXCR6 [8] et pour des facteurs de
restriction potentiels du VIH-2 tels que TRIM5α (tripartite motif protein
5a). L’ADN du VIH-2 n’étant détectable que dans les cellules TTM et
TCM, nous avons concentré notre analyse sur ces deux sous-populations. Les résultats
obtenus ont permis de montrer que le gène CXCR6 était moins exprimé
dans les TCM que dans les TTM (Figure
2), et nous avons pu confirmer cette différence en analysant
l’expression de la protéine CXCR6 par cytométrie en flux (Figure 3A). Comme il a été récemment
montré que l’utilisation du CXCR6 caractérise l’infection par les lentivirus non
pathogènes [9] et qu’elle est abrogée par la
présence d’une proline en position 326 de la boucle V3 de la glycoprotéine
d’enveloppe gp105, nous avons examiné les 259 séquences de gp105 du VIH-2 dont nous
disposions pour la cohorte ANRS-VIH-2, mais aucune de ces séquences ne comportait
une proline à cette position.
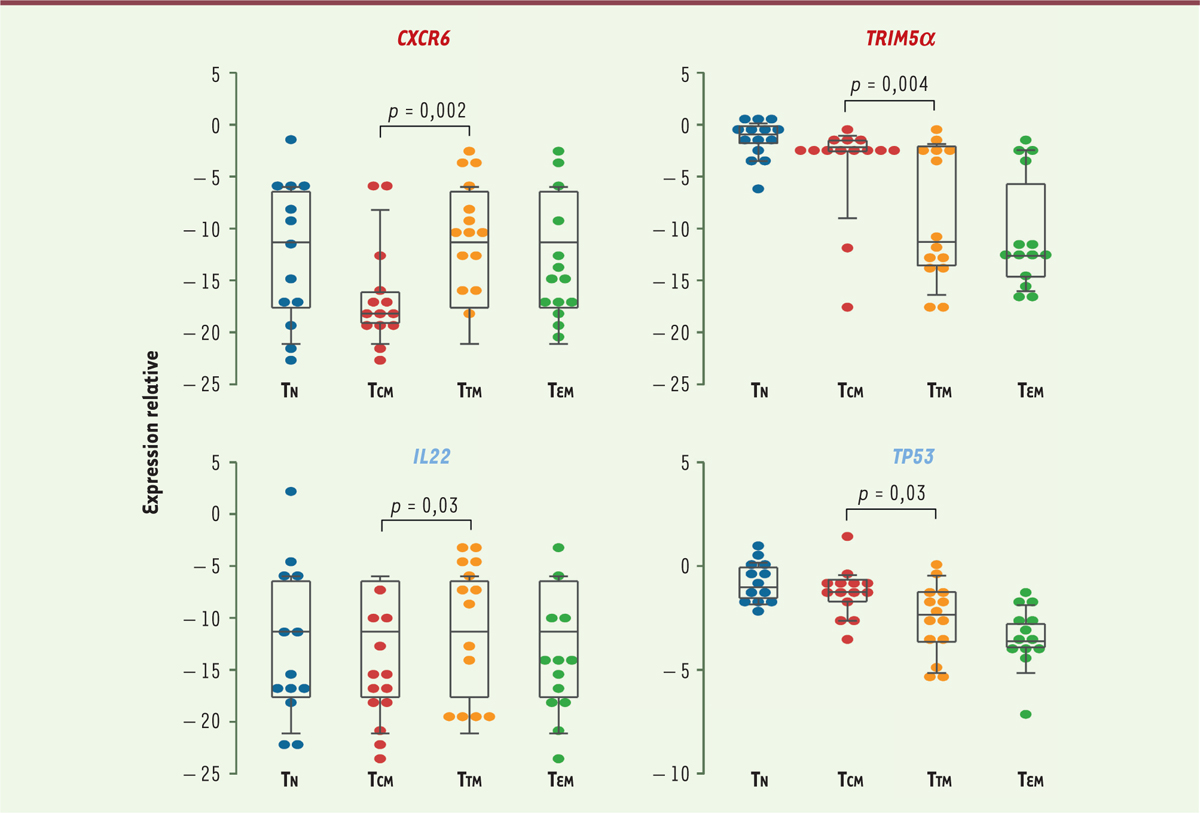
 | Figure 2. Analyse transcriptomique des monocytes et des
sous-populations de lymphocytes T CD4+ au
repos. Une analyse des transcrits de 96 gènes a
été réalisée dans les monocytes (CD3- CD4-
CD14+) et les sous-populations de lymphocytes T
CD4+ au repos : les lymphocytes T naïfs (TN ;
CD45RA+ CCR7+ CD27+), les
lymphocytes T à mémoire centrale (TCM ; CD45RA-
CCR7+ CD27+), les lymphocytes T à mémoire
transitionnelle (TTM ; CD45RA- CCR7-
CD27+), et les lymphocytes T à mémoire effectrice (TEM ;
CD45RA- CCR7- CD27-) de 14 sujets
infectés par le VIH-2. La figure montre l’expression relative des gènes
CXCR6, TRIM5a, IL22, et TP53 dans les sous-populations de lymphocytes T
CD4+ au repos. L’expression de ces gènes a été normalisée
par rapport à celle du gène « de ménage » RPS14. |
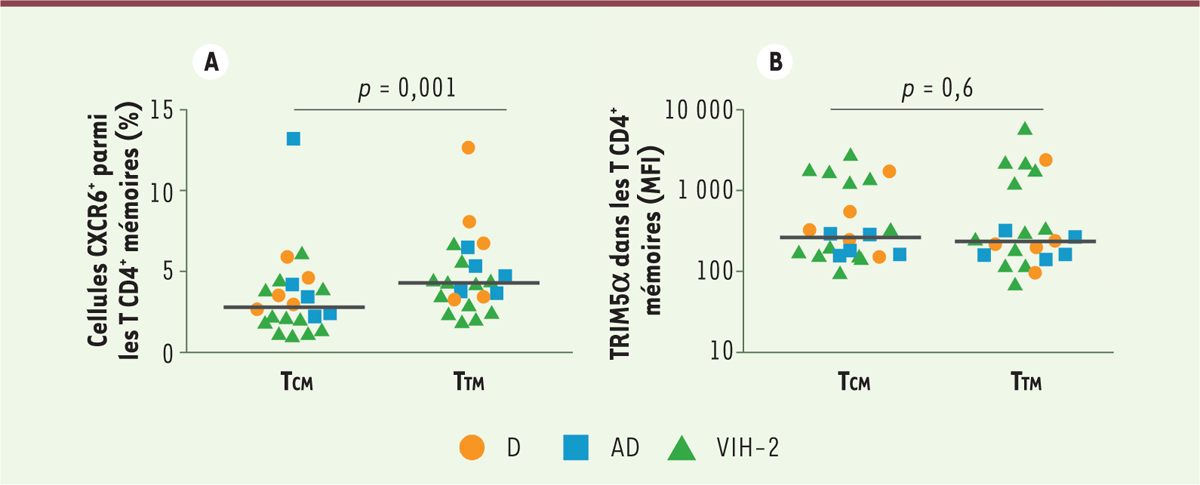
 | Figure 3. Analyse de l’expression des protéines CXCR6 et TRIM5a dans
les lymphocytes T CD4+ TCM et TTM par cytométrie en
flux. Analyse des lymphocytes T CD4+
à mémoire centrale (TCM ; CD45RA- CCR7+
CD27+) et transitionnels (TTM ; CD45RA-
CCR7- CD27+) par cytométrie en flux chez 12
sujets infectés par le VIH-2 (triangles), 5 donneurs ouest-africains
non-infectés (AD, carrés) et 4 autres donneurs non-infectés de
l’Établissement français du sang (D, ronds). La figure montre le
pourcentage de cellules CXCR6+ parmi les lymphocytes T
CD4+ mémoire en A, et l’intensité moyenne de fluorescence
(MFI) de TRIM5a intracellulaire en B. Chaque symbole représente un
sujet, et les valeurs médianes pour chaque groupe sont indiquées par des
barres horizontales. |
L’analyse transcriptomique a également montré que le gène TRIM5α
était plus exprimé dans les TCM que dans les TTM (Figure 2), mais l’analyse de l’expression de la
protéine par cytométrie en flux n’a pas permis de confirmer cette différence
(Figure 3B). Alors que
TRIM5α n’a pas d’effet sur l’infection par le VIH-1, c’est un
puissant facteur de restriction du VIS. Du fait de la similitude des séquences de
capside entre VISsm et VIH-2, le VIH-2 montre des niveaux élevés de
sensibilité au TRIM5α humain [16]. TRIM5α pourrait donc
également contribuer à réduire l’infection par le VIH-2 des TCM par rapport aux
TTM. Ainsi, nos résultats indiquent que la faible expression de CXCR6 et,
dans une moindre mesure, la surexpression de TRIM5α par les TCM
[15], pourraient expliquer les
différences de contribution des différentes sous-populations de cellules T
CD4+ mémoires aux réservoirs latents du VIH-2 et du VIH-1. En conclusion, ce travail a identifié deux éléments caractéristiques de la
distribution du réservoir du VIH-2 dans les cellules mononucléées du sang
périphérique de personnes infectées par ce virus, progressant ou non dans la
maladie. L’absence d’infection des monocytes par le VIH-2, alors que ces cellules
servent fréquemment de réservoir au VIH-1, suggère que le virus VIH-2, dérivé du
VIS, est mal adapté aux cellules de la lignée myéloïde. Par ailleurs, la plus faible
infection des lymphocytes T CD4+ à mémoire centrale, conséquence d’une
moindre expression du co-récepteur CXCR6, et peut-être de la présence plus
importante du facteur de restriction TRIM5a, suggère que le VIH-2 pourrait également
être moins adapté aux lymphocytes T CD4+ à mémoire centrale que ne l’est
le VIH-1. L’ensemble de ces résultats suggère que cette distribution particulière du
réservoir du VIH-2 pourrait être liée en partie à des facteurs clés de l’hôte,
jetant ainsi un nouvel éclairage sur la moindre pathogénicité du VIH-2, encore mal
comprise. Ce travail s’inscrit dans le cadre du programme ANRS Immunovir2, qui a
également permis de montrer que des réponses immunes puissantes, par l’intermédiaire
des cellules NK (natural killer) ou des lymphocytes T
CD8+, pouvaient contribuer au contrôle prolongé de l’infection par le
VIH-2, suggérant que plusieurs modalités de la relation hôte-virus régissent la
faible pathogénicité du VIH-2. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données
publiées dans cet article.
|
1.
Clavel
F
,
Guetard
D
,
Brun-Vezinet
F
, et al.
Isolation of a new human retrovirus from West African patients
with AIDS . Science.
1986; ; 233 :
:343.–346. 2.
Nyamweya
S
,
Hegedus
A
,
Jaye
A
, et al.
Comparing HIV-1 and HIV-2 infection: lessons for viral
immunopathogenesis . Rev Med Virol.
2013; ; 23 :
:221.–240. 3.
Visseaux
B
,
Damond
F
,
Matheron
S
, et al.
HIV-2 molecular epidemiology . Infect
Genet Evol.
2016; ; 46 :
:233.–240. 4.
De Silva
TI
,
Cotten
M
,
Rowland-Jones
SL
. HIV-2: the forgotten AIDS virus .
Trends Microbiol.
2008; ; 16 :
:588.–595. 5.
Santiago
ML
,
Range
F
,
Keele
BF
, et al.
Simian immunodeficiency virus infection in free-ranging sooty
mangabeys (Cercocebus atys atys) from the Tai Forest, Côte d’Ivoire:
implications for the origin of epidemic human immunodeficiency virus type
2 . J Virol.
2005; ; 79 :
:12515.–12527. 6.
Sol
N
,
Ferchal
F
,
Braun
J
, et al.
Usage of the coreceptors CCR-5, CCR-3, and CXCR-4 by primary and
cell line-adapted human immunodeficiency virus type 2 .
J Virol.
1997; ; 71 :
:8237.–8244. 7.
Shimizu
N
,
Soda
Y
,
Kanbe
K
, et al.
A putative G protein-coupled receptor, RDC1, is a novel
coreceptor for human and simian immunodeficiency viruses .
J Virol.
2000; ; 74 :
:619.–626. 8.
Blaak
H
,
Boers
PH
,
Gruters
RA
, et al.
CCR5, GPR15, and CXCR6 are major coreceptors of human
immunodeficiency virus type 2 variants isolated from individuals with and
without plasma viremia . J Virol.
2005; ; 79 :
:1686.–1700. 9.
Wetzel
KS
,
Yi
Y
,
Yadav
A
, et al.
Loss of CXCR6 coreceptor usage characterizes pathogenic
lentiviruses . PLoS Pathog.
2018; ; 14 :
:e1007003.. 10.
Chomont
N
,
El-Far
M
,
Ancuta
P
, et al.
HIV reservoir size and persistence are driven by T cell survival
and homeostatic proliferation . Nat Med.
2009; ; 15 :
:893.–900. 11.
Bacchus
C
,
Cheret
A
,
Avettand-Fenoel
V
, et al.
A single HIV-1 cluster and a skewed immune homeostasis drive the
early spread of HIV among resting CD4+ cell subsets within one
month post-infection . PLoS One.
2013; ; 8 : :e64219.. 12.
Saez-Cirion
A
,
Bacchus
C
,
Hocqueloux
L
, et al.
Post-treatment HIV-1 controllers with a long-term virological
remission after the interruption of early initiated antiretroviral therapy
ANRS VISCONTI Study . PLoS Pathog.
2013; ; 9 :
:e1003211.. 13.
Paiardini
M
,
Cervasi
B
,
Reyes-Aviles
E
, et al.
Low levels of SIV infection in sooty mangabey central memory
CD4+ T cells are associated with limited CCR5
expression . Nat Med.
2011; ; 17 :
:830.–836. 14.
Descours
B
,
Avettand-Fenoel
V
,
Blanc
C
, et al.
Immune responses driven by protective human leukocyte antigen
alleles from long-term nonprogressors are associated with low HIV reservoir
in central memory CD4+ T cells . Clin
Infect Dis.
2012; ; 54 :
:1495.–1503. 15.
Samri
A
,
Charpentier
C
,
Diallo
MS
, et al.
Limited HIV-2 reservoirs in central-memory CD4+
T-cells associated to CXCR6 co-receptor expression in attenuated HIV-2
infection . PLoS Pathog.
2019; ; 15 :
:e1007758.. 16.
Takeuchi
JS
,
Perche
B
,
Migraine
J
, et al.
High level of susceptibility to human TRIM5a conferred by HIV-2
capsid sequences . Retrovirology.
2013; ; 10 : :50.. |