Médicaments psychotropes
Consommations et pharmacodépendances
2012
→ Aller vers ANALYSE
D’après les sources institutionnelles, l’utilisation globale de médicaments psychotropes en France est estimée comme étant l’une des plus élevées en Europe. Les principaux médicaments psychotropes classiquement distingués sont les tranquillisants ou anxiolytiques, les somnifères ou hypnotiques, les neuroleptiques ou antipsychotiques, les antidépresseurs et les thymorégulateurs. D’autres médicaments qui peuvent agir sur l’activité psychique sont également considérés dans les études disponibles : les psychostimulants, les analgésiques opiacés et les médicaments de substitution aux opiacés.
Des enquêtes déclaratives comme le Baromètre santé mené tous les cinq ans en France sur un échantillon représentatif de la population générale permettent de connaître la consommation de médicaments psychotropes et de suivre les tendances de consommation en particulier des tranquillisants et somnifères appartenant en majorité à la classe des benzodiazépines (médicaments psychotropes les plus consommés). Toujours plus élevée chez les femmes que chez les hommes, la consommation d’au moins un médicament psychotrope en 2010 concerne moins d’un quart de la population des 18-75 ans et atteint un plateau vers l’âge de la cinquantaine. Si les médicaments consommés sont essentiellement des médicaments prescrits, les enquêtes déclaratives ne permettent pas de savoir s’ils sont utilisés aux doses et fréquences indiquées sur l’ordonnance. Par ailleurs, les travaux analysés dans cette expertise n’abordent pas l’adéquation de la prescription avec les indications définies par l’autorisation de mise sur le marché du médicament. Cette question importante mérite une expertise à part entière. Dans ce rapport, le terme de mésusage en population générale est ainsi réservé à un usage non conforme à une prescription établie par un médecin ou à un usage hors prescription. Le terme de détournement sera réservé, dans la mesure du possible, au mode d’obtention détournée du médicament.
Dans les études en population générale, plusieurs sous-groupes (populations cliniques, usagers de drogues...) échappent à l’évaluation et il faut avoir recours à des études spécifiques. Chez les usagers de drogues, des études menées à partir des centres d’accueil et de soins ont conduit à caractériser différentes situations d’usage. Dans cette population, la consommation de médicaments psychotropes non prescrits (mésusage) est importante et la consommation de médicaments psychotropes prescrits s’accompagne souvent de mésusage tant du point de vue des doses absorbées, des fréquences d’utilisation que des modes d’administration. Les motivations et contextes de l’usage et du mésusage sont très variés : visées thérapeutique, récréative ou toxicomaniaque. L’approvisionnement en médicaments psychotropes peut provenir de polyprescriptions (nomadisme médical) ou encore de voies illicites de distribution (marché de rue...). Les médicaments de substitution aux opiacés (MSO) prescrits aux usagers de drogues font également l’objet de mésusage sous forme de non respect des doses et d’injections (principalement la buprénorphine haut dosage, BHD) et le détournement alimente le marché illicite. Mésusages et détournements de médicaments psychotropes sont de même rencontrés en milieu carcéral. Des dispositifs mis en place en France sont susceptibles d’alerter sur l’émergence de nouveaux médicaments détournés.
La pharmacodépendance est une conséquence problématique d’une consommation chronique et de l’abus de certains médicaments psychotropes, en particulier des benzodiazépines. Des consommations couvrant plusieurs années sont fréquemment observées. Cependant, l’enjeu de santé publique en France de telles consommations ne peut pas être évalué tant que la prévalence de la dépendance en population générale n’est pas mesurée. D’après les études internationales, chez les patients suivis pour des troubles psychiatriques, la prévalence de la dépendance aux médicaments psychotropes semble plus élevée qu’en population générale et des facteurs de risque communs (biologiques ou sociaux) sont suspectés dans cette population.
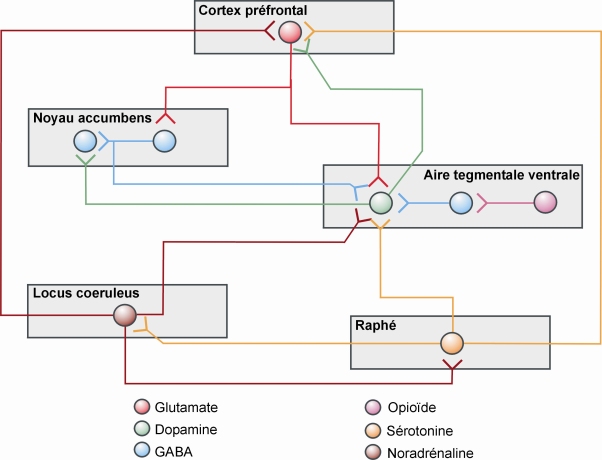
Connaître les mécanismes neurobiologiques qui conduisent à une pharmacodépendance constitue un champ de recherche en plein essor. Comme pour toute substance psychoactive, les études menées dans le domaine expérimental renseignent sur les propriétés renforçantes d’un médicament psychotrope à l’origine du maintien, voire d’une augmentation de sa consommation. Ces travaux permettent de caractériser le potentiel d’abus et de dépendance de différents médicaments psychotropes et peuvent s’intégrer dans l’évaluation de ce risque avant la mise sur le marché. Des recherches fondamentales renseignent sur les cibles de ces médicaments et permettent de les comparer à celles de substances psychoactives de référence (alcool, tabac, cocaïne...). Associé à un autre produit psychoactif (licite ou illicite), un médicament psychotrope peut provoquer des effets plus prononcés. Par ailleurs, un mode de consommation inadapté (augmentation des doses ou de la fréquence des prises, injection...) peut accroître les concentrations cérébrales du produit. Comme pour toutes les addictions, des vulnérabilités individuelles s’exprimant dans des contextes d’usage particuliers entrent en jeu dans la survenue d’une pharmacodépendance.
Outre la pharmacodépendance, les complications somatiques aiguës liées au mésusage de médicaments psychotropes peuvent être à l’origine de morbidité et de mortalité. Par ailleurs, l’exploration des conséquences (à court et long terme) tant cliniques que neurobiologiques d’une exposition précoce (fœtus, enfant) aux médicaments psychotropes est un champ de recherche encore insuffisamment développé.
Afin de limiter le mésusage, l’abus des substances psychoactives médicamenteuses et la pharmacodépendance, des politiques publiques, mises en place au plan international et national, interviennent à différentes étapes du développement du médicament et tout au long de son parcours. Les stratégies élaborées au niveau national peuvent concerner le champ éducatif, inclure des recommandations de bonne pratique clinique et des interventions auprès des professionnels de santé et/ou des patients. Pour éviter le détournement, une réglementation de la prescription et de la délivrance et une réduction de l’accessibilité à ces médicaments sont des mesures qui, pour certaines, ont fait l’objet d’évaluations dans quelques pays.
Comparée aux autres pays européens, la consommation de médicaments psychotropes en France est parmi les plus élevées
Différentes sources institutionnelles internationales ou nationales fournissent des données sur l’utilisation de médicaments psychotropes, le terme « utilisation » faisant référence aux données de vente, de remboursement, voire de production ; ces données ne permettent donc pas d’apprécier directement les niveaux réels de consommation. Les données d’utilisation de médicaments sont agrégées en quantité de substance par nombre d’habitants (le plus souvent selon la méthodologie standardisée proposée par l’Organisation mondiale de la santé, c’est-à-dire en dose définie journalière (DDJ) pour 1 000 habitants et par jour, ou DID
1
La dose définie journalière (DDJ) ou DDD (Defined Daily Dose en anglais) correspond à la posologie journalière théorique (exprimée le plus souvent en gramme) d’une substance médicamenteuse utilisée dans son indication principale chez l’adulte. Pour les comparaisons d’utilisation internationale et au cours du temps, l’OMS recommande d’utiliser la DID (Ddd/1 000 Inhabitants/Day), correspondant au nombre de DDJ pour 1 000 habitants et par jour.
), ou en unités standards dans les rapports réalisés à partir des données de vente le plus fréquemment issues de l’
IMS-Health (International Marketing Services-Health). Il existe également des données issues d’études spécifiques correspondant à des enquêtes déclaratives sur un échantillonnage de la population générale ou sur des populations ciblées, qui permettent d’estimer directement les niveaux réels de consommation par les sujets.
Parmi les données institutionnelles les plus systématiques, les rapports annuels de l’OICS (Organe international de contrôle des stupéfiants) sur les stupéfiants et les substances psychotropes permettent de comparer dans le temps les niveaux d’utilisation par pays. Ces données présentées en s-DDD
2
s-DDD : Dose définie journalière à des fins statistiques. Terminologie utilisée par l’OICS (Organe international de contrôle des stupéfiants) et adaptée du principe de la DDJ
s’appliquent au champ des stupéfiants (quel qu’en soit le statut, médicament ou non) et à celui des médicaments psychotropes (sédatifs-hypnotiques, anxiolytiques, antiépileptiques et stimulants). Elles correspondent aux informations transmises par les États et sont le plus souvent déterminées à partir de la différence entre la quantité de principe actif produite et/ou importée et celle exportée. Il faut rester prudent dans l’exploitation de ces données, notamment pour la comparaison entre pays, car il s’agit de données agrégées d’utilisation et les renseignements sur la fabrication et le commerce fournis par les États peuvent être incomplets.
Malgré les limites soulignées, les données de l’OICS permettent de comparer la France à ses voisins européens pour les niveaux d’utilisation de 9 médicaments qui relèvent des conventions internationales sur les stupéfiants (1961) et sur les substances psychotropes (1971) : buprénorphine, codéine, fentanyl, hydrocodone, hydromorphone, méthadone, morphine, oxycodone, pethidine. Elles permettent également des comparaisons pour quelques médicaments psychotropes : benzodiazépines hypnotiques, benzodiazépines anxiolytiques, benzodiazépines antiépileptiques, psychostimulant comme le méthylphénidate, et carbamates. D’après le rapport de l’OICS publié en 2010, pour les benzodiazépines anxiolytiques, la France apparaît comme un pays au niveau d’utilisation élevé avec 57 s-DDJ/1 000 habitants/jour, en 4e position en Europe après la Belgique, le Portugal et l’Espagne. Pour les hypnotiques en général (benzodiazépines et autres), elle se situe en 2e position après la Belgique, avec 44 s-DDJ/1 000 habitants/jour. En revanche, la France est très largement en retrait pour les psychostimulants et les opiacés. Le niveau d’utilisation de méthylphénidate est 40 fois inférieur à celui du pays le plus consommateur (Islande). Concernant les MSO, le niveau d’utilisation de la buprénorphine est largement supérieur en Grande-Bretagne et en Belgique, par rapport à celui de la France. De même, l’utilisation de la méthadone est importante en Grande-Bretagne, en Irlande, dans les pays scandinaves, et surtout en Suisse où le niveau est 5 fois plus élevé qu’en France.
L’Afssaps publie depuis 1998 un rapport annuel sur l’analyse des ventes de médicaments aux officines et aux hôpitaux en France, permettant d’apprécier leur évolution dans le temps et éventuellement de la comparer à d’autres pays disposant du même type de recueil de données. Entre 2002 et 2009, on constate une discrète décroissance d’utilisation de la classe des anxiolytiques (de 60 DDJ à 53 DDJ/1 000 habitants/jour) et une stabilité d’utilisation des hypnotiques (autour de 33 DDJ/1 000 habitants/jour). En 2012, un rapport de l’Afssaps sur la consommation de benzodiazépines en France confirme cette décroissance pour les benzodiazépines et apparentés.
Plusieurs études déclaratives en population générale ont été menées au cours des dernières décennies au niveau de l’Europe. L’étude EseMed (European Study of the Epidemiology of Mental Disorders) (2001 et 2003) aborde la prévalence de consommation de 4 groupes de substances (antidépresseurs, anxiolytiques-hypnotiques, antipsychotiques, régulateurs de l’humeur) dans une population de plus de 20 000 personnes adultes de 6 pays européens (France, Allemagne, Belgique, Espagne, Pays-Bas et Italie). Les prévalences sont plus élevées en France que dans les autres pays européens dont la moyenne de consommation déclarée au cours des 12 derniers mois est de 10 % pour les anxiolytiques ou hypnotiques (18 % en France) et de 3,5 % pour les antidépresseurs (6 % en France). S’il existe de nombreuses données nord-américaines sur la consommation d’analgésiques opiacés en population générale, la seule étude européenne disponible de type déclaratif sur la douleur chronique (2006) rapporte une prévalence d’utilisation des analgésiques opiacés « faibles » (tramadol, codéine, dextropropoxyphène) et « forts » (morphine, fentanyl, oxycodone...) très largement inférieure en France par rapport au Royaume-Uni, à l’Irlande ou aux pays scandinaves (NorvègeSuède) (de l’ordre de deux à trois fois inférieure).
D’autres études ciblent la consommation de médicaments dans des sous-groupes de population telles que l’enquête internationale Espad (European School Survey Project on Alcohol and Other Drugs) menée chez les adolescents de 16 ans dans plusieurs pays européens. La France partage avec l’Italie, la Lituanie, Monaco et la Pologne une prévalence vie entière de consommation de médicaments psychotropes (anxiolytiques-hypnotiques) sans prescription médicale supérieure à 10 % en 2007 (15 % en France) alors que la prévalence moyenne est de 6 % pour l’ensemble des pays européens. En parallèle, la prévalence moyenne de consommation médicale (avec prescription) est de 8 % pour l’ensemble des pays et d’environ 13 % en France.
Au cours de l’année 2010, environ 18 % de la population française déclarent avoir consommé au moins un médicament psychotrope
Différentes enquêtes déclaratives régulières mises en place depuis plusieurs années permettent de suivre la consommation de médicaments psychotropes en population générale : l’enquête Baromètre santé représentative de la population générale ; l’enquête Escapad (Enquête sur la santé et les consommations lors de l’appel de préparation à la défense) menée chez les jeunes de 17 ans ; et deux enquêtes en milieu scolaire (Espad : European School Survey Project on Alcohol and Other Drugs ; HBSC : Health Behaviour in School-Aged Children).
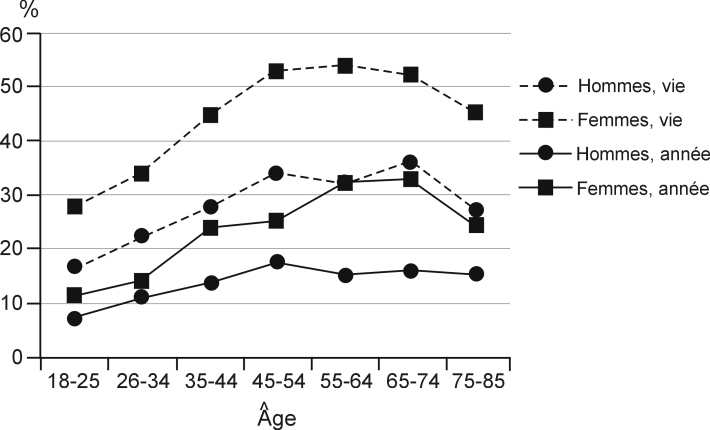
Selon les données de l’édition 2010 du Baromètre santé, environ 18 % de la population de 18 à 75 ans ont consommé des médicaments psychotropes au cours de l’année écoulée, et 36 % au cours de la vie. Les sujets consommateurs de médicaments psychotropes sont majoritairement des femmes : 23 % versus 13 % chez les hommes au cours de l’année écoulée. La prévalence de sujets consommateurs augmente régulièrement avec l’âge : jusqu’à 55-64 ans chez les femmes (prévalence supérieure à 30 %) et jusqu’à 45-54 ans chez les hommes (prévalence d’environ 18 %) au cours de l’année écoulée. Comparée à l’édition 2005 du Baromètre santé, la prévalence au cours de l’année a augmenté chez les hommes et les femmes.
La prévalence des consommateurs de médicaments psychotropes a été analysée par classe de médicaments : au cours de l’année, les prévalences des sujets consommant des anxiolytiques, des somnifères et des antidépresseurs sont respectivement de 10 %, 6 % et 6 %. La prévalence de consommation de thymorégulateurs au cours de l’année est de 0,7 %. Quelle que soit la classe des médicaments psychotropes, leur usage est plus élevé chez les femmes, notamment pour les antidépresseurs et anxiolytiques.
La prise de médicaments psychotropes varie peu selon les catégories socioprofessionnelles, à l’exception des cadres et des professions intellectuelles supérieures qui en consommeraient moins. Par ailleurs, la prévalence de consommation au cours des douze derniers mois ne dépend pas de la situation professionnelle travail versus chômage.
Chez les 55-64 ans, l’usage dans l’année des médicaments psychotropes n’est pas différent entre les actifs et les retraités (24 % dans les deux cas). Les données du Baromètre santé 2005 indiquaient, chez les 60-75 ans inactifs, une différence nette selon le statut marital, les personnes seules (veuves ou non) ayant une prévalence de consommation légèrement supérieure à 30 %.
Selon les données de l’enquête Escapad (Enquête sur la santé et les consommations lors de l’appel de préparation à la défense) de 2008, les jeunes de 17 ans sont 18 % à avoir expérimenté
3
Expérimentation : au moins un usage au cours de la vie (cet indicateur sert principalement à mesurer la diffusion d’un produit dans la population)
des tranquillisants, 15 % des somnifères, 7 % des antidépresseurs, 2 % des thymorégulateurs, 1 % des neuroleptiques et 1 % un psychostimulant (méthylphénidate ou Ritaline®). Selon les premiers résultats de l’enquête Escapad de 2011, 15 % des jeunes de 17 ans ont pris au cours de leur vie des tranquillisants, 11 % des somnifères et 5,6 % des antidépresseurs ; ces prévalences apparaissent en baisse par rapport à celles de 2008. La consommation des médicaments psychotropes concerne davantage les jeunes filles : 23 % d’entre elles pour les tranquillisants (
versus 14 % chez les garçons), 17 % pour les somnifères (
versus 12 %) et 10 % pour les antidépresseurs (
versus 5 %) d’après l’enquête de 2008. En revanche, la consommation de méthylphénidate est deux fois plus répandue chez les garçons. C’est dans le cadre d’une prescription médicale que les antidépresseurs, les neuroleptiques et le méthylphénidate sont principalement consommés (par 3/4 des sujets), suivis par les tranquillisants et les régulateurs de l’humeur (2/3 des sujets) et les somnifères (1/3 des sujets). Les somnifères sont les médicaments les plus consommés hors de tout contrôle médical : lors de la dernière prise, les adolescents les ont obtenus par leurs parents (37 % des cas) ou les ont pris de leur propre initiative (20 % des cas).
Selon les données de l’enquête Espad (European School Survey Project on Alcohol and Other Drugs) de 2007, l’expérimentation de tranquillisants ou de somnifères sans prescription médicale concerne 15 % des élèves de 16 ans en France (12 % de garçons et 18 % de filles) ; en parallèle, la prévalence de l’utilisation médicale (avec prescription médicale) est d’environ 13 %. La prise concomitante d’alcool et de médicaments psychotropes est déclarée par 6 % des élèves (4 % de garçons et 8 % de filles). Concernant la perception de l’accessibilité de médicaments psychotropes, 36 % considèrent qu’il est « assez à très facile de se les procurer » contre 23 % « impossible de se les procurer ». Très peu de changements ont été observés entre 2003 et 2007. Dans l’enquête HBSC (Health Behaviour in School-Aged Children) de 2006, menée également en milieu scolaire, la consommation de médicaments psychotropes « pour se droguer » est citée par 2 % des élèves de 15 ans (3 % de filles et 1 % de garçons).
D’après l’exploitation des sources de données évoquées ci-dessus (Baromètre santé, Escapad, Espad), le nombre d’expérimentateurs de médicaments psychotropes (usage médical et usage non médical) en France est estimé à 16 millions (soit environ 30 % de la population âgée de 11-75 ans). À titre de comparaison, le nombre d’expérimentateurs de tabac est environ deux fois supérieur et le nombre d’expérimentateurs de cannabis légèrement inférieur, plaçant la consommation de médicaments psychotropes en 3e position après l’alcool et le tabac. Les consommateurs occasionnels (au moins un usage dans l’année) seraient 11 millions, soit près de trois fois plus que les consommateurs occasionnels de cannabis.
Chez les personnes âgées, les données recueillies à l’entrée (année 1988-1989) dans la cohorte Paquid (Personnes Âgées QUID) indiquaient que 39 % des personnes vivant à domicile et 66 % des personnes en institution consommaient au moins un médicament psychotrope. Alors que 90 à 95 % des sujets sont traités par au moins un médicament, les médicaments psychotropes sont en deuxième position après les médicaments à visée cardiovasculaire. Pour 32 % des personnes vivant à domicile et 43 % des personnes en institution, il s’agit d’une benzodiazépine. La majorité des sujets n’avait fait usage que d’une seule benzodiazépine. Les principales caractéristiques associées à l’utilisation de benzodiazépines sont les antécédents de pathologie mentale et une dégradation de l’état de santé.
Près d’un quart des assurés du régime général d’Assurance maladie ont bénéficié du remboursement d’au moins un médicament psychotrope en 2000
Les bases de données de remboursement de l’Assurance maladie constituent une source d’informations sur les prescriptions de médicaments psychotropes et permettent d’estimer indirectement la consommation.
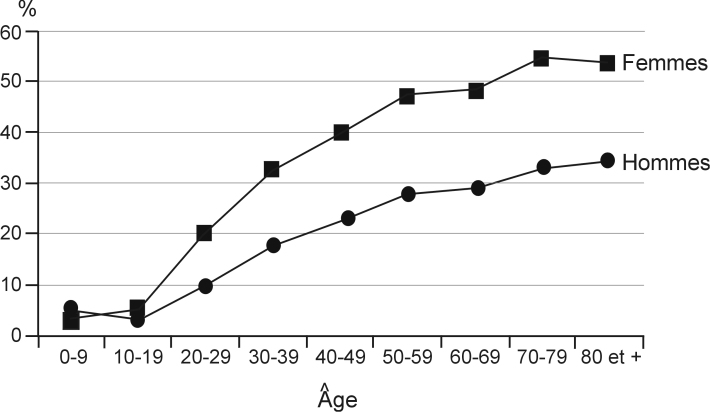
D’après l’étude de la Cnamts de 2000, près d’un quart des sujets (24,5 %) du régime général ont eu au moins une ordonnance portée au remboursement avec au moins un médicament psychotrope au cours de l’année. Le taux annuel de personnes avec remboursement de médicaments psychotropes est plus élevé chez les femmes (31 %) que chez les hommes (17 %). Ce taux augmente avec l’âge. Il atteint environ 50 % des femmes de la tranche d’âge des 50-59 ans. Chez les hommes, le taux de remboursement augmente plus lentement, pour atteindre 34,5 % chez les hommes les plus âgés.
Pour les assurés qui ont eu au moins une ordonnance remboursée avec au moins un médicament psychotrope, il s’agissait dans plus de 80 % des cas d’anxiolytiques et dans environ 40 % des cas d’antidépresseurs ou d’hypnotiques. Les femmes étaient environ deux fois plus consommatrices que les hommes quelle que soit la classe de médicaments. D’après le rapport 2012 de l’Afssaps, le taux de prévalence annuelle d’exposition à au moins une benzodiazépine est estimé à 20 % des sujets affiliés au régime général (ce qui est compatible avec le taux de prévalence annuel aux médicaments psychotropes précédemment cité en 2000).
Les assurés en affections longue durée (ALD) représentent 25 % des consommateurs de médicaments psychotropes. Alors que les affections mentales sont estimées à 2 % des ALD, ce sont les affections chroniques non psychiatriques et les troubles somatiques qui apparaissent comme « facteurs » de prescription de médicaments psychotropes.
Alors que les personnes bénéficiant de la couverture maladie universelle (CMU) représentent 6,3 % des affiliés au régime général (taux standardisé sur l’âge des consommateurs de médicaments psychotropes), elles représentent 9,5 % des personnes traitées par les médicaments psychotropes et 20,5 % des personnes traitées pour dépendance alcoolique.
Ce sont très largement les médecins généralistes qui sont prescripteurs de médicaments psychotropes. D’après l’étude de la Cnamts 2000, sur 18 régions, le suivi par un médecin généraliste est retrouvé dans 90 % des cas. Le suivi psychiatrique est identifié pour 10 % des personnes recevant un anxiolytique ou hypnotique, pour 17 % des assurés recevant un antidépresseur et pour 49 % des personnes recevant du lithium.
En 2008, près de 30 % des usagers de drogues déclarent avoir consommé des médicaments psychotropes (hors médicament de substitution aux opiacés) au cours du dernier mois
Les principaux médicaments psychotropes, hors médicaments de substitution aux opiacés (MSO), susceptibles d’être utilisés par les usagers de drogues sont d’une part des sédatifs, les benzodiazépines et apparentés et, d’autre part des opiacés (essentiellement les sulfates de morphine et, dans une moindre mesure, les dérivés codéinés).
Parmi les usagers actifs
4
Le terme « actif » signifie que l’usager continue à prendre des substances psychoactives illicites ou à détourner des médicaments psychotropes de leurs objectifs thérapeutiques, par opposition aux patients abstinents (sous traitement de substitution ou autre traitement psychotrope non détourné, ou sevrés).
rencontrés dans les Caarud (Centres d’accueil et d’accompagnement à la réduction des risques pour usagers de drogues) en 2008, 28 % déclaraient avoir consommé des benzodiazépines au cours du mois précédent, quotidiennement pour plus de la moitié d’entre eux. Quant à la population suivie en médecine générale, la prévalence d’usage au cours des 7 derniers jours était de 28 % en 2009. En revanche, les personnes qui fréquentent l’espace festif proche de la culture « techno » en consomment peu (1,3 % d’usage récent en 2004-2005).
Dans le champ des opiacés hors MSO (BHD et méthadone), les sulfates de morphine restent les plus consommés : 15 % des usagers de drogues des Caarud en 2008. La prise des autres morphiniques majeurs tels que l’oxycodone n’a pas fait l’objet de données publiées. Les médicaments codéinés accessibles sans ordonnance ont vu leur consommation chuter avec la diffusion des traitements de substitution aux opiacés à partir de la seconde moitié des années 1990. En 2006, un peu moins de 5 % des usagers des Caarud signalaient l’usage d’un dérivé codéiné au cours du mois précédent.
D’autres molécules sont utilisées dans des groupes plus restreints ; c’est le cas du méthylphénidate (Ritaline®), dont l’usage détourné pourrait se développer au cours des prochaines années, d’un antiparkinsonien – le trihexyphénidyle (Artane®) – ou, plus rarement, de neuroleptiques tels que la cyamémazine (Tercian®). Les antidépresseurs ne font pas l’objet de détournement. La kétamine (un anesthésique) occupe une place en marge des substances précédentes, dans la mesure où elle est toujours obtenue illégalement
5
La majorité de la kétamine consommée en France est importée sous forme liquide ou sous forme de poudre en provenance d’Asie ou d’Europe de l’Est.
.
Prévalences d’usage au cours du dernier mois des substances médicamenteuses (hors MSO) les plus consommées par les usagers des Caarud, 2008 (source : ENa-Caarud 2008, OFDT)
|
|
Usages récents (mois précédent) (%)
|
Part des usagers quotidiens parmi les usagers récents (%)
|
|
Benzodiazépines
|
28
|
57
|
|
Sulfates de morphine
|
15
|
39
|
|
Kétamine
|
7
|
5
|
Le trihexyphénidyle (Artane®) est peu consommé en France métropolitaine, essentiellement dans les régions marseillaise et dans une moindre mesure parisienne, et par des usagers extrêmement désocialisés souvent porteurs de comorbidités psychiatriques. En revanche, sa consommation constitue une préoccupation importante à l’Île de La Réunion. Le méthylphénidate (Ritaline®) connaît également une diffusion cantonnée pour le moment en région Provence-Alpes-Côte d’Azur.
En 2009, parmi les usagers des Csapa (Centres de soins, d’accompagnement et de prévention en addictologie), 64 % de ceux ayant consommé de la morphine l’ont obtenue illégalement. Ils étaient 48 % pour le flunitrazépam (Rohypnol® ; hypnotique) et 34 % pour le clonazépam (Rivotril® ; anti-épileptique). Ces taux d’obtention illégale peuvent être plus élevés chez les usagers actifs des Caarud ; par exemple, 78 % des usagers consommant de la morphine l’ont obtenue totalement ou partiellement au marché parallèle en 2006.
En 2006, 39 % des usagers de benzodiazépines (hors flunitrazépam – Rohypnol® – quasiment toujours mésusé) fréquentant les Caarud et interrogés dans l’étude Prelud
6
Étude multisite se déroulant dans certains Caarud répartis sur 9 villes françaises. Usagers interrogés par des intervenants ou des enquêteurs expérimentés par rapport à leurs usages de drogues (N=1 017).
signalaient consommer ces médicaments uniquement dans un objectif « toxicomaniaque » (défonce, gestion du manque ou de l’usage d’un autre produit), 44 % visaient un effet « thérapeutique » (se soigner ou diminuer ses consommations) et 17 % mêlaient les deux objectifs. Les motivations à l’usage des produits codéinés connaissaient les mêmes proportions. Pour la morphine, en revanche, 84 % des consommateurs recherchaient un effet de « défonce ».
C’est dans les consommations à visée de « défonce » que se concentre majoritairement le mésusage de médicaments psychotropes. Ce dernier s’intensifie avec certaines conditions de l’usage de drogues (polyconsommation, injection, précarité...). Il s’accroît également avec la jeunesse des usagers et le genre masculin. Il est possible de repérer deux groupes d’usagers de médicaments psychotropes particulièrement mésuseurs : les usagers de drogues les plus désocialisés, le plus souvent des hommes de plus de 35 ans, dont les usages se centrent sur les médicaments psychotropes qui constituent les drogues les moins chères et qui fréquentent peu le système de soins ou de réduction des risques, et des jeunes particulièrement polyusagers âgés d’environ 25 ans, fréquemment en errance, et caractérisés par d’importantes prises de risques.
Près de 130 000 personnes ont bénéficié de traitements de substitution aux opiacés en 2007
Près de 130 000 personnes ont bénéficié de remboursements de traitements de substitution pour une dépendance aux opiacés en 2007, avec – spécificité française – une nette prédominance de la BHD représentant près de 80 % de l’ensemble, devant la méthadone
7
Deux médicaments de substitution aux opiacés sont autorisés en France : la méthadone, mise sur le marché en 1995, et la BHD disponible dès l’année suivante. Les sulfates de morphine (Moscontin®, Skénan®) sont exceptionnellement prescrits sous certaines conditions.
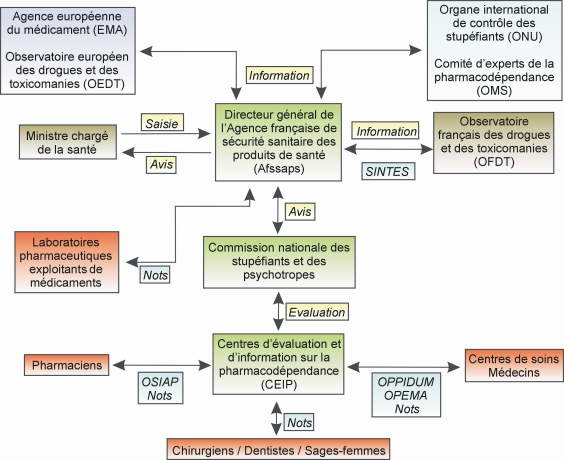
. Différentes sources de données permettent d’estimer le niveau d’usage de MSO en France. Les données de l’Assurance maladie permettent d’appréhender le niveau d’usage des MSO prescrits en ville ou en structures de soins et délivrés en officine de ville parmi les bénéficiaires affiliés au régime général de l’Assurance maladie. Des enquêtes reproductibles menées auprès des populations usagères de drogues vues au travers de centres de soins (enquête Oppidum : Observation des Produits Psychotropes Illicites ou Détournés de leur Utilisation Médicamenteuse ; CEIP, Centre d’évaluation et d’information sur la pharmacodépendance), en médecine de ville (enquête Opema : Observation des Pharmacodépendances En Médecine Ambulatoire ; CEIP), ou au travers de structures dites à « bas seuil d’exigence »
8
Les dispositifs dits à « bas seuil d’exigence » proposent de partir de la demande de l’usager de drogues et de s’y adapter. Ils proposent ainsi un accueil ouvert sans exigence explicitement formulée auprès des usagers de drogues.
(enquêtes ENa-Caarud et Prelud) permettent de compléter ces données.
Les différents types d’enquêtes ont pour point commun d’appréhender les niveaux d’usage de MSO ainsi que les modalités de traitement des populations concernées. Les niveaux d’utilisation des MSO sont le plus souvent évalués par le biais des doses quotidiennes moyennes
9
La dose quotidienne moyenne se calcule le plus souvent au travers des études en additionnant toutes les quantités prescrites par produit (BHD ou méthadone) de la première à l’avant dernière délivrance de l’année en les divisant par la durée de traitement (de la première à la dernière date de délivrance).
(DQM) reçues, alors que les types de traitement peuvent être approchés, suivant les cas, par la régularité des prescriptions ou par leur finalité (obtention dans le cadre d’un protocole thérapeutique de substitution ou non).
Ces enquêtes offrent également la possibilité de définir l’intentionnalité de recours aux MSO selon que les individus en font un usage thérapeutique (en protocole médical ou en « auto-substitution »
10
L’« auto-substitution » correspond à un usage thérapeutique hors protocole médical en vue également d’arrêter ou de diminuer toute consommation opiacée.
) ou non (à visée « toxicomaniaque » ou de « défonce »). L’analyse des données de remboursement de l’Assurance maladie permet quant à elle de différencier les types de traitements (« continu » ou « non régulier ») selon la durée effective de traitement sur l’année et les intervalles entre deux délivrances. Les mésusages éventuels des MSO, en particulier ceux relatifs à la BHD, peuvent par ailleurs être appréhendés de manière quantitative (part des individus bénéficiant d’une dose quotidienne moyenne supérieure à 32 mg/jour de BHD) mais aussi de manière qualitative via l’étude de l’intentionnalité de la consommation, de la voie d’administration (orale, intraveineuse, sniffée ou inhalée) et aussi du mode d’acquisition (prescription, polyprescription et/ou marché parallèle).
D’après les données recueillies auprès d’un échantillon représentatif de sujets ayant obtenu un remboursement de MSO en 2007 (enquête Cnamts/OFDT), les deux tiers des individus – ceci quel que soit le MSO dont ils ont bénéficié au cours de l’année – sont considérés comme étant en traitement régulier et donc inclus
a priori dans un processus thérapeutique. En 2007, 1,6 % des sujets ont reçu une DQM supérieure à 32 mg/jour de BDH alors qu’ils étaient 6 % en 2002, signifiant une réduction du mésusage. Le nomadisme médical et officinal
11
Consultations successives de 5 médecins ou plus et/ou 5 pharmacies ou plus alors même que le sujet ne subit pas de contraintes organisationnelles. Ces seuils laissent présager une forte présomption de détournement, surtout s’ils coexistent.
, autre indicateur de détournement, diminue également. Cette baisse du détournement de BHD – toujours préférentiellement localisé en Île-de-France, Provence-Alpes-Côte d’Azur et Alsace – est sous-tendue par l’instauration dès 2004 d’un plan de contrôle de l’Assurance maladie sur les consommations de MSO suspectes de mésusage.
Les études pharmaco-épidémiologiques nationales (Oppidum et Opema), menées annuellement auprès de patients recevant un MSO, respectivement dans des structures de soins et au sein de cabinets de médecine générale, montrent en 2008 que la grande majorité des sujets sont dans une démarche de soin (respectivement 92 et 99 %) avec très peu de mésusages (voie d’administration orale de la BHD dans respectivement 94 et 97 % des cas et acquisition du médicament par prescription dans la très grande majorité). À l’inverse, les sujets qui ne sont pas dans une démarche de soin (respectivement 8 et 1 %) ont recours majoritairement à des voies d’administration autres que la voie orale et à un approvisionnement illégal.
En revanche, les études menées auprès des sujets fréquentant les structures à « bas seuil d’exigence » – enquête Prelud en 2006 et enquête Ena-Caarud en 2008 – retrouvent des intentionnalités d’usage beaucoup moins marquées vers le soin (seule la moitié des sujets interrogés dans l’enquête Prelud disent recourir à la BHD uniquement à cette fin), avec un usage de BHD principalement par voie intraveineuse (respectivement 58 et 56 % des sujets inclus dans ces enquêtes).
Certaines de ces études apportent également des éléments d’information sur les co-consommations de médicaments psychotropes parmi les sujets bénéficiaires de MSO, sans préjuger de leur mésusage. L’analyse de la base de données de la Cnamts en 2007 montre en particulier qu’un peu moins de la moitié des patients ont reçu également au moins une molécule de la famille des benzodiazépines (anxiolytique et/ou hypnotique) au cours de l’année
12
Parmi une liste de molécules préétablie.
. Cette prévalence est plus élevée parmi les sujets bénéficiaires de la CMU quel que soit le MSO reçu (54 %) et particulièrement parmi les sujets bénéficiant d’une DQM>32 mg/jour de BHD (85 %).
En 2010, 9 % des personnes détenues ont bénéficié de médicaments de substitution aux opiacés
De nombreuses données françaises et internationales attestent des liens multiples entre l’usage de drogues illicites, la morbidité psychiatrique, le mésusage de médicaments psychotropes et l’incarcération. En prison, la présence d’usagers de drogues, de personnes présentant une pathologie psychiatrique mais aussi de trafiquants explique une part de la consommation de médicaments psychotropes. Au 1er janvier 2009, parmi les personnes détenues condamnées, 14 % étaient incarcérées au titre d’une ILS (infraction à la législation des stupéfiants) qui recouvre essentiellement des faits liés au trafic. En dix ans, le nombre de sujets incarcérés pour ce motif a augmenté de 165 %. La prévalence des personnes souffrant de pathologies psychiatriques en prison a été estimée à 70,5 % (2006). Selon les professionnels, il s’agit de la morbidité psychiatrique préexistante mais également de la souffrance psychique qui peut naître du processus judiciaire et de la détention.
Chez les sujets entrant en détention, l’enquête de la Drees (Direction de la recherche, des études, de l’évaluation et des statistiques) menée en 2003 indique qu’un tiers d’entre eux déclare une utilisation prolongée et régulière de drogues illicites dans les douze mois précédents et que 10 % sont polyusagers. Cinq pour cent des sujets déclarent une consommation de médicaments psychotropes de type « toxicomaniaque »
13
Le terme toxicomaniaque n’étant pas défini, on ignore ce qu’il intègre exactement. Les prises de médicaments psychotropes en gestion du manque ou de la chute d’effets de stimulants ne sont vraisemblablement pas incluses, conduisant peut-être à une sous-évaluation des consommations de médicaments détournés.
« prolongée et régulière » et près de 15 % sont en cours de traitement par médicaments psychotropes. En 2003, près de 8 % des entrants déclaraient avoir un traitement de substitution aux opiacés (8 fois sur 10, il s’agissait de BHD).
Prévalence (%) de consommations déclarées de médicaments psychotropes et de médicaments de substitution aux opiacés chez les entrants en détention en 2003 (d’après Drees, 2003)
|
Utilisation prolongée et régulière de drogues illicites au cours des 12 mois avant l’incarcération dont :
|
33
|
|
Médicaments utilisés dans un but toxicomaniaque
|
5
|
|
Traitement de substitution en cours par :
| |
|
Méthadone
|
1,5
|
|
BHD
|
6
|
|
Traitement en cours par médicaments psychotropes dont :
|
15
|
|
Neuroleptiques
|
5
|
|
Antidépresseurs
|
5
|
|
Anxiolytiques ou hypnotiques
|
12
|
Au cours de l’incarcération, la prévalence d’usage de médicaments psychotropes reste peu documentée en France, en lien avec la difficulté de s’adresser directement aux personnes détenues. Les études menées en Europe indiquent l’existence d’une consommation plus importante de médicaments psychotropes en milieu carcéral que dans la population générale. En France, une étude réalisée en 2000, dans la prison de Lyon, estime que 37 % des hommes incarcérés sont des usagers chroniques de benzodiazépines.
La consommation de médicaments psychotropes apparaît moindre dans les établissements les moins surpeuplés. On observe davantage de consommation de médicaments psychotropes parmi les prévenus que parmi les condamnés, et davantage d’usage dans les premiers mois d’incarcération. Enfin, l’accès aux soins favoriserait également la consommation de médicaments psychotropes, l’usage mesuré englobant usage approprié et mésusage.
En 2010, 9 % de l’ensemble des personnes détenues bénéficient d’un traitement de substitution aux opiacés. Les TSO sont de plus en plus facilement poursuivis après l’entrée en prison (dans 9 cas sur 10), voire initiés à l’entrée en détention. D’après l’enquête Prevacar (Prévalence du VIH, du VHC et des TSO en milieu carcéral) mise en place en juin 2010, un tiers des traitements sont initiés pendant l’incarcération (avec une part de la méthadone en légère hausse). Cependant, d’après l’inventaire Pri2de (Programme de recherche et intervention sur la prévention des risques infectieux en milieu pénitentiaire) réalisé en juin 2010, 19 % des établissements pénitentiaires déclaraient piler ou diluer la BHD afin de limiter son détournement ; de telles pratiques compromettant l’efficacité thérapeutique de la BHD.
On dispose de très peu de données quantitatives françaises sur les usages de substances illicites et des médicaments psychotropes détournés au cours de l’incarcération. Les benzodiazépines sont le plus souvent prises par voie orale, y compris chez les usagers de drogues. Pour la BHD, les modes de consommation évoluent avec l’accroissement de l’utilisation du snif et, dans une moindre mesure, de la voie fumée, mais l’injection persiste pour certains usagers.
Des travaux sociologiques montrent qu’une partie des usagers de drogues effectuent un transfert des usages de drogues illicites vers les médicaments psychotropes à l’entrée en détention. Certains cherchent à consommer n’importe quel produit disponible pour supporter l’incarcération, alors que d’autres visent à combler le manque. Les personnes détenues non usagères de drogues utilisent les médicaments psychotropes pour s’adapter aux conditions carcérales ou fuir la réalité. En outre, des initiations à l’utilisation détournée de médicaments tels que la BHD sont documentées chez des personnes détenues non usagères de drogues ainsi que l’existence de micro-trafics.
En population générale, différentes situations de pharmacodépendance aux médicaments psychotropes peuvent être évoquées
D’abord classée par la nosographie psychiatrique dans la rubrique des toxicomanies (DSM-III, 1980)
14
Diagnostic and Statistical of Mental disorders
, la dépendance aux médicaments psychotropes est redéfinie ensuite par cette même nosographie comme « une dépendance psychologique sans dépendance physiologique » (DSM-III-R, DSM-IV). Néanmoins, en 1990, l’
American Psychiatric Association reconnaît pour les benzodiazépines la manifestation d’une dépendance physiologique à l’arrêt du traitement. L’Association retient alors comme définition susceptible de s’appliquer à la population générale celle du « syndrome de retrait » : les sujets auxquels on retire le médicament sont, dans une très large proportion, incapables d’y renoncer et réitèrent leur consommation. L’état de malaise vécu à l’arrêt du traitement n’est pas un état de manque mais plutôt un faisceau de symptômes. Dans le prochain DSM-V, la distinction entre abus et dépendance devrait disparaître au profit d’une catégorie unique appelée « trouble lié à une substance ». De ce fait, on pourra parler de trouble lié à l’usage de psychotrope devant l’existence d’un seul critère : tolérance ou syndrome de sevrage à l’arrêt ou envie impérieuse de consommer à nouveau (
craving) quand le médicament n’est plus disponible ou survenues répétées de dommages que ce soit dans le domaine familial, professionnel ou social.
Néanmoins, la caractérisation et la prévalence de ce phénomène restent sujettes à débats. D’abord, l’idée selon laquelle le syndrome de retrait serait d’origine purement physiologique côtoie une explication cognitive, sans que ces deux hypothèses suffisent à rendre compte de la variance du phénomène dans la population ayant arrêté de consommer les produits. Ensuite, la part des anciens consommateurs ayant souffert du syndrome varie selon les études de 15 % à 50 %, et pourrait concerner 90 % d’entre eux. Le phénomène paraît donc extrêmement variable selon les substances et connaît une intensité elle-même variable selon les consommateurs et les motifs de consommation. En dépit de ces multiples imprécisions, il semble exister des formes de dépendance singulières et diverses mais une dépendance néanmoins.
Les facteurs sociaux de l’usage, susceptibles d’expliquer la distribution de la consommation dans la population, peuvent être ramenés à quelques processus principaux. La consommation des médicaments psychotropes est un phénomène extrêmement répandu dans la population générale. La prescription des médicaments psychotropes s’intègre le plus souvent dans une médecine somatique, des troubles digestifs et cardiovasculaires en particulier, car seulement 17 % des ordonnances ne comprennent que ces médicaments. Dans 30 % des cas, la durée de la consommation est inférieure à 6 mois, soit inférieure au seuil défini pour la prescription efficace des antidépresseurs. Pour les benzodiazépines, elle atteint, à l’inverse, des durées supérieures à 2 ans dans plus de 30 % des cas, et supérieures à 5 ans dans plus de 15 % des cas, soit une chronicité sans commune mesure avec les règles de prescription.
L’analyse des prescriptions semble indiquer qu’il existe des sujets qui, bien que ne présentant probablement pas de trouble psychiatrique caractérisé, reçoivent des traitements (principalement anxiolytiques) pour répondre à des plaintes somatiques mais également sociales, auxquelles on peut associer des durées de consommation, une proximité aux médicaments et donc des degrés de dépendance aux médicaments psychotropes assez différents.
Les sciences sociales ont peu analysé les consommations chroniques et, parmi elles, moins encore les consommations problématiques. En réalité, ou bien les analyses ont d’emblée conclu à l’effet addictif des substances à partir d’une simple reprise de l’argument physiologique, ou bien elles ont cherché au contraire à mettre en avant l’autonomie du patient, allant parfois jusqu’à suggérer une maîtrise parfaite de celui-ci sur le produit. Néanmoins, une typologie des recours en fonction de leur durée peut être esquissée.
Les recours conjoncturels (inférieurs à 6 mois) concernent essentiellement la population la plus jeune (moins de 45 ans). Ce type de recours serait épisodique parce qu’il est lié le plus souvent à des effets de situation susceptibles d’évoluer dans le temps (rupture, chômage, deuil...). Dans la mesure où le recours reste temporaire, l’usage est rarement vécu dans les termes d’une situation de dépendance.
Les recours de nécessité (plus d’une décennie de traitement) correspondent aux durées de prescription les plus longues, parfois supérieures à 20 ans. Ces prescriptions concernent la population la plus âgée et viseraient l’accompagnement des maladies somatiques invalidantes, la prise en charge de la douleur, du vieillissement et de l’isolement ou bien encore le traitement massif, mais lié à de multiples causes, de l’entité transnosographique qu’est l’insomnie. L’attachement aux médicaments, en particulier aux hypnotiques, est indéniable, et le sentiment de dépendance est très largement partagé. Toutefois, le traitement s’appuie sur une définition de la santé qui n’est pas celle de la psychiatrie mais qui bénéficie d’une légitimité tout aussi réelle. Cette définition commande de traiter la douleur ou la souffrance associée à la maladie chronique ou à l’isolement. C’est pourquoi, si la dépendance est réelle, elle est rarement vécue comme un problème.
Les recours problématiques aux médicaments (au moins 5 ans d’usage) s’observent dans une population, âgée de 45 à 55 ans, qui est la plus proche du cœur de cible de la clientèle psychiatrique. Traités pour anxiété ou dépression par les généralistes, ces patients ont des difficultés à situer l’origine de leur trouble : selon eux, il est « en soi » et se manifeste par une forte auto-dévalorisation. Le médecin généraliste, ne reconnaissant pas ces patients dans les grands cadres diagnostiques de la psychiatrie, a tendance à tenter de les soulager de façon symptomatique. De ce contexte, se déduit une consommation chronique et souvent compulsive du produit. Le patient vit sa consommation à la fois comme une nécessité et comme un déni de lui-même. La dépendance est patente, et vécue comme néfaste et problématique.
Ainsi, les consommations chroniques s’inscrivent souvent hors du cadre des préconisations énoncées par la psychiatrie, mais elles s’entourent néanmoins d’une légitimité sanitaire, soudée, entre autres, au traitement de la douleur et de la souffrance. Ce constat est confirmé d’une certaine manière par la difficulté que présente l’évaluation du rapport bénéfice/risque. Les risques liés aux consommations chroniques sont bien réels, notamment chez la personne âgée (perte de vigilance, de mémoire, confusion, aggravation des symptômes de démence...) mais leurs bénéfices sont tout aussi patents pour les patients et les prescripteurs (accompagnement des maladies chroniques, traitement de l’insomnie, de la douleur et du mal-être en général, évitement du recours à d’autres psychotropes dont l’alcool...).
Chez les usagers de drogues, la dépendance s’accompagne le plus souvent de mésusages de médicaments psychotropes
La population des usagers de drogues apparaît à haute prévalence d’usage de substances psychotropes. Il s’agit soit de personnes consommatrices de substances illicites ou détournées
15
Issues du trafic ou correspondant à un mésusage.
, approchées du fait de leur fréquentation de lieux institutionnels spécifiques à caractère sanitaire, social ou judiciaire, soit de personnes appréhendées dans un espace plus ou moins ciblé et homogène (espace festif, « rue »...) au travers d’enquêtes de type socio-ethnographique. Ces enquêtes ne prétendent pas représenter l’exhaustivité de la population des usagers de drogues, mais des segments de celle-ci, limitant ainsi les conclusions possibles. Il serait illusoire d’envisager cette population de façon homogène ; elle recouvre en effet des sous-groupes socioculturels et des trajectoires individuelles d’usages disparates.
Les phénomènes de mésusages et de pharmacodépendances aux médicaments psychotropes sous formes d’usage non conforme, d’usage problématique, de modification des modes d’administration ou d’obtention, d’addiction ou de toxicomanie y sont observables dans des proportions variables selon les médicaments concernés, les contextes sociodémographiques et d’usage.
En France, la notion de mésusage est souvent associée à l’usage détourné ou au détournement d’usage. En fait, le mésusage est une notion englobante qui fonctionne avec « et » et « ou » ; elle s’appréhende dans trois dimensions distinctes.
Les finalités d’usage d’un médicament psychotrope en dehors du champ médical sont multiples et recoupent des contextes et des moments différents dans l’histoire de la personne. De plus, les usagers sont souvent engagés dans des polyconsommations où chaque molécule peut être consommée dans un objectif particulier.
En matière de médicaments psychotropes, en dehors des traitements de substitution aux opiacés, les usages problématiques concernent essentiellement les somnifères et les tranquillisants.
Le mésusage des anesthésiques comme la kétamine ou le GHB (gamma-hydroxybutyrate) concerne des sous-groupes de populations essentiellement en contexte festif ou très marginalisés dans des usages récréationnels. Ces contextes peuvent induire parfois du trafic, des abus d’usage et des usages problématiques, mais peu de pharmacodépendances.
Les antidépresseurs, les antipsychotiques et les antiparkinsoniens ne font pas l’objet de phénomènes de pharmacodépendance significatifs chez les usagers de drogues. En revanche, des cas de consommation massive à visée d’ivresse sont parfois constatés.
Récemment, une augmentation des phénomènes de mésusages (ou de pharmacodépendance) de stimulants (méthylphénidate, modafinil) a été observée dans certains sous-groupes de populations.
Les usagers de drogues ont un rapport différent avec les traitements de substitution aux opiacés, selon qu’ils demandent une prise en charge médicale, visent une gestion du manque ou recherchent des effets psychotropes marqués. Les profils sociodémographiques, psychopathologiques, les trajectoires d’usage, les attentes spécifiques à l’égard des traitements, conduisent à une diversité des besoins ressentis et des attentes des usagers en matière de MSO.
Il convient de distinguer l’approvisionnement de la BHD hors prescription qui inscrit le mésusage dans une dimension collective, des autres formes d’usages détournés (modes d’administration, doses, fréquences...) qui concernent en premier lieu une dimension personnelle de l’usage. Le trafic contribue également à détériorer la représentation d’un médicament utile, au profit d’une image de « mauvaise drogue ».
Pour des raisons qui sont à la fois pharmacologiques, psychiques et sociales, le rapport qu’un usager pharmacodépendant va développer dans le temps avec les opiacés est évolutif. L’introduction de MSO dans cette dynamique est un paramètre qui va en influencer l’évolution. Ces constats cliniques ont conduit à envisager les stratégies de prises en charge en distinguant des seuils d’exigence qui correspondent à des intentionnalités thérapeutiques différentes : le soin et la réduction des risques. Ces objectifs pluriels ont été à l’origine de pratiques médicales diverses et qui s’opposent parfois.
Si une partie des usagers recherche une prise en charge médicale, une autre est encore en quête de produits. Ainsi pour certains, y compris un sous-groupe engagé dans des usages qui ne sont pas toujours conformes, les MSO sont des ressources pour sortir de la toxicomanie, alors que pour d’autres, ils sont utiles pour mieux gérer une vie dans laquelle l’usage de drogue est une composante.
En population générale, la prévalence de la pharmacodépendance, estimée entre 1 et 2 % d’après les études américaines, reste inconnue en France
Il existe peu d’études traitant spécifiquement du mésusage et de la dépendance en France et en Europe. Davantage d’éléments peuvent être extraits des études américaines qui se sont intéressées aux sédatifs, aux stimulants et aux opiacés (en raison de l’importance de la dépendance aux antalgiques opiacés aux États-Unis).
Dans l’étude épidémiologique Nesarc (National Epidemiologic Survey on Alcohol and Related Conditions) portant sur 40 000 sujets représentatifs de la population américaine, la prévalence vie entière de l’usage non médical, de l’abus ou de la dépendance (critères DSM-IV) à plusieurs types de médicaments psychotropes a été décrite. Les taux de prévalence de l’usage non médical de sédatifs, tranquillisants, antalgiques opiacés et amphétamines se situent entre 3 et 5 %, ceux de l’abus ou de la dépendance entre 1 et 2 %. Les facteurs de risque identifiés pour l’abus/la dépendance étaient le sexe masculin, l’appartenance au groupe Native Americans, le fait d’être jeune et séparé/divorcé. Les abus/dépendances à chacun de ces médicaments étaient corrélés entre eux et avec l’usage de drogues illicites. Les troubles psychiatriques étaient également un facteur de risque ; le trouble bipolaire, le trouble panique et le trouble de personnalité antisociale étaient les plus fortement corrélés à l’abus/dépendance aux médicaments psychotropes.
Prévalence de l’usage non médical vie entière et prévalence de l’abus/dépendance vie entière aux médicaments psychotropes aux États-Unis (d’après l’étude Nesarc 2001-2002)
| |
Prévalence vie entière de l’usage non médical (%)
|
Prévalence abus/dépendance(%)
|
|
Sédatifs
|
4
|
1
|
|
Tranquillisants
|
3
|
1
|
|
Antalgiques opiacés
|
5
|
1
|
|
Amphétamines
|
5
|
2
|
Une étude plus précise de la même population s’est focalisée sur l’usage non médical dans l’année écoulée des antalgiques opiacés. La prévalence retrouvée était de 1,8 %. Parmi ces sujets, 53 % avaient utilisé ces traitements pendant moins d’un mois, mais 20 % réunissaient les critères d’abus ou de dépendance et 13 % avaient présenté un usage quotidien sur l’année. Les facteurs associés à la dépendance aux antalgiques non prescrits étaient l’existence de douleurs, de troubles psychiatriques, d’abus et de dépendance à l’alcool et l’usage de drogues illicites (odds ratio entre 1,5 et 3). Les troubles psychiatriques préexistants apparaissent comme un facteur de risque d’apparition ultérieure d’usage non médical d’antalgiques opiacés et, inversement, l’usage non médical de ces traitements est un risque de survenue ultérieure de troubles psychiatriques (odds ratio entre 2 et 4). Il en est de même pour la relation temporelle entre dépendance aux antalgiques opiacés résultant de l’usage non médical et troubles psychiatriques (multiplication du risque entre 5 et 10). Les auteurs en concluent que ces troubles partagent des facteurs de vulnérabilité communs.
Dans l’étude américaine NSDUH (National Survey on Drug Use and Health) portant sur près de 92 000 sujets (âgés de 18 ans et plus) représentatifs de la population générale, l’usage non médical de médicaments opiacés dans l’année écoulée était retrouvé avec une prévalence de 4,5 %, parmi lesquels 12,5 % des sujets présentaient les critères d’abus ou de dépendance (soit environ 0,5 % de la population générale). Le premier médicament cité par les sujets était l’hydrocodone (68 %). Les facteurs associés à l’usage non médical étaient des troubles psychiatriques : le trouble panique, la dépression majeure et les symptômes phobiques. Les autres facteurs associés identifiés étaient un moins bon état de santé, un antécédent d’abus à un autre traitement prescrit, un usage passé d’héroïne et un âge précoce d’initiation aux substances (inférieur à 13 ans).
Dans certains sous-groupes de la population générale (sujets âgés, femmes, adolescents ou étudiants), les prévalences de mésusage ou de dépendance médicamenteuse peuvent atteindre 9 %. Au Canada, dans un échantillon d’environ 3 000 personnes de plus de 65 ans interrogées à leur domicile, la prévalence sur les 12 derniers mois de l’usage de benzodiazépines (selon prescription) était de 25 %. La prévalence de la dépendance chez ces patients était de 9 %. Les facteurs associés à la dépendance étaient le sexe féminin, les troubles cognitifs et les difficultés à trouver de l’aide pour des problèmes émotionnels ou psychologiques (odds ratio de 2 à 3).
Sur 3 000 adolescents de 12-17 ans représentatifs de la population générale américaine, une étude a rapporté une prévalence du mésusage de médicaments au cours de l’année de 6,7 %. Les facteurs associés à ce mésusage étaient des antécédents de conduites délictueuses, des usages d’autres substances, avoir été témoin de violence et présenter un PTSD (Post-Traumatic Stress Disorder) (avec des odds ratio autour de 2 sauf pour l’usage d’autres substances pour lequel l’odds ratio est de 8).
De même, des études réalisées en Australie et au Japon mettent en relation la présence de troubles affectifs de type dépression majeure et trouble bipolaire ainsi que des troubles anxieux et la survenue ultérieure d’abus et de dépendance aux drogues en général, y compris les sédatifs, psychostimulants et opiacés.
En population générale, une association entre diagnostic de mésusage de médicaments prescrits (tranquillisants, stimulants, antalgiques) et diagnostic vie entière d’abus et de dépendance à l’alcool est fréquemment retrouvée. Le sens de l’association serait bidirectionnel, soulignant la vulnérabilité des patients alcoolodépendants à développer une dépendance médicamenteuse et inversement.
En population clinique, la prévalence de la pharmacodépendance peut atteindre 50 % d’après les études internationales
Il n’existe pas d’étude en France sur la prévalence du mésusage et de la dépendance aux traitements psychotropes dans des échantillons sélectionnés de patients traités pour des troubles psychiatriques, et sur les facteurs de risque associés.
Dans des études internationales, la prévalence de l’abus ou de la dépendance (selon les critères DSM-IV) à des médicaments psychotropes a pu être évaluée à des taux atteignant 50 % dans certains troubles si l’on prend en compte l’ensemble des classes de médicaments pouvant faire l’objet d’abus. Il s’agit fréquemment de sédatifs-anxiolytiques, et moins souvent de stimulants et d’antalgiques opiacés. Certaines études montrent que la prévalence d’abus ou de dépendance aux médicaments psychotropes est statistiquement plus élevée en cas de trouble addictif associé au trouble psychiatrique (schizophrénie 63 %, trouble bipolaire 75 %, dépression majeure 66 %, autre diagnostic 48 %). De même, les patients réunissant les critères de trouble de la personnalité de type « border-line » (émotionnellement labile) sont plus à risque que les autres de présenter un abus de médicaments.
Parmi les patients souffrant de TDAH (trouble du déficit de l’attention avec hyperactivité), les plus à risque d’usage de drogues licites et illicites sont ceux qui présentent une comorbidité avec un trouble de personnalité antisociale, un trouble bipolaire, un trouble des conduites alimentaires, des symptômes plus sévères, et un abandon de l’école. De plus, une mise en place tardive du traitement (durant l’adolescence ou l’âge adulte plutôt que dans l’enfance) apparaît également comme un facteur de risque identifié d’abus des traitements amphétaminiques prescrits dans cette indication.
Outre le mésusage d’anxiolytiques-sédatifs, psychostimulants et antalgiques opiacés, le mésusage de quelques autres classes de médicaments psychotropes a été recherché chez des patients traités pour des affections psychiatriques. C’est notamment le cas des atropiniques, habituellement prescrits pour leur effet correcteur des symptômes neurologiques extrapyramidaux (akinésie, rigidité, tremblements) qui sont un effet secondaire bien connu des traitements neuroleptiques. Ils font l’objet d’un abus du fait de leurs propriétés hallucinogènes quand ils sont pris à forte dose. Cet abus peut être observé chez des sujets toxicomanes qui n’ont pas d’indication médicale à recevoir ce traitement.
Chez les patients suivis en soins généraux, l’association entre abus de médicaments psychotropes et troubles ou symptômes psychiatriques est constamment retrouvée. Là encore, l’association entre abus de médicaments psychotropes et sévérité des troubles est la règle. Les mésusages et la dépendance sont le plus souvent identifiés pour les anxiolytiques, les opiacés et les stimulants.
Une étude française a concerné des patients suivis en médecine générale et recevant des prescriptions de benzodiazépines en continu depuis plus de 6 mois et parmi lesquels 80 % présentaient des affections psychiatriques (troubles dépressifs, troubles anxieux) avec des niveaux de handicap importants (retentissement sur la vie sociale et le fonctionnement général noté 5 sur une échelle de 7). La dépendance aux benzodiazépines concernait 50 % des patients.
Quelques études (américaines ou européennes) indiquent que les patients recevant des opiacés pour des douleurs chroniques et chez lesquels on dépiste une tendance à l’abus du traitement, présentaient en majorité une comorbidité psychiatrique.
Les patients toxicomanes
16
La terminologie de « toxicomane » est aujourd’hui remplacée par celle d’« usager problématique de drogues ». La définition opérationnelle retenue par l’Observatoire européen des drogues et des toxicomanies (OEDT) pour « usager problématique de drogues » (UPD ; en anglais, PDU pour Problematic Drug User) est la suivante : usager de drogues par voie intraveineuse ou usager régulier d’opiacés, cocaïne ou amphétamines durant l’année passée pour le groupe d’âges de 15-64 ans.
présentent fréquemment un mésusage ou une dépendance aux traitements psychotropes prescrits. Selon les études, le taux de prévalence varie de 30 à 50 %. Dans cette population à haut risque, l’association avec la sévérité soit de la toxicomanie, soit des troubles psychiatriques est constamment retrouvée. Le sens de l’association peut être bidirectionnel : les troubles psychiatriques favorisant la dépendance aux traitements psychotropes ou la prise chronique de ces médicaments étant à l’origine d’une apparition ou d’une aggravation de ces symptômes. Un grand nombre d’études européennes et américaines s’est intéressé plus particulièrement à la dépendance aux benzodiazépines dans la population de toxicomanes. Dans plusieurs études, cette dépendance a été identifiée comme un facteur de mauvais pronostic dans le suivi des traitements de substitution aux opiacés. En effet, à fortes doses, les benzodiazépines entraînent des effets appétitifs chez les patients traités par méthadone ou BHD. Dans une étude écossaise portant sur des femmes toxicomanes, la prévalence de la dépendance aux benzodiazépines était de 50 %. Les facteurs associés étaient la polytoxicomanie, des antécédents d’usage de drogue par voie intraveineuse, de comportements auto-agressifs et de tentatives de suicide et la présence de symptômes psychiatriques. Dans une autre étude, 25 % des patients toxicomanes recevant un traitement par benzodiazépines présentaient un diagnostic vie entière de dépendance à ce traitement et 22 % présentaient une dépendance actuelle associée aux critères de trouble anxieux ou dépressif vie entière (
odds ratio compris entre 2 et 4).
Les études mettant en évidence chez des sujets toxicomanes une association entre troubles psychiatriques et abus de médicaments psychotropes autres que les benzodiazépines sont moins fréquentes. Dans le groupe de patients toxicomanes (présentant un abus ou une dépendance aux opiacés) issus de l’étude Nesarc, les prévalences d’abus et de dépendance ont été mesurées pour les sédatifs et tranquillisants (abus 33 %, dépendance 10 %), ainsi que pour les amphétamines (abus 33 %, dépendance 15 %).
Contrairement aux patients toxicomanes, les patients suivis pour une dépendance à l’alcool ont fait l’objet de très peu d’études en matière d’abus et de dépendance à des traitements psychotropes. Pourtant, ils présentent de nombreux facteurs de risque (notamment biologiques) : une tolérance croisée entre alcool et benzodiazépines, une comorbidité fréquente de troubles addictifs et une fréquence élevée de troubles psychiatriques. Aucune étude sur la dépendance aux sédatifs, aux psychostimulants, aux antalgiques opiacés ou à d’autres médicaments psychotropes dans des populations cliniques de patients alcoolodépendants en France n’a été identifiée. On peut supposer que les patients dépendants aux médicaments psychotropes sont aussi ceux qui présentent les symptômes les plus sévères au plan alcoolodépendance et psychiatrique.
Les modalités de traitement de la dépendance aux médicaments psychotropes se fondent sur les mêmes principes que tout traitement de la dépendance
Une fois la dépendance à un médicament psychotrope installée, son traitement devient un objectif thérapeutique en soi. Plusieurs études ont décrit des stratégies de sevrage pour des dépendances aux benzodiazépines et aux opiacés prescrits. Les principes des traitements proposés sont alors le plus souvent les mêmes que pour des dépendances aux opiacés illicites. Par analogie, ce type de stratégies de traitement de la dépendance médicamenteuse s’inspire des stratégies de décroissance progressive. En cas d’échec, les traitements de maintenance ou de substitution sont toujours proposés en derniers recours.
En revanche, ce schéma de substitution-décroissance ne s’applique pas à la dépendance aux psychostimulants. Par analogie aux études sur les traitements pharmacologiques dans la dépendance aux psychostimulants illicites (cocaïne et méthamphétamines), il n’y a pas de bénéfice démontré d’une approche substitutive utilisant des amphétamines à demi-vie longue. Il n’y a d’ailleurs pas d’études sur lesquelles se fonder pour recommander cet usage chez des patients dépendants à des traitements psychostimulants prescrits.
Les principes de prise en charge de la dépendance aux sédatifs et aux opiacés prescrits en population générale sont consensuels dans les différentes études. Ils se fondent sur quelques idées fortes :
• le changement de classe médicamenteuse quand il est possible ;
• une diminution progressive des doses en cas d’échec d’un sevrage brutal ;
• l’adjonction d’une autre classe (antidépresseur, antiépileptiques) pour traiter les manifestations dépressives ou anxieuses qui peuvent constituer des facteurs de maintien de la dépendance ;
• le traitement de maintenance (ou de substitution) en cas d’échec des stratégies de sevrage progressif ;
• l’adjonction d’un traitement psychothérapique ou d’accompagnement psychosocial est la règle, notamment dans les cas de rechute.
Même si elles sont peu nombreuses dans des populations spécifiques, les études existantes chez les patients toxicomanes proposent les mêmes principes généraux de réduction des benzodiazépines. Le pronostic de ces stratégies de sevrage est toutefois défavorable dans cette population, avec des taux de succès très limités. Ainsi, il a été rapporté dans une étude réalisée en Angleterre, plus de 75 % d’abandon dans des programmes de réduction de dose de 10 % par mois de diazépam chez des polytoxicomanes. Le pronostic n’est pas meilleur dans les populations de patients dépendants aux benzodiazépines non toxicomanes. Bien que les résultats de ces stratégies de sevrage soient décevants, il est à noter que ce sont celles recommandées par les autorités de santé dans la prise en charge des dépendances aux benzodiazépines. Les stratégies de substitution au long cours restent une alternative de dernier recours, par défaut.
Mésusages et pharmacodépendance semblent associés à un risque plus élevé de suicide, même si peu d’études ont caractérisé ce lien
Les études s’intéressant à la relation entre mésusage de médicaments psychotropes et suicide sont peu nombreuses. La plupart traite des substances psychoactives dans leur ensemble, sans distinguer les médicaments des substances illicites. De plus, rares sont les études qui permettent de différencier usage, mésusage, abus, dépendance et intoxication volontaire dans un but suicidaire. Il existe quelques données concernant le risque de mésusage de médicaments psychotropes chez les sujets qui présentent des conduites suicidaires ou le risque de conduites suicidaires chez les usagers de médicaments psychotropes.
Parmi les études menées chez les usagers de médicaments psychotropes, deux études, l’une suédoise, l’autre allemande, montrent que la dépendance (ou le mésusage) aux médicaments psychotropes multiplie par un facteur supérieur à deux le risque de mort par suicide. Ce risque est encore plus élevé pour ceux qui présentent un trouble lié à l’usage d’alcool et il est multiplié par 10 pour les sujets qui font également usage de substances illicites. Cette surmortalité est plus prononcée dans les cas de dépendance que d’abus. En population clinique psychiatrique, les sujets dépendants aux médicaments psychotropes présentent un risque accru de mortalité et de suicide, avec la perte de près de neuf ans de vie. Plusieurs études ont montré, chez des patients traités pour un trouble lié à l’usage de substances psychoactives, que l’utilisation de médicaments sédatifs ou de benzodiazépines est associée à un plus grand risque de tentative de suicide. Dans l’étude française « Subazur » (2008) qui a inclus des patients traités par buprénorphine haut dosage, une plus grande fréquence d’idéations ou de conduites suicidaires était observée chez les patients utilisant cette molécule par voie intraveineuse (mésusage). De telles données viennent corroborer le lien entre mésusage de médicaments et suicide. Bien qu’il existe très peu d’études évaluant le risque de conduites suicidaires dans le mésusage de médicaments psychotropes, celles disponibles identifient cependant une augmentation importante de ce risque.
La plupart des études menées chez les victimes de suicide sont anglo-saxonnes. Aucune n’a eu un accès direct au mode d’usage des médicaments psychotropes impliqués dans les décès. Les données qui s’appuient sur les études dont la méthodologie permettait d’estimer la prévalence des abus et dépendances aux médicaments psychotropes chez les patients ayant fait une tentative de suicide et les victimes de suicide montrent l’existence d’une association forte entre mésusage de médicaments psychotropes et actes suicidaires. Les études réalisées post mortem suggèrent une association entre mésusage de médicaments psychotropes et mortalité par surdose, mais celle-ci semble plus souvent accidentelle qu’intentionnelle.
Ainsi, il semble exister une association entre mésusage de médicaments psychotropes et conduites suicidaires. Peu d’études ont été consacrées à ce sujet et leur méthodologie variable ne permet pas de caractériser cette association. Les différentes substances sont souvent confondues en un unique groupe et l’usage est rarement distingué du mésusage, lui-même exceptionnellement défini.
Mésusages et pharmacodépendance sont associés à des complications somatiques
À l’exception des décès, il n’existe pas de données de prévalence ou d’incidence concernant les complications somatiques liées à l’usage, au mésusage et à la pharmacodépendance aux médicaments psychotropes, ce qui limite les possibilités d’évaluation de leur gravité en termes de santé publique. Les services d’urgences et les services de réanimation sont, parmi d’autres, des acteurs clés dans l’évaluation épidémiologique des complications liées aux médicaments, mais une telle veille sanitaire ne fait pas partie actuellement de leurs missions en France.
Le mésusage des médicaments psychotropes expose à des dangers liés aux voies et modes d’administration, aux complications non spécifiques, communes aux situations de surdose par ces substances et à des complications spécifiques liées à certaines molécules par une toxicité d’organe surajoutée à l’effet psychotrope en surdose. Cette toxicité d’organe peut être le fait du principe actif psychotrope ou d’autres principes actifs normalement associés dans les spécialités délivrées.
Le consommateur est exposé à tous les effets adverses sur les différents organes, induits par ces substances aux doses pharmacologiques recommandées ou en situation de mésusage. Des interactions pharmacologiques potentiellement délétères et graves peuvent apparaître sur le plan clinique. L’existence de telles interactions devrait être recherchée lorsque le mésusage est établi, et portée à la connaissance des consommateurs lorsqu’elles sont reconnues.
Selon une étude s’appuyant sur les bases de données des services de réanimation en Île-de-France, couvrant une période de 12 ans, le nombre annuel d’admissions pour intoxications médicamenteuses a connu une baisse légère mais significative passant d’environ 1 300 en 1997 à 1 200 en 2008. Les classes pharmacologiques les plus concernées (parmi les médicaments T46 à T50 selon la CIM-10) sont les antiépileptiques, les sédatifs, les hypnotiques, les antiparkinsoniens, les psychotropes non classés et les médicaments agissant sur le système cardiovasculaire. Cette légère diminution ne concerne pas une classe particulière.
Au cours des douze années d’observation, parmi les admissions pour intoxications médicamenteuses, la proportion d’hommes est restée stable, autour de 40 %, avec un âge moyen qui est passé de 41±16 à 47±17 ans. La proportion de patients de moins de 25 ans est passée de 14 à 10 % tandis que le pourcentage des intoxications médicamenteuses chez les personnes âgées de 80 ans et plus est passé de 2,5 à 5 %. La gravité de l’état des patients intoxiqués par des médicaments et admis en réanimation a augmenté de façon significative tout comme la durée de séjour en réanimation (sans modification de la durée du séjour hospitalier). La mortalité en réanimation et la mortalité hospitalière ont plus que doublé sur cette période de 12 ans, passant respectivement de 2 à 6 % et de 3 à 7 %.
Le mésusage de médicaments psychotropes expose également à des dangers liés à une toxicité cumulative.
Que ce soit en toxicité aiguë ou en toxicité cumulative, il existe des facteurs individuels de variabilité de réponse et de vulnérabilité, d’origine génétique et environnementale. Mal connus, ces facteurs sont des éléments confondants dans l’établissement de relations dose-durée d’exposition pour la survenue des complications somatiques liées au mésusage des médicaments psychotropes.
L’analyse toxicologique est une aide indispensable à la précision des causes et mécanismes de toxicité d’organe et de décès. Elle est couramment pratiquée et de façon performante dans le domaine médico-légal ; en toxicologie clinique, elle reste encore balbutiante avec des résultats ne permettant que très rarement de conclure avec certitude. Il faut souligner l’intérêt de l’analyse toxicologique dans la prise en charge en réanimation des intoxications graves par médicaments psychotropes et substances illicites chez l’adulte.
Les conséquences cliniques à long terme d’une exposition précoce aux médicaments psychotropes sont peu étudiées
La prévalence de l’exposition précoce aux médicaments psychotropes est peu étudiée en France, notamment au cours de la grossesse. Dans l’étude française Efemeris (Evaluation chez la Femme Enceinte des MEdicaments et de leurs RISques) sur les médicaments délivrés pendant la grossesse, 6 % des femmes enceintes en Haute-Garonne avaient reçu des médicaments psychotropes entre juillet 2004 et juin 2005, dont 3 % des benzodiazépines et 1 % d’autres anxiolytiques. Les produits les plus prescrits étaient à demi-vie longue (bromazépam, diazépam, prazépam), avec un risque associé accru d’hypotonie et de syndrome de sevrage néonatal. Globalement, le taux d’exposition fœtale aux médicaments psychotropes était supérieur à celui rapporté dans d’autres pays européens (Finlande, Italie, Allemagne, Royaume-Uni, Norvège).
Peu d’études de cohorte ont été menées sur les conséquences de l’exposition in utero aux médicaments psychotropes. Un syndrome de sevrage néonatal est rapporté après une exposition pendant la grossesse aux opiacés, aux benzodiazépines et aux barbituriques dans les jours qui suivent la naissance, avec des symptômes neurologiques, végétatifs et digestifs. Ce syndrome perturbe la relation mère-enfant. Dans une étude prospective aux États-Unis menée dans deux centres de soins prénatals depuis 1996, l’usage de benzodiazépines était associé à un risque accru de naissance prématurée, un petit poids à la naissance, un score d’Apgar inférieur à sept, une détresse respiratoire chez le nouveau-né et la nécessité de pratiquer des actes de réanimation néonatale. L’exposition fœtale aux amphétamines semble entraîner certaines complications périnatales telles qu’un faible poids de naissance ou la prématurité. Elle n’augmenterait pas le risque de malformation. Comparée à l’usage d’héroïne qui entraîne une diminution du poids de naissance et un risque de prématurité, la prise de traitement de substitution aux opiacés se montre moins délétère, ces traitements diminuant le retard de croissance intra-utérin et le risque de prématurité. Les traitements de substitution aux opiacés ne semblent pas être à l’origine de malformations congénitales.
Au total, malgré le manque de données et leur divergence, il semble que les médicaments psychotropes puissent entraîner certaines complications néonatales comme le retard de croissance ou la prématurité. Ces études sont cependant soumises à de nombreux biais parmi lesquels le biais d’indication, c’est-à-dire que le trouble ou la pathologie à l’origine de la prescription des médicaments psychotropes peut elle-même augmenter ces risques.
Peu de données sont disponibles sur les conséquences à long terme de l’exposition fœtale aux psychotropes sur la croissance et le neurodéveloppement. Quelques études menées sur les trois premières années de l’enfant n’ont pas montré d’impact significatif de l’exposition fœtale aux benzodiazépines. L’exposition fœtale aux opiacés entraîne un retentissement sur le comportement de l’enfant. Cependant, les enfants qui ont été exposés à la méthadone in utero et qui présentaient un retard moteur à l’âge de quatre mois ne le conservaient dans les années suivantes que s’ils se trouvaient dans une famille « à haut risque » de carences.
Chez les enfants et les adolescents, la prescription de médicaments psychotropes reste peu fréquente en France, de l’ordre de 2 %, (0,15 % pour le méthylphénidate et 0,3 % pour les benzodiazépines). Les risques liés aux médicaments psychotropes prescrits chez des enfants sont faibles. Entre 1995 et 2001, 14 notifications d’effets indésirables potentiellement imputables au méthylphénidate ont été faites auprès de la Pharmacovigilance française. Ces symptômes étaient le plus souvent améliorés par une adaptation thérapeutique de dose ou de forme galénique. Cependant, les enfants en âge préscolaire pourraient présenter davantage d’effets indésirables suite aux traitements, tels que la lenteur, l’apathie ou la survenue de mouvements répétitifs. Certains anxiolytiques sont commercialisés en population pédiatrique, même si leur usage est peu documenté. Leurs effets indésirables rapportés dans cette population sont une sédation, une altération des performances cognitives et des réactions paradoxales associant désinhibition et agressivité.
De nombreuses études se sont intéressées au risque de développer une dépendance ultérieure chez les enfants et les adolescents traités par des psychostimulants pour un trouble du déficit de l’attention avec hyperactivité (TDAH). Dans toutes ces études, sauf une, il n’existe pas d’augmentation du risque de dépendance ultérieure aux substances psychoactives, que ce soit le tabac, l’alcool, les stimulants ou autres substances. L’âge et la durée d’exposition ne semblent pas influencer ce risque. La seule étude ayant rapporté une augmentation du risque souffrait de nombreux biais méthodologiques et, en particulier, n’avait pas pris en compte l’impact du trouble et de ses comorbidités. La plupart de ces études sont observationnelles et pourraient souffrir d’un biais d’indication. Un essai clinique a cependant comparé le méthylphénidate au placebo donné sur des périodes de 12 à 18 semaines, chez des enfants âgés de 7 à 12 ans, présentant uniquement un trouble de l’apprentissage de la lecture. À un âge moyen de 26 ans, ces sujets n’étaient pas différents en ce qui concerne l’usage ou les troubles liés à l’usage de substances psychoactives. Ainsi, les psychostimulants ne semblent pas accentuer le risque de dépendance ultérieure aux substances psychoactives lorsque les règles de prescription sont respectées.
Chez l’animal, une exposition précoce à certains médicaments pourrait engendrer des modifications neurochimiques ayant des répercussions à l’âge adulte
Parmi les études précliniques menées chez les rongeurs, on peut distinguer celles qui considèrent les effets neurobiologiques et comportementaux de traitements médicamenteux reçus au cours de la vie fœtale et jusqu’au sevrage, et celles qui étudient l’impact des traitements effectués pendant la période assimilée à l’adolescence (chez le rongeur, entre 4 et 6 semaines d’âge postnatal).
Selon les molécules psychotropes utilisées, un traitement pendant la gestation produit des effets variables chez l’animal à l’âge adulte. La métamphétamine administrée pendant la gestation altère le développement postnatal de la descendance et induit des effets persistants chez le rat adulte, aussi bien au niveau comportemental qu’au niveau de la neurotransmission dopaminergique (la dopamine étant un neurotransmetteur impliqué dans le circuit de la récompense). La morphine et les opiacés affectent la plasticité synaptique hippocampique, avec altération de la mémoire spatiale, et diminuent la neurotransmission GABAergique (le GABA étant le principal neurotransmetteur inhibiteur). Quant à l’exposition à la méthadone pendant la gestation, elle induit à l’âge adulte des effets comportementaux comme l’augmentation de l’activité locomotrice et l’auto-administration de substances psychoactives (morphine).
Le diazépam (benzodiazépine de référence dans les études expérimentales) modifie l’expression de certaines sous-unités des récepteurs pour l’acide gamma-aminobutyrique GABA A des rats exposés pendant la gestation. Administré pendant la période postnatale, le midazolam (benzodiazépine) n’a d’impact ni sur l’activité locomotrice ni sur les fonctions cognitives à l’âge adulte. Il n’a pas non plus d’effet à long terme sur la maturation des épines dendritiques de l’hippocampe.
En ce qui concerne les antidépresseurs, l’administration de fluoxétine (inhibiteur sélectif de la recapture de la sérotonine) pendant la phase précoce du développement altère, à l’âge adulte, les comportements émotionnels et augmente les effets renforçants de la cocaïne.
Ainsi, l’exposition précoce à certains psychotropes semble induire à l’âge adulte chez l’animal des modifications dans la régulation des comportements émotionnels et des conduites addictives, modifications sous-tendues probablement par l’altération de circuits neurochimiques. Néanmoins, ces données nécessitent d’être confortées par d’autres études.
Les investigations des effets des psychotropes administrés chez le rongeur juvénile (« adolescent ») sont plus nombreuses. Beaucoup portent sur les effets de la prise de méthylphénidate pendant la période pubertaire, évalués soit chez l’animal adulte sain, soit dans un modèle d’hyperactivité chez le rat. Dans leur grande majorité, ces études montrent que le méthylphénidate administré pendant la période juvénile ne modifie pas la sensibilité à la cocaïne chez l’animal adulte sain, mais, au contraire, augmente les effets aversifs à cette molécule et réduit les taux de son auto-administration. Cet effet n’est pas retrouvé lorsque le méthylphénidate est administré à l’âge adulte.
Dans des modèles d’hyperactivité, comme le rat spontanément hypertendu, les données montrent une amélioration de paramètres fonctionnels, comme l’attention ou la mémoire de travail sous méthylphénidate, accompagnée d’une réduction des taux tissulaires de neurotransmetteurs monoaminergiques (dopamine, sérotonine et noradrénaline) et d’une diminution des effets de la cocaïne sur le circuit de la récompense.
Ainsi, l’ensemble des données neurobiologiques tend à confirmer que le méthylphénidate en période juvénile n’induit pas d’action délétère notable.
L’avancée des connaissances sur les propriétés pharmacologiques des médicaments psychotropes améliore l’évaluation du risque de pharmacodépendance
Les médicaments psychotropes activent des cibles pharmacologiques et agissent sur des réseaux neuronaux qui sont les mêmes que ceux activés par des substances susceptibles d’abus telles que l’alcool, la cocaïne ou l’héroïne. En particulier, il a été montré que tous les produits qui entraînent une dépendance chez l’Homme augmentent la libération de dopamine (neurotransmetteur impliqué dans la dépendance) dans le noyau accumbens. Ce noyau fait partie d’un ensemble de structures cérébrales qui constituent le « circuit de la récompense ». Le noyau accumbens et le cortex préfrontal sont innervés par les neurones dopaminergiques issus de l’aire tegmentale ventrale (ATV). Ces neurones dopaminergiques sont régulés par de nombreux autres types de neurones libérant différents neurotransmetteurs, les principaux étant l’acide gamma-aminobutyrique (GABA), le glutamate, la sérotonine, la noradrénaline et les peptides opioïdes.
Les médicaments psychotropes capables d’agir, directement ou indirectement (comme certains anticholinergiques ou antipsychotiques atypiques), sur ces systèmes de neurotransmetteurs peuvent entraîner une pharmacodépendance per se, d’autant plus si leur mésusage permet d’augmenter les concentrations plasmatiques et donc cérébrales. Alternativement, ils peuvent potentialiser les effets positifs et subjectifs d’autres produits (topiramate et métamphétamine, ou trihexyphénidyle associé à l’alcool ou à des benzodiazépines, par exemple).
L’activité des neurones dopaminergiques de la voie mésolimbique est inhibée par des neurones GABAergiques. Toutes les molécules agissant sur le système GABA pourront donc modifier l’activité de la voie mésolimbique (tout comme le font les drogues d’abus). C’est le cas de certaines classes de benzodiazépines ou de substances apparentées (par exemple le zolpidem), agonistes des récepteurs GABA A capables de diminuer la libération de GABA, permettant ainsi l’activation de la voie mésolimbique et donc la libération de dopamine. Les substances opioïdes étant également capables d’inhiber cette activité GABAergique, un effet additif peut être observé après co-administration d’un opiacé et d’une benzodiazépine.
L’avancée des connaissances sur les propriétés pharmacologiques des médicaments psychotropes améliore l’évaluation du risque de pharmacodépendance en cas de mésusage. Ainsi, il a été montré que le méthylphénidate (Ritaline®), un psychostimulant indiqué dans la prise en charge du TDAH, partage deux mécanismes d’action de la cocaïne : l’inhibition de la recapture de la dopamine et celle de la noradrénaline. L’administration de méthylphénidate par une voie permettant d’atteindre rapidement ces cibles (par exemple, voie intraveineuse) peut donc entraîner des effets très proches de ceux observés avec la cocaïne. De plus, ces effets pourront être potentialisés par la consommation conjointe d’inhibiteurs sélectifs de la recapture de sérotonine (classe des antidépresseurs) en permettant de compléter l’action du méthylphénidate sur la troisième cible de la cocaïne, le système de recapture de la sérotonine. L’atomoxétine (Stattera®), un médicament non stimulant également indiqué dans le TDAH, est quant à lui sélectif du transporteur de la noradrénaline. Cette sélectivité lui confère des propriétés très différentes du méthylphénidate, avec en particulier une absence d’effets renforçants évalués dans différents modèles animaux.
D’autres classes de médicaments psychotropes, notamment les analgésiques opiacés, peuvent entraîner une pharmacodépendance. Toutefois, ils n’ont pas tous le même potentiel d’induction d’une pharmacodépendance ni le même potentiel de mésusage. Certains, comme le tramadol présent dans de nombreuses spécialités, sont de faibles agonistes des récepteurs opioïdes mu. D’autres, comme l’oxycodone (Oxycontin®), le rémifentanil ou la morphine sont des agonistes forts et présentent un potentiel plus élevé d’abus et de dépendance.
Enfin, il est important de prendre en considération toute exposition antérieure à des drogues licites ou illicites qui est susceptible de potentialiser le risque de pharmacodépendance à certains médicaments psychotropes. Ainsi, l’ensemble des données indique que les antidépresseurs n’entraînent pas de pharmacodépendance dans la population générale, mais leur consommation chez des patients dépendants à d’autres produits (opiacés, alcool par exemple) peut néanmoins conduire à un mésusage et à une utilisation abusive. Cette différence peut s’expliquer par des neuroadaptations, avec notamment une sensibilisation des systèmes de neurotransmetteurs comme les systèmes sérotoninergique et noradrénergique, à l’origine d’une exacerbation des effets des antidépresseurs et/ou une potentialisation des effets des drogues lors d’une co-consommation. Les mêmes observations peuvent être faites avec certains anti-histaminiques, des mésusages pouvant être rapportés chez des personnes ayant des problèmes de dépendance à l’alcool ou à d’autres produits, mais pas en population générale.
L’avancée des connaissances sur les mécanismes neurobiologiques des dépendances aux drogues licites et illicites permet de mieux appréhender les risques de mésusage et de pharmacodépendance des médicaments psychotropes. Néanmoins, il est important de noter que cette évaluation ne peut être pertinente que si la pharmacologie des médicaments est bien connue. En effet, un certain nombre de circuits neuronaux et de cibles pharmacologiques est maintenant bien identifié comme jouant un rôle essentiel dans la mise en place des conduites addictives et leur maintien. Toutes les molécules capables d’interagir sur ces circuits et/ou avec ces cibles peuvent donc présenter des risques de mésusage et de pharmacodépendance. Les propriétés pharmacocinétiques doivent également être intégrées dans l’équation finale de l’évaluation des risques de mésusage et de pharmacodépendance.
Des facteurs de vulnérabilité individuels interviennent dans la survenue d’une pharmacodépendance
Les facteurs de vulnérabilité individuels à la survenue d’une pharmacodépendance ont très certainement en partie une origine génétique comme pour d’autres addictions.
Les facteurs génétiques peuvent intervenir à plusieurs niveaux. De façon globale, les facteurs environnementaux seraient davantage impliqués dans l’initiation de la consommation, tandis que les facteurs génétiques auraient un rôle important sur la transition entre l’usage régulier et le développement d’une addiction.
Par ailleurs, il pourrait exister des facteurs de risque familiaux qui sous-tendent les troubles liés à l’usage de substances en général et des facteurs de risque familiaux spécifiques à certaines classes de substances psychoactives.
Les études d’agrégation familiale ont montré une élévation du risque de survenue d’une dépendance chez les apparentés des sujets présentant une dépendance à une substance psychoactive ; cette majoration du risque semble spécifique pour chaque produit. Les études d’adoption montrent une élévation du risque de mésusage de substances psychoactives chez les enfants dont les parents biologiques en souffrent. D’après les études de jumeaux, la vulnérabilité génétique pour les addictions repose en grande partie sur des facteurs communs pour le tabac, l’alcool et les autres substances, plutôt que sur des facteurs spécifiques aux différentes substances. Des études ont rapporté que la dépendance aux médicaments sédatifs dont les benzodiazépines reposait essentiellement sur des facteurs génétiques. Il est important de souligner que dans une étude de jumeaux n’incluant que des femmes, l’usage des médicaments sédatifs n’était lié qu’à des facteurs génétiques, de même que la dépendance quelle que soit la substance psychoactive étudiée (hallucinogènes, psychostimulants, opiacés, médicaments sédatifs).
Comme en attestent les études récentes, la susceptibilité génétique ne peut être appréhendée que dans une dynamique d’interactions des différents facteurs de risque et de protection.
De façon étonnante, étant donné le pouvoir addictogène élevé des benzodiazépines, peu d’études se sont intéressées aux différents gènes candidats vis-à-vis d’une sensibilité particulière à ces molécules.
Les benzodiazépines exercent leurs effets pharmacologiques via leur interaction avec un site du récepteur GABA A. Le gène codant la sous-unité GABA gamma 2 est un candidat potentiel à l’origine de différences phénotypiques dans la dépendance aux pouvoirs sédatif et hypnotique des benzodiazépines. En outre, le variant Pro385Ser de la sous-unité GABA A α6 diminue la sensibilité aux benzodiazépines, c’est-à-dire leur effet sédatif. Par ailleurs, d’autres systèmes, comme les récepteurs glutaminergiques de type AMPA, ont été associés à la sensibilité aux benzodiazépines puisque leur délétion génique modifie l’adaptation aux effets aigus et chroniques de ces benzodiazépines.
En revanche, de nombreuses études se sont penchées sur les facteurs génétiques de la pharmacodépendance aux opiacés. Il ressort de façon claire une association entre les variants du gène Abcb1b/Mdr1 codant la glycoprotéine P 170 (transporteur des xénobiotiques) et les doses requises de méthadone pour atteindre l’efficacité thérapeutique chez les patients héroïnomanes en substitution. Le polymorphisme 1236C versus T serait impliqué dans la différence entre les doses thérapeutiques nécessaires « hautes » versus « basses » de méthadone. Ces données sont confortées par une étude préclinique mettant en évidence l’implication de ce même gène dans la sensibilité à la morphine chez la souris. D’autres cibles ont été étudiées. En particulier, le rôle du récepteur μ des opiacés dans la réponse GABAergique à la morphine a été montré chez le rongeur. Chez l’Homme, les variants des gènes codant les récepteurs μ, δ et κ semblent jouer un rôle dans l’addiction à l’héroïne mais aussi à la cocaïne.
Le rôle des récepteurs des monoamines (dopamine, sérotonine, noradrénaline) dans la pharmacodépendance aux opiacés a été également souligné, en particulier ceux du système dopaminergique. Les polymorphismes géniques du récepteur D2 mais aussi de certains éléments clés de la régulation monoaminergique (COMT, TPH1, TPH2)
17
COMT : catéchol-O-méthyltransférase ; TPH : tryptophane hydroxylase
sont clairement impliqués dans le développement des addictions aux opiacés et à la cocaïne et dans leur traitement.
Enfin, certains gènes semblent avoir une place non négligeable dans le développement de l’addiction aux opiacés. C’est le cas de gènes codant le canal potassique GIRK2, la protéine régulatrice des protéines G (RGS4) ou encore la cytokine IL-1β et le facteur neurotrophique BDNF.
En matière de dépendance aux psychostimulants, les études effectuées sur des modèles de souris transgéniques ont montré que de nombreux éléments des systèmes dopaminergique et sérotoninergique sont sollicités, que ce soient les récepteurs dopaminergiques dans leur ensemble, le transporteur dopaminergique et sérotoninergique, ou encore les récepteurs de la sérotonine 5-HT1A, 5-HT1B, 5-HT2A ou 5-HT2C.
Enfin, des études de type pangénomique ont mis en évidence dans l’addiction le rôle du gène neurexine 3 qui intervient dans les fonctions synaptiques.
Toutefois, les données recueillies par la seule analyse génétique de la pharmacodépendance ne suffisent pas à donner une vision claire et convergente de l’intervention d’un gène donné dans cette pathologie. Récemment, les études consacrées au rôle des mécanismes épigénétiques ont mis en lumière l’importance de l’environnement dans l’expression de gènes impliqués dans les phénomènes de dépendance.
Le terme « épigénétique » définit les modifications transmissibles et réversibles de l’expression des gènes ne s’accompagnant pas de changements dans la séquence nucléotidique de l’ADN. L’expression d’un gène peut être régulée par différents facteurs dont l’état compacté ou décompacté de la chromatine, régulé par les modifications post-traductionnelles des histones liées à l’ADN. La méthylation de ces protéines au niveau de résidus lysine ou arginine induit une fermeture de la chromatine quand l’acétylation des résidus lysine entraîne une ouverture de la chromatine permettant ainsi la transcription. Par ailleurs, l’expression d’un gène peut également être contrôlée par la méthylation de l’ADN au niveau des résidus cytosine des îlots CpG essentiellement localisés dans les régions proximales des promoteurs des gènes : une faible méthylation se traduit le plus souvent par une forte expression du gène alors qu’un haut niveau de méthylation inactive le gène.
Des hypothèses émergentes suggèrent que ces altérations épigénétiques sont des mécanismes importants sous-tendant la dépendance et la réponse neurobiologique aux substances addictives, que ce soit l’alcool, la nicotine, la cocaïne, les amphétamines ou les opiacés. La dépendance à différents types de substances entraîne des adaptations liées à la plasticité neuronale dans le circuit de récompense. Ces adaptations sont médiées en partie par des modifications épigénétiques de l’expression de certains gènes. L’intervention par exemple du facteur de répression de la transcription du gène MeCP2 (methyl CpG-binding protein-2, fortement impliqué dans la neuroplasticité) dans la réponse comportementale aux psychostimulants a été clairement établie. Néanmoins, la majorité de ces travaux a été réalisée chez les rongeurs et peu de données sont disponibles chez l’Homme. De plus, la plupart des études chez l’Homme ont trait à la régulation épigénétique de gènes en relation avec l’alcool et/ou la nicotine. Pour les médicaments psychotropes, on peut toutefois citer une étude chez les patients traités par méthadone, qui montre une augmentation de la méthylation de l’ADN au niveau du promoteur du gène du récepteur μ des opiacés OPRM1, pouvant conduire à la réduction de son expression. La recherche épigénétique est en plein essor et les avancées technologiques permettront dans un proche futur d’analyser les patterns de méthylation (« méthylome ») et les profils épigénétiques liés en particulier aux pathologies addictives.
Les politiques publiques s’appuient sur des dispositifs nationaux de vigilance et d’évaluation de la pharmacodépendance
Au niveau international, les substances psychotropes comme les stupéfiants figurent sur des listes annexées à des conventions établies dans le cadre des Nations Unies. L’application des traités internationaux relatifs au contrôle des stupéfiants est surveillée par l’Organe international de contrôle des stupéfiants (OICS). Ses missions s’articulent autour des trois conventions internationales : la Convention unique sur les stupéfiants de 1961 (qui classe les stupéfiants en 4 tableaux – tableaux I, II, III, IV – selon le niveau de risque pour la santé publique), la Convention de 1971 sur les substances psychotropes (classées comme les stupéfiants, en 4 tableaux) et la Convention des Nations Unies de 1988 contre le trafic illicite de stupéfiants et de substances psychotropes.
Les conventions internationales s’appliquent au niveau des États. Au niveau de l’Europe, deux institutions interviennent à l’échelle communautaire dans le cadre des médicaments psychotropes et des stupéfiants ; il s’agit de l’Observatoire européen des drogues et des toxicomanies (OEDT)
18
chargé de collecter, analyser et diffuser des informations objectives, fiables et comparables sur le phénomène des drogues et des toxicomanies au niveau européen, et de l’Agence européenne du médicament (EMA)
19
chargée de l’évaluation des médicaments. L’OEDT a mis en place en 2008 une base de données sur le statut des médicaments psychotropes et des stupéfiants dans les 27 États membres et en Norvège (l’
European Legal Database on Drugs, ELDD). Cette base présente les classements de chaque substance (y compris les précurseurs) et le profil de la législation par pays
20
. Par ailleurs, les principes des règles de prescription et de délivrance des médicaments (qu’il s’agisse de psychotropes ou de toute autre catégorie de médicament) sont définis dans un code communautaire relatif aux substances médicinales à usage humain.
La réglementation française actuelle applique la classification internationale des stupéfiants et des psychotropes et précise par ailleurs les substances nécessitant une surveillance particulière au niveau national. Ce classement repose sur une évaluation du potentiel d’abus et de dépendance mais aussi du risque évalué en termes de santé publique auprès de la population au regard de l’intérêt thérapeutique. La transposition en droit français de la réglementation internationale des stupéfiants et des psychotropes a été effectuée par l’arrêté du 22 février 1990 modifié. Le processus national de classement d’une substance comme stupéfiant ou comme psychotrope se base sur les éléments d’appréciation élaborés par l’OMS ainsi que sur les données fournies par le système français d’évaluation de la pharmacodépendance. Ce dispositif, mis en place en 1990
21
Circulaire ministérielle DPHM/03/09/01
et officialisé par décret en 1999
22
Décret n°99-2 49, et décret n°2007-157 du JORF
, participe à la politique de lutte contre la drogue et la toxicomanie en coordination avec la Mission interministérielle de lutte contre la drogue et la toxicomanie (Mildt). Il comprend notamment un réseau national de centres d’évaluation et d’information sur la pharmacodépendance (CEIP), ou réseau d’addictovigilance, chargé de recueillir et d’évaluer les cas d’abus et de pharmacodépendance auprès des professionnels de santé et de réaliser des travaux d’expertise. Par rapport au système classique de pharmacovigilance, principalement fondé sur la notification spontanée des professionnels de santé et désormais des patients, cette activité d’addictovigilance se distingue par une approche originale combinant le principe de la notification spontanée avec des informations complémentaires issues de recueils spécifiques soit sur des populations ciblées, soit sur des conséquences de l’abus et de la dépendance. Par ailleurs, il est important de souligner que l’addictovigilance concerne aussi bien les médicaments que des substances illicites, produits souvent successivement ou simultanément impliqués dans les cas d’abus ou de dépendance, qui dépasse largement le champ de la pharmacovigilance classique. Ce réseau représente l’outil de travail de la Commission Nationale des Stupéfiants et Psychotropes (CNSP), instance scientifique qui examine les possibilités de classement des substances psychoactives et transmet son avis au Directeur Général de l’Afssaps et au Ministre en charge de la santé. Ce dispositif original pourrait servir de modèle aux autres pays européens qui souhaiteraient se doter d’une politique de surveillance.
La plupart des médicaments commercialisés en France, appartenant aux substances dites « vénéneuses », sont au moment de leur AMM (autorisation de mise sur le marché) classés sur des listes qui réglementent leur prescription et leur délivrance. Les produits pour lesquels la sécurité d’emploi est considérée comme élevée peuvent être non listés et ne pas nécessiter un support de prescription (prescription médicale facultative, PMF). Même s’ils contiennent des substances psychoactives (exemple de la codéine, classée au tableau II des stupéfiants, mais pouvant être délivrée sans ordonnance, à dose exonérée de 20 mg par unité thérapeutique), ils peuvent être directement accessibles au public en automédication. Les substances classées sur les listes I et II nécessitent une prescription médicale. Le renouvellement des médicaments de la liste I est possible sur indication écrite du médecin précisant le nombre de renouvellements ou la durée du traitement (dans une limite de 12 mois). Le renouvellement des médicaments de la liste II est possible pendant 12 mois, sauf si le prescripteur l’interdit. La durée de prescription est en général au maximum de 3 mois pour la liste I, sauf pour les hypnotiques (durée de prescription limitée à 4 semaines) et pour les anxiolytiques (12 semaines).
Les substances classées comme stupéfiants et certains médicaments de la liste I (buprénorphine, flunitrazépam, clonazépam, clorazépate 20 mg) ont des modalités de prescription et de délivrance plus restrictives que les autres substances vénéneuses pour limiter le risque d’abus et de dépendance. Cette réglementation impose une prescription sur ordonnance sécurisée non falsifiable, avec une durée de prescription de 7 jours au maximum pour les formes injectables et de 28 jours pour les formes orales. Il existe des exceptions avec des limitations à 14 jours, notamment pour la méthadone ou le flunitrazépam. La délivrance de ces produits par le pharmacien doit se faire par fraction de 7 jours.
La mise en place de plans de gestion des risques depuis 2005, notamment dans le contexte de l’évaluation du rapport bénéfice/risque d’un médicament présentant un potentiel d’abus et de dépendance, prolonge et élargit la démarche de pharmacovigilance, principalement pour les nouveaux médicaments. Mise en œuvre par les laboratoires pharmaceutiques, avec une validation et un contrôle par les autorités de santé compétentes, cette démarche a permis une formalisation et une standardisation des exigences en termes d’utilisation et de surveillance d’un médicament psychotrope.
En France, les programmes de surveillance de l’abus et de la dépendance aux médicaments psychotropes sont encore à perfectionner
Aux États-Unis, de nombreux programmes ont été mis en œuvre depuis 1972 pour surveiller l’abus et la dépendance aux médicaments psychotropes. Ces programmes sont aujourd’hui utilisés de façon coordonnée dans le cadre d’une stratégie nationale de contrôle et de surveillance des drogues (
National Drug Control Strategy), pilotée par l’ONCDP (
Office of National Drug Control Policy)
23
L’ONCDP est directement sous la responsabilité de la « Maison Blanche ».
. Les programmes déployés sur l’ensemble du territoire des États-Unis dépendent le plus souvent d’organismes fédéraux tels que le ministère de la justice (DEA,
Drug Enforcement Administration), le NIDA (
National Institute on Drug Abuse), la SAMHSA (
Substance Abuse and Mental Health Services Administration) ou le CDC (
Centers for Disease Control and Prevention) ou encore par des associations de professionnels comme l’ASIPP (
American Society Of Interventional Pain Physicians). Par ailleurs, d’autres programmes (le plus souvent des PDMP –
Prescription Drug Monitoring Programs) ont été mis en place dans certains États.
De méthodologies variées, ces programmes rassemblent divers types d’enquêtes ou de recueil : enquêtes transversales par enquêteurs ou questionnaires auto-administrés, suivis de cohortes, analyses de bases de données (files actives, délivrances, notifications spontanées, analyses toxicologiques...), interviews d’experts, analyses des flux Internet.
Ces programmes concernent des populations diverses : population générale, adolescents, usagers de drogues reçus en centres spécialisés, patients recevant un traitement de substitution aux opiacés, patients reçus aux urgences ou décédés en relation avec l’usage de drogues.
Les programmes ont en commun un certain nombre de caractéristiques : chaque programme est sous la responsabilité d’un promoteur/financeur bien déterminé ; un site Internet spécifique leur est consacré ; leur objectif est bien défini ; leur méthodologie est clairement exposée. Ces programmes sont la source de nombreuses publications et font l’objet de multiples travaux d’évaluation et de comparaison de leurs résultats.
L’approche est presque exclusivement quantitative. Il n’existe pas de programme fédéral selon une approche qualitative (observations anthropologiques, focus groupes...).
Cependant, l’accessibilité aux résultats est très variable : elle est souvent très facile et complète (par exemple, DAWN ou MTF) mais peut être difficile en dehors des publications scientifiques ou d’un accès payant (par exemple, Navippro) ; enfin, leur représentativité est très variable selon les programmes.
Certains de ces programmes apportent des informations concernant l’abus et la dépendance aux médicaments psychotropes. Les programmes NSDUH et MTF permettent de mesurer l’usage de psychotropes en population générale et chez les adolescents ; le programme TEDS effectue le suivi du détournement de psychotropes chez les usagers de drogues en demande de traitement auprès des centres spécialisés. Le programme DAWN renseigne sur les recours des sujets aux services d’urgence et l’analyse des causes de décès et apporte des informations sur les conséquences médicales de l’abus ou la dépendance aux psychotropes. Le département de la Justice américaine a mis en place en 2002 un PDMP pour certains médicaments classés comme stupéfiants, ce qui permet le suivi des prescriptions de médicaments et donne de ce fait des informations sur les pratiques des médecins et sur le nomadisme médical. Le NFLIS renseigne sur l’ensemble des analyses toxicologiques réalisées sur des usagers de drogues ou lors des saisies et apporte des données sur la composition des produits utilisés (substances actives, produits de coupe...) et leur disponibilité.
Principaux programmes de surveillance aux États-Unis en fonction de leur méthodologie, de leur organisme financeur et de leur ancienneté
|
Intitulé du programme
|
Organisme /Année de début
|
Principe
|
|
Enquêtes de consommation en population
|
|
Enquêtes de consommation en population générale
| | |
|
NSDUH (National Survey on Drug Use & Health)
|
SAMHSA / 1972
|
Enquête transversale annuelle randomisée sur échantillon représentatif
|
|
Nesarc (National Epidemiologic Survey on Alcohol and Related Conditions)
|
NIAAA / 2001
|
Cohorte/questionnaires
|
|
Enquêtes de consommation chez les jeunes
| | |
|
MTF (Monitoring The Future)
|
NIDA / 1975
|
Enquête transversale annuelle/auto-questionnaire
|
|
YRBS (Youth Risk Behavior Surveillance)
|
CDC / 1991
|
Cohortes
|
|
Enquêtes de consommation chez les usagers de drogues
| | |
|
TEDS (Treatment Episode Data Set)
|
SAMHSA / 1987
|
Enquête transversale annuelle
|
|
Enregistrement des conséquences médicales de l’abus
|
|
DAWN (Drug Abuse Warning Network)
|
SAMHSA / 1972
|
Enregistrements des admissions aux urgences et des décès
|
|
NPDS (National Poison Data System Information)
|
CDC / 1983
|
Base de données centresantipoison + notifications
|
|
AERS (Adverse Event Reporting System)
|
FDA / 2000
|
Base de données d’événements indésirables
|
|
Enregistrement des délivrances de psychotropes et des analyses des laboratoires
|
|
NFLIS (National Forensic Laboratory Information System)
|
DEA / 1998
|
Base de données analysestoxicologiques
|
|
PDMP (Prescription Monitoring Database)
|
D. Justice / 2002
|
Base de données de délivrance pour certains médicaments dont les opioïdes
|
|
Programmes utilisant des sources d’information multiples
|
|
CEWG (Community Epidemiology Work Group)
|
NIDA / 1976
|
Synthèse d’experts
|
|
Navippro (National Addictions Vigilance Intervention and Prevention Program)
|
NIDA / 2001
|
Auto-questionnaires ASI+ analyses Internet
|
|
Radars (Researched Abuse, Diversion and Addiction-Related Surveillance)
|
Denver Health / 2002
|
Enquêtes transversales + cohortes
|
NIAAA : National Institute on Alcohol Abuse and Alcoholism ; SAMHSA : Substance Abuse and Mental Health Services Administration ; CDC : Centers for Disease Control et Prevention ; NIDA : National Institute on Drug Abuse ; FDA : Food and Drug Administration ; D. Justice : US Department of Justice, DEA ; ASI : Addiction Severity Index
Principaux programmes de surveillance en France
|
Enquêtes
|
Coordination
|
Population
|
Fréquencede l’enquête
|
|
Enquêtes en population générale
|
|
Baromètre santé
|
Inpes
|
Adultes : 15-75 ans
|
5 ans
|
|
Espad (European School Survey Project on Alcohol and other Drugs)
|
OFDT (pour l’enquête en France)
|
15-16 ans
|
4 ans
|
|
Escapad (Enquête sur la santé et les consommations lors de la journée d’appel de préparation à la défense)
|
OFDT
|
17 ans
|
Annuelle initialement puis tous les 3 ans
|
|
Enquêtes dans les populations d’usagers de drogues
|
|
Oppidum (Observation des produits psychotropes illicites ou détournés de leur utilisation médicamenteuse)
|
CEIP
|
Sujets présentant un abus ou une pharmacodépendance
|
Annuelle
|
|
Opema (Observation des pharmacodépendances en médecine ambulatoire)
|
CEIP
|
Patients usagers de drogues illicites ou de médicaments détournés de leur usage thérapeutique pris en charge en médecine ambulatoire (enquête auprès des médecins généralistes)
|
Annuelle
|
|
Recap (Recueil commun sur les addictions et les prises en charge)
|
OFDT
|
Usagers des Csapaa
|
Recueil en continu (analyse annuelle)
|
|
ENa-Caarud (Enquête nationale-Caarud)
|
OFDT
|
Usagers des Caarudb
|
Tous les 2 ans
|
|
Trend (Tendances récentes et nouvelles drogues)
|
OFDT
|
Population à forte prévalence d’usage de drogues
|
Annuelle
|
|
Enquête Coquelicot
|
InVS, Inserm, Anrs
|
Population d’usagers de drogue injectée ou sniffée
|
6/7 ans
|
|
Enregistrement des conséquences médicales de l’abus
|
|
Drames (Décès en relation avec l’abus de médicaments et de substances)
|
CEIP
|
Cas de décès liés à l’abus de substances psychoactives survenant chez les usagers de drogues
|
Recueil annuel prospectif
|
|
Surveillance des délivrances
|
|
Osiap (Ordonnances suspectes, indicateur d’abus possible)
|
CEIP
|
Ordonnances falsifiées présentées en pharmacie d’officine (recueil auprès des pharmacies d’officine)
|
Annuelle
|
|
Asos (Antalgiques stupéfiants et ordonnances sécurisées)
|
CEIP
|
Population traitée par antalgiques stupéfiants (enquête auprès des pharmaciens d’officine)
|
Annuelle
|
a Centres de soins, d’accompagnement et de prévention en addictologie ; b Centres d’accueil et d’accompagnement à la réduction des risques pour les usagers de drogues
La France dispose également de programmes couvrant une large part des différents champs explorés par les programmes américains.
Ces programmes apportent des informations sur la consommation en population générale ou en populations spécifiques (usagers de drogues), les conséquences médicales de l’abus, le suivi des délivrances de psychotropes et des analyses toxicologiques des laboratoires.
Les enquêtes du Baromètre santé en population générale, coordonnées par l’Inpes, fournissent des données sur le nombre de consommateurs de substances psychoactives, dont les médicaments psychotropes, selon l’âge et le sexe ainsi que les principaux types de médicaments consommés.
L’enquête française Escapad à l’occasion de la journée d’appel de préparation à la défense et l’enquête européenne Espad renseignent sur les niveaux d’usage et les évolutions en termes de produits et de modalités de consommation et d’obtention chez les adolescents.
Chez les usagers de drogues, différentes enquêtes sont menées selon un rythme annuel ou de façon continue. Il s’agit principalement des programmes Oppidum (CEIP) conduit dans les centres d’accueil spécialisés et Opema en médecine ambulatoire, spécialement conçus pour observer l’abus et la dépendance aux psychotropes ou encore les programmes ENa-Caarud et Recap menés par l’OFDT. Par ailleurs, un programme original d’observations qualitatives, l’enquête annuelle Trend (OFDT) qui n’a pas d’équivalent au niveau national aux États-Unis, complète très utilement les observations quantitatives.
La France dispose d’un programme conduit par les CEIP enregistrant les décès en relation avec l’abus de médicaments et de substances (Drames). En revanche, il n’y a pas d’équivalent du programme DAWN auprès des services d’urgences. Pourtant, les très nombreuses publications réalisées à partir de DAWN montrent à l’évidence l’intérêt de ce type de programme pour suivre les conséquences médicales de l’usage de stupéfiants et médicaments psychotropes.
Enfin, les délivrances de médicaments psychotropes sont analysées à partir des bases de données de remboursement de l’Assurance Maladie et auprès de l’EGB (Échantillon Généraliste de Bénéficiaires), ou bien à partir des enquêtes nationales périodiques auprès des pharmaciens d’officine, via l’enquête Osiap (CEIP) recueillant les ordonnances suspectes présentées en officine, ou via l’enquête Asos (CEIP) sur les modalités de prescriptions des stupéfiants sur ordonnance sécurisée.
Même s’ils ne sont pas aussi nombreux qu’aux États-Unis, les programmes existant en France sont des sources importantes d’observations et d’informations sur la consommation, le mésusage, le détournement, l’abus et la dépendance. Cependant, il semble manquer une stratégie de coordination de l’ensemble des programmes pour en faciliter l’accès et la mise en commun des données.
Le système national de vigilance et d’évaluation permet d’étudier les sources d’approvisionnement en médicaments détournés
Les sources d’approvisionnement en médicaments détournés sont multiples. Elles peuvent être réparties en trois grandes catégories selon leur origine : le détournement de prescription et/ou de délivrance (nomadisme médical ou « doctor shopping », nomadisme pharmaceutique ou « pharmacy hopping », ordonnances falsifiées) ; les cyberpharmacies et l’approvisionnement par Internet ; enfin, la contrefaçon et la chaîne de distribution.
Selon les contextes des études (populations et médicaments ciblés), les données sur la part de ces diverses sources d’approvisionnement en médicaments psychotropes sont différentes.
Les données recueillies dans le cadre du système national d’évaluation de la pharmacodépendance, mis en place en 1990 en France, permettent d’identifier les différentes sources d’approvisionnement en médicaments psychotropes et d’obtenir une estimation indirecte de la quantité détournée. Les études réalisées auprès de personnes visitant les centres de soins (telles que l’enquête Oppidum) montrent que la principale source d’approvisionnement en médicaments détournés est le nomadisme médical (doctor shopping) ou polyprescription. Ce mode d’approvisionnement permet d’obtenir une quantité importante de médicaments par la multiplication de prescriptions concomitantes sur une période de temps déterminée. La polyprescription concerne aussi bien les sujets désirant de grandes quantités de médicaments pour leur propre consommation, que les sujets dont l’objectif est de les revendre au marché parallèle, ou de les échanger contre d’autres substances.
À partir des bases de données de remboursement de l’Assurance maladie, le phénomène de nomadisme médical ou polyprescription, considéré comme un indicateur indirect du détournement de médicament, montre qu’une frange marginale de sujets (2 à 5 % de l’ensemble des sujets recevant au moins une prescription) est généralement à l’origine de 80 % de la totalité du détournement par polyprescription, quel que soit le médicament (buprénorphine, méthylphénidate, flunitrazépam ou clonazépam, par exemple).
Les enquêtes Osiap et Asos (Asos ciblant uniquement les délivrances de médicaments opiacés sur ordonnances sécurisées) permettent d’évaluer, pour certains médicaments, le détournement par falsification d’ordonnance. La falsification d’ordonnance consiste soit à modifier une prescription licite faite par un médecin sur un support adéquat (modification de la posologie et/ou de la durée de la prescription, ou rajout de médicaments non prescrits), soit à présenter une ordonnance volée ou fabriquée. La proportion exacte des ordonnances falsifiées n’est pas connue (d’autant que les falsifications peuvent être difficiles à identifier), mais représenterait une très faible part de l’ensemble des prescriptions médicales. En 2003, dans l’étude Asos, 1 % des ordonnances pour analgésiques stupéfiants étaient falsifiées.
Concernant le nomadisme pharmaceutique (pharmacy hopping), l’absence de base de données de délivrance établie à partir de pharmacies d’officine rend difficile l’évaluation de ce phénomène. Il concerne notamment les médicaments à prescription médicale facultative, comme les dérivés codéinés ou des hypnotiques-sédatifs de type anti-histaminiques H1, qui peuvent être obtenus plus aisément dans le cadre de l’automédication.
La diffusion et le détournement d’usage des médicaments à potentiel d’abus par le biais d’Internet sont évoqués depuis plus de 10 ans. Le projet de recherche européen PsychoNaut 2002 qui a été financé par la Commission européenne (DG Sanco) en 2002, a recensé et mis à jour une base de données sur les différentes substances psychoactives disponibles via Internet
24
. Selon ce projet, on peut distinguer quatre grands types de « cyberpharmacies » permettant l’accès à des médicaments psychotropes : des pharmacies « légitimes » qui délivrent uniquement sur prescription médicale valide authentifiée (reconnues par la
Food and Drug Administration aux États-Unis) ; des pharmacies qui délivrent à des abonnés payant une souscription mais ne disposant pas de prescription ; des pharmacies spécialisées dans les «
smart drugs »
25
Substances consommées à visée de performance
qui disposent d’une liste limitée de produits ; enfin, des pharmacies qui proposent sans prescription des substances dont l’accès est contrôlé (stupéfiants et psychotropes). Les recommandations de l’OICS de 2009 invitent les États à prendre des mesures efficaces pour prévenir la vente illégale via Internet de substances classées. En effet, le volume des ventes illicites de stupéfiants et de psychotropes aurait considérablement augmenté au cours des dernières années, « faisant de ce moyen une source importante d’approvisionnement pour les toxicomanes »
26
ORGANE INTERNATIONAL DE CONTRÔLE DES STUPÉFIANTS (OICS). Principes directeurs à l’intention des gouvernements pour la prévention de la vente illégale via l’Internet de substances placées sous contrôle international. 2009 : 17p
. Cependant, selon les études disponibles auprès des usagers de substances ou des enquêtes en population générale aux États-Unis ou en France, ce phénomène concerne très peu de sujets.
Le médicament de contrefaçon est, selon l’OMS (1992), un produit étiqueté frauduleusement de manière délibérée pour en dissimuler la nature et/ou la source. Les médicaments psychotropes présentant un potentiel d’abus et de dépendance peuvent être concernés à double titre, d’une part en alimentant le trafic de substances psychoactives (comme les drogues illicites) et d’autre part, comme médicaments de qualité douteuse proposés dans des pays, des zones géographiques ou des populations défavorisées pour lesquels l’accès à ces produits est limité. L’Europe est concernée par les médicaments de contrefaçon depuis le début des années 2000. Des coopérations internationales ont été mises en place, avec des opérations coordonnées entre Interpol et l’OMS. L’opération PANGEA II en 2009 (impliquant la France) a permis des saisies importantes de médicaments contrefaits (notamment des psychotropes), plusieurs interpellations en France et l’identification de plus de 150 sites illégaux dont 20 rattachés à la France. En 2009, aucune contrefaçon n’a été identifiée dans le circuit d’approvisionnement officiel de la distribution pharmaceutique.
Le détournement des médicaments peut s’opérer tout au long de la chaîne de distribution (sites de fabrication, grossistes, centres de distribution, entrepôts, pharmacies à usage intérieur pour les établissements de soins ou communautaires). Ce phénomène est évoqué dans la littérature nord-américaine, sans donner d’informations sur son importance. En Europe et plus particulièrement en France, il n’existe pas de données publiées sur cette question. Les médicaments à usage vétérinaire peuvent également être impliqués en raison d’un détournement au niveau de la chaîne de distribution (exemple des vols de kétamine dans les cliniques vétérinaires avant le classement de la substance comme stupéfiant en France en 1997).
En France, l’enquête Oppidum apporte trois types de résultats concernant l’acquisition illégale des médicaments psychotropes. Cette enquête a permis d’identifier la part respective des différentes sources d’acquisition illégale de médicaments psychotropes. En 2008, les deux principales sources d’acquisition illégale étaient le marché de rue (78 %) et le don par les pairs (17 %), suivies par le vol (2,3 %), la falsification d’ordonnance (2,3 %) et enfin Internet (0,7 %).
Cette enquête identifie que parmi les usagers de BHD et de méthadone interrogés, la proportion d’usagers ayant obtenu le médicament par le marché de rue est respectivement de 35 % et 20 %.
L’enquête Oppidum permet également d’évaluer la part d’obtention illégale de certains médicaments psychotropes : la kétamine (100 % d’obtention illégale), le flunitrazépam (61 %), la morphine (56 %), le trihexyphénidyle (50 %) et le méthylphénidate (47 %). Il faut cependant souligner que ces médicaments sont beaucoup moins consommés que la BHD et la méthadone puisque cette enquête concerne des sujets vus en centre de soins.
Les programmes de prévention en population générale spécifiques aux médicaments psychotropes sont rares
Un premier exemple de politiques publiques est donné par les recommandations réglementaires d’évaluation pré-AMM du potentiel de dépendance d’un médicament afin d’anticiper les risques d’abus et de mésusage lors de l’utilisation du médicament en population générale. Une telle évaluation s’est mise en place progressivement au niveau national et international
27
Les premières recommandations de la FDA pour la réalisation d’études précliniques et cliniques du potentiel d’abus pour tout médicament agissant au niveau du système nerveux central datent des années 1990 et leur version actualisée date de 2003. En Europe, l’EMA a proposé des recommandations pour l’évaluation préclinique du potentiel d’abus en 2006.
. Elle inclut la détermination des caractéristiques pharmacologiques et pharmaceutiques dans le but de réduire le détournement (propriétés pharmacocinétiques permettant de limiter les effets intenses et rapides, caractéristiques galéniques limitant l’utilisation d’une autre voie d’administration...). Les informations recueillies à l’étape pré-AMM conduisent à mettre en place une réglementation appropriée, par exemple en fixant des règles strictes de prescription ou de délivrance du médicament, ou encore en restreignant son accessibilité dans le milieu ambulatoire. Ces informations à l’étape pré-AMM peuvent également aboutir à des mesures d’éducation thérapeutique et de minimisation du risque. Depuis 2005, tout nouveau médicament mis sur le marché est accompagné d’un plan de gestion des risques, le plus souvent international, avec la possibilité d’une déclinaison nationale. Pour tout médicament psychoactif, l’évaluation de son potentiel d’abus et de dépendance entre de fait dans ce plan de gestion des risques et des propositions d’action de minimisation des risques d’abus ou de dépendance sont exigées pour l’obtention de l’AMM. Aux États-Unis, des programmes de surveillance et de contrôle (tels que les «
Medicament Therapy Management Systems » ou les
« Prescription Drug Monitoring Programs ») se sont très largement développés depuis la fin des années 1990, en réponse aux abus d’analgésiques opiacés. L’objectif de ces programmes est de surveiller les signaux éventuels d’abus et de mésusage des médicaments psychoactifs (et des médicaments non psychoactifs également) en apportant une réponse extrêmement rapide. Par ailleurs, l’impact de mesures réglementaires ou éducatives peut être évalué rapidement en raison de la pérennité du système de surveillance.
Les programmes de gestion des risques (PGR) accompagnant la mise sur le marché des nouveaux médicaments depuis 2005 se sont greffés sur les systèmes pré-existants. Ces programmes sont également demandés par les autorités de régulation à l’échelle nationale : par exemple, PGR de la buprénorphine et de la méthadone en France, oxycodone aux États-Unis. L’impact des mesures mises en place dans le cadre des programmes de gestion des risques est en cours d’évaluation. En France, l’exemple de la mise sur le marché de la méthadone gélule (forme galénique rendant le détournement de la voie d’administration difficile) accompagnée d’actions de minimisation (réglementaire pour la restriction de prescription, éducative avec le conditionnement sécurisé et les plaquettes d’information au patient) est pour l’instant un argument plutôt favorable à ce type de démarche, même si une vigilance attentive reste nécessaire.
Les programmes de limitation des prescriptions frauduleuses peuvent cibler un médicament donné (ou une classe) ou encore être généralisés à l’ensemble des médicaments prescrits. Il existe de nombreuses déclinaisons de stratégies de protection de la prescription à travers le monde. Ces stratégies reposent sur une protection du support de prescription, allant d’un support papier sécurisé : support d’ordonnances sécurisées filigranées pour la prescription des stupéfiants depuis 1999 en France ; ordonnances à plusieurs feuillets avec l’exemple des ordonnances tripliquées dans les années 1990 dans l’État de New York pour les benzodiazépines ; support électronique de prescription, reliant directement le prescripteur à l’exécutant pour la délivrance du médicament, système généralisé en Suède ou dans quelques États nord-américains. Les résultats de ces mesures d’ordre réglementaire sont mitigés. La mise en place des ordonnances tripliquées dans l’État de New York dans les années 1990 a conduit à une diminution globale de la consommation des benzodiazépines, mais avec un transfert de prescription vers d’autres substances psychoactives comme les carbamates. Des analyses récentes évaluant l’impact à long terme de cette mesure, montrent surtout une diminution importante de l’utilisation non problématique des benzodiazépines, avec notamment l’absence de stratégie de substitution et une diminution de la prise en charge médicale des patients psychiatriques.
La limitation de l’accessibilité à certains médicaments psychoactifs, mesure réglementaire assez largement répandue, s’inscrit souvent dans les programmes de surveillance et de contrôle. Il peut s’agir d’une prohibition stricte, assortie dans toutes les expériences d’un transfert vers d’autres produits (autres médicaments moins contraints ou substances illicites), ou d’une limitation avec un accompagnement éducatif approprié. La mise en place progressive, à partir de 1992-93, d’une administration supervisée de la méthadone dans les centres de soins en Grande-Bretagne s’est accompagnée d’une diminution des décès par surdosage, sans restriction de l’accès à la méthadone. Cependant, si les mesures ne sont pas accompagnées d’interventions éducatives ou intégrées à une approche globale, des résultats variables et parfois totalement négatifs (transferts de consommation vers des substances, licites ou non, beaucoup plus dangereuses) sont observés. L’accessibilité au médicament à risque peut également être modifiée par des restrictions du remboursement par les systèmes d’assurance maladie. À la suite d’un déremboursement, on observe en général une diminution de la consommation, mais la diminution parallèle de l’abus et du mésusage de ces médicaments n’est pas toujours mesurée. L’accessibilité devient de fait plus difficile pour les sujets présentant un niveau socioéconomique plus défavorable. En Europe, plusieurs pays (Allemagne, Belgique, Danemark, Italie) ont exclu du remboursement les benzodiazépines anxiolytiques ou hypnotiques au cours des dernières années. Très peu d’études ont évalué l’impact de ces mesures sur les populations de sujets abuseurs, et sur le transfert vers d’autres substances (en particulier illicites). Les mesures de déremboursement sont le plus souvent décidées par les organismes d’assurance maladie avec une justification autant économique que de santé publique. Toutefois, dans quelques rares exemples, une évaluation globale de l’impact du déremboursement a été effectuée : en mai 2002, l’Australie a pris la décision de ne plus rembourser le témazépam sous forme gélule, en raison d’un usage problématique de cette forme, plus facilement injectable que la forme comprimé, et donc pourvoyeuse d’un risque infectieux et thrombotique accru chez les usagers de drogues par voie intraveineuse. L’analyse des prescriptions et une enquête ciblée auprès des usagers ont montré que la diminution de la prescription de témazépam gélule a été compensée par un transfert équivalent vers la forme comprimé, sans effet apparent sur les pratiques d’injection. Ce résultat souligne la faible efficacité des mesures de restriction isolées, sans accompagnement par d’autres stratégies, par exemple de formation des professionnels de santé, et d’information et de sensibilisation des patients.
Les actions de formation et d’information auprès des professionnels ou de la population sont développées pour limiter l’abus ou le mésusage de médicaments psychotropes. De nombreuses publications rapportent principalement l’évaluation d’expériences de formation et de sensibilisation des pharmaciens d’officine en Amérique du Nord, Australie, Europe (Royaume-Uni). Ces études soulignent le rôle clé de ces professionnels pour la délivrance des médicaments d’automédication et les médicaments de substitution aux opiacés. Du côté des prescripteurs, les interventions proposant aux cliniciens des outils tels qu’un contrat de soins ou d’observance (avec ou sans contrôle objectif des consommations de produits et sanction éventuelle pour les patients) semblent présenter des effets positifs, même s’il existe peu de données dans le domaine ambulatoire, lieu majoritaire du détournement des médicaments. Comme pour les pharmaciens, la sensibilisation des prescripteurs conditionne leur adhésion et la réussite des actions proposées.
Enfin, les programmes de prévention en population générale abordant le problème spécifique de l’abus et du détournement d’usage des médicaments sont rares et toujours intégrés dans une approche générale de l’usage problématique de substances psychoactives, qu’elles soient médicamenteuses ou non. Des actions ciblées spécifiquement sur les médicaments psychotropes s’appuyant sur les caractéristiques propres de l’usage, du mésusage, du détournement, de l’abus et de la dépendance à ces médicaments pourraient s’avérer plus efficaces qu’une stratégie globale sur l’ensemble des substances psychoactives.