| |
| Med Sci (Paris). 2002 February; 18(2): 205–209. Published online 2002 February 15. doi: 10.1051/medsci/2002182205.Que “ trafiquent ” les mélanosomes ? Philippe Bahadoran,* Jean-Paul Ortonne, and Robert Ballotti Inserm U. 385, UFR de Médecine, avenue de Valombrose, 06107 Nice Cedex 2, France |
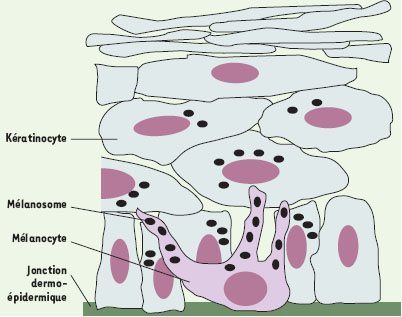
L’épiderme est un épithélium malpighien kératinisé constitué à 90 % de cellules d’origine ectodermique, les kératinocytes. Les mélanocytes sont des cellules originaires de la crête neurale, situées dans la couche basale de l’épiderme dont elles représentent 5 à 10% des cellules. Ce sont ces cellules qui sont responsables de la pigmentation cutanée en synthétisant un pigment, la mélanine. La mélanine est synthétisée et stockée dans des vésicules spécialisées appelées mélanosomes [1, 2]. Les mélanosomes sont des organites morphologiquement et fonctionnellement uniques. Ils ont des caractéristiques communes avec les lysosomes, notamment leur origine endosomale, mais diffèrent de ces derniers par de nombreux aspects, notamment leur fonction secrétoire. A ce titre, ils appartiennent à la famille récemment individualisée des « lysosomes sécrétoires », qui comporte aussi les granules cytotoxiques des lymphocytes (➜), et les corps denses des plaquettes [3]. Les mélanocytes possèdent des prolongements dendritiques leur permettant d’entrer en contact avec plusieurs kératinocytes. Les mélanosomes sont transportés du corps cellulaire où ils sont produits, jus-qu’à l’extrémité des dendrites où ils s’accumulent, puis sont transférés aux kératinocytes adjacents. Ce système de transport intra- puis inter-cellulaire permet donc de délivrer de la mélanine à tous les kératinocytes. Dans les kératinocytes, la mélanine se positionne ensuite en situation supra-nucléaire pour protéger l’ADN contre les effets mutagènes des rayons ultraviolets (Figure 1). 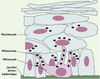 | Figure 1. Interaction mélanocyte/kératinocyte et distribution des mélanosomes dans l’épiderme. Les mélanocytes, situés dans la couche basale de l’épiderme, synthétisent la mélanine dans les mélanosomes. Les mélanosomes sont transportés du corps cellulaire des mélanocytes jusqu’à l’extrémité de leurs dendrites où s’accumulent, puis sont transférés aux kératinocytes. |
(➜) m/s 1995, n°1, p. 99 |
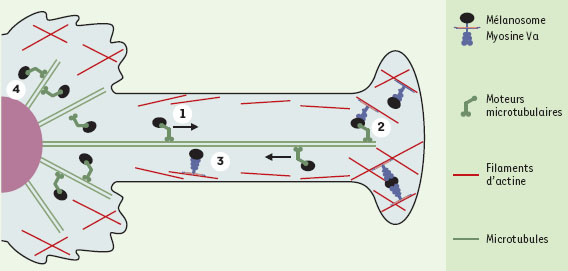
Implication et rôle de la myosine Va dans le transport des mélanosomes L’implication de la myosine Va dans le phénotype de la souris dilute [4] a mis en lumière le rôle de cette molécule dans le transport intracellulaire des mélanosomes. Ces souris, qui présentent une dilution de la couleur de leur pelage en rapport avec un défaut de distribution périphérique des mélanosomes dans les dendrites des mélanocytes [5, 6] et des troubles neurologiques graves, sont homozygotes pour des mutations du gène codant pour la myosine Va (Myova). Des mutations du gène humain (MYOVA), situé en 15q21, sont responsables de la forme cutanéo-neurologique du syndrome de Griscelli-Prunieras dont le phénotype associe, comme celui de la souris dilute, une hypopigmentation en rapport avec un défaut de distribution périphérique des mélanosomes et des troubles neurologiques sévères(➜) [7]. La myosine Va est un moteur moléculaire, dépendant de l’actine, appartenant à la famille des chaînes lourdes de myosine. La partie N-terminale de la myosine Va assure l’activité motrice et la partie C-terminale est responsable de la liaison aux organites transportés [8]. En accord avec les données génétiques et moléculaires précédentes, il a été confirmé que, dans les mélanocytes, la myosine Va est bien un moteur moléculaire des mélanosomes. En effet, il n’y a pas d’accumulation des mélanosomes dans les dendrites des mélanocytes de souris dilute, ni dans ceux de mélanocytes normaux exprimant un mutant “ dominant négatif ” de la myosine Va dépourvu de son domaine d’interaction avec l’actine; de plus, la myosine Va s’associe bien aux mélanosomes [9–12]. Enfin, une étude vidéo-microscopique détaillée réalisée dans des mélanocytes normaux et des mélanocytes dilute dépourvus de myosine Va a conduit à proposer un modèle biphasique pour le transport des mélanosomes dans les mélanocytes : (1) un transport long, entre la région péri-nucléaire et la partie centrale des dendrites, le long des microtubules. Ce transport antérograde par l’intermédiaire de kinésines [12, 13], ou rétrograde par l’intermédiaire de dynéines [14] permettrait aux mélanosomes de circuler dans les dendrites; (2) un transport court, ou peut-être simplement une capture, le long du réseau d’actine sous-corticale, qui permettrait par l’intermédiaire de la myosine Va l’accumulation des mélanosomes à l’extrémité des dendrites [15] (Figure 2). 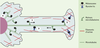 | Figure 2. Modèle hypothétique du transport et de l’accumulation périphérique des mélanosomes. La myosine Va permet de retenir dans le réseau d’actine sous-cortical les mélanosomes délivrés en périphérie par la composante centrifuge du transport microtubulaire (1). Cette rétention se produit surtout à l’extrêmité des dendrites (2), mais également le long des bords latéraux (3). Les mélanosomes se déplacent aussi au centre de la cellule le long du réseau dense de microtubules (4). (schéma adapté d’après [ 11]). |
(➜) m/s 2000, n°6-7, p. 745 |
Implication de Rab27a dans le transport des mélanosomes Récemment, une autre molécule appartenant à la famille des petites GTPases de type Rab, Rab27a, a été impliquée dans le transport des mélanosomes. Des mutations du gène humain (RAB27A) sont impliquées dans la forme cutanée et immunologique du syndrome de Griscelli-Prunieras, qui comporte les mêmes anomalies pigmentaires et mélanocytaires que la forme cutanée et neurologique, associées non plus à une atteinte neurologique primitive, mais à des épisodes de lymphohistiocytose hémophagocytaire [16](➜). Des mutations de ce même gène (Rab27a) ont été trouvées chez la souris ashen [17], qui présente les mêmes anomalies pigmentaires et mélanocytaires que la souris dilute [18], une anomalie des lymphocytes cytotoxiques [19, 20], sans atteinte neurologique. L’anomalie observée dans les mélanocytes des patients et des souris ashen est une accumulation des mélanosomes autour du noyau, et non plus dans les dendrites comme dans les mélanocytes normaux. De plus, dans les deux cas, la réintroduction par transfection de la forme sauvage de Rab27a permet de rétablir l’accumulation des mélanosomes à l’extrémité des dendrites, établissant ainsi le rôle clé de Rab27a dans ce processus [21, 22]. Inversement, l’expression dans des mélanocytes normaux d’un mutant « dominant négatif » de Rab27a produit le même phénotype que celui des souris ashen [23]. (➜) m/s 2000, n°6-7, p. 745 |
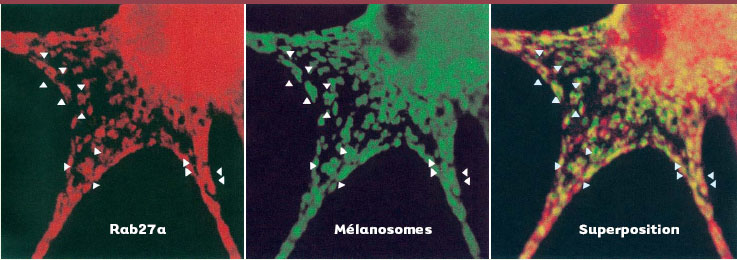
Rôle de Rab27a dans le transport des mélanosomes et interaction Rab27a-myosine Va Les protéines Rab forment la plus large famille au sein de la super famille des petites GTPases Ras. Ce sont elles qui contrôlent le trafic vésiculaire intracellulaire et il semble que la plupart des protéines Rab ont une localisation sub-cellulaire spécifique et, par conséquent, qu’elles contrôlent des étapes spécifiques de ce trafic. Les fonctions les mieux caractérisées des protéines Rab dans le trafic vésiculaire se situent au niveau de la biogenèse, de l’adressage, et de la fusion de vésicules entre des compartiments cellulaires donneurs et receveurs de membranes. Toutefois, des études récentes suggèrent que les protéines Rab pourraient aussi régler les interactions entre les vésicules et certains éléments du cytosquelette, notamment les moteurs moléculaires [24]. La similitude des phénotypes pigmentaires induits indifféremment par les mutations de MyoVa et Rab27a suggérait que dans les mélanocytes, Rab27a et la myosine Va agissent dans une même voie. Rab27a pourrait faire le lien entre les mélanosomes et la myosine Va. En effet, il a été montré que Rab27a d’une part s’associe aux mélanosomes, et d’autre part interagit avec la myosine Va (Figure 3) [21–23]. Dans les mélanocytes des souris ashen, qui sont dépourvus de protéine Rab27a, la myosine Va n’est plus localisée avec les mélanosomes ; tandis que dans les mélanocytes de souris dilute, en l’absence de myosine Va, Rab27a co-localise toujours avec les mélanosomes [22, 23]. Ceci suggère que Rab27a est nécessaire pour recruter la myosine Va sur les mélanosomes (Figure 4).  | Figure 3. Rab27a (en rouge) et les mélanosomes (en vert) sont co-localisés (en jaune) dans les mélanocytes humains. |
|
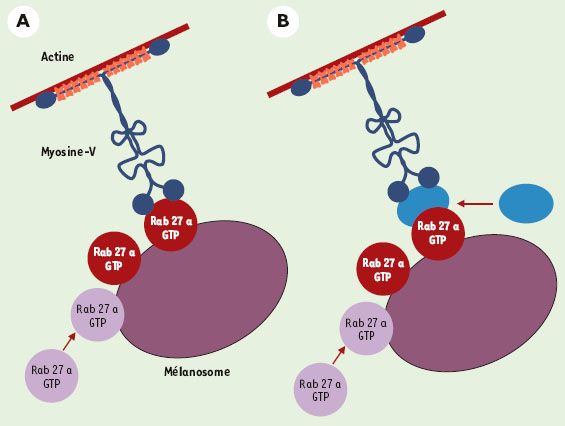
Rôles de la myosine Va et de Rab27a en dehors des mélanocytes Dans les neurones déficients en myosine Va, il existe un défaut de transport du réticulum endoplasmique granuleux dans les dendrites [8]. Rab27a ne semblait pas impliqué dans ce processus dans la mesure où les patients ayant des mutations de ce gène, et les souris ashen, n’ont pas d’anomalies neurologiques [25]. En accord avec ces observations, Rab27a n’est pas exprimé dans les cellules nerveuses [26]. Comme il existe un épissage alternatif du transcrit de la myosine Va aboutissant à l’expression d’isoformes différentes selon les types cellulaires [8], on peut supposer que la myosine Va n’a pas, dans les neurones, les mêmes partenaires moléculaires que dans les mélanocytes. Dans les lymphocytes cytotoxiques déficients en Rab27a, il existe un défaut d’exocytose des granules cytotoxiques. La myosine Va ne semblait pas impliquée dans ce processus dans la mesure où les patients ayant des mutations de ce gène, ainsi que les souris dilute , n’ont pas d’anomalies immunologiques [25]. De plus, dans les lymphocytes cytotoxiques déficients en myosine Va, il n’y a pas de défaut de cytotoxicité [8, 20]. Il est donc possible que Rab27a ait pour partenaire un autre moteur moléculaire que la myosine Va pour transporter les granules cytotoxiques, ou que Rab27a agisse sur une autre étape du transport qui ne nécessite pas la myosine Va, comme la fusion des granules cytotoxiques à la membrane plasmique. 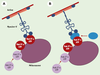 | Figure 4. Rôle hypothétique de Rab27a dans le transport distal des mélanosomes. Rab27a pourrait être le récepteur de la myosine Va à la surface des mélanosomes (A), ou pourrait recruter un effecteur qui lierait la myosine Va (B). |
|
Il reste à déterminer si Rab27a est la molécule qui lie directement la myosine Va, ce qui serait le premier exemple d’une interaction directe entre une petite GTPase Rab et un moteur moléculaire de type myosine. Alternativement, Rab27a pourrait permettre le recrutement à la surface des mélanosomes de molécules effectrices qui pourraient à leur tour assurer la liaison avec la myosine Va. Il existe, en plus des souris dilute et ashen, une troisième hypomélanose murine comportant un blocage du transport distal des mélanosomes, la souris leaden [5, 6]. Or, il vient d’être montré que des mutations d’un nouveau gène, appelé Mlph sont responsables de ce phénotype. Mlph code pour une protéine appelée mélanophiline [27], qui présente des homologies avec des protéines effectrices de Rab connues comme Rabphilin-3A. Il paraît donc probable que la mélanophiline soit un effecteur de Rab27a, et il reste maintenant à déterminer sa fonction dans le transport distal des mélanosomes. Enfin, on attend l’identification, sans doute dans un proche avenir, du gène muté chez la souris, dilute suppressor (dsu) qui ne présente pas de phénotype particulier, mais qui est capable de complémenter les souris dilute, ashen, et leaden. |
Les nombreuses connaissances acquises en quelques années, et les questions de plus en plus ciblées que ces connaissances ont engendrées, laissent augurer des progrès rapides dans la compréhension du transport distal, dépendant de l’actine, des mélanosomes. Il reste à espérer que les autres étapes du transport des mélanosomes, c’est-à-dire le transport proximal dépendant des microtubules, et le transfert dans les kératinocytes, pour lesquelles les connaissances sont beaucoup plus limitées, pourront bénéficier à leur tour de progrès aussi spectaculaires. |
1. Raposo G, Tenza D, Murphy D, Berson J, Marks M. Distinct protein sorting and localization to premelanosomes, melanosomes and lysosomes in pigmented cells. J Cell Biol 2001 : 143; 809–23. 2. Bertolotto C, Busca R, Ballotti R, Ortonne JP. L’AMP cyclique est un régulateur de la pigmentation de la peau. Med Sci 2001; 17 : 177–85. 3. Marks MS, Seabra MC. The melanosome: membrane dynamics in black and white. Nat Rev Mol Cell Biol 2001; 2 : 738–48. 4. Mercer G, Seperack P, Strobel M, Copeland N, Jenkins N. Novel myosin heavy chain encoded by murine dilute coat color locus. Nature 1992; 349 : 709–13. 5. Silvers WK. Dilute and leaden, the p-locus, ruby-eye, and ruby-eye-2. In: Silvers WK, ed. The coat colors of mice. New York : Springer-Verlag, 1979 : 83–104. 6. Provance D, Wei M, Ipe V, Mercer JA. Cultured melanocytes from dilute mutant mice exhibit dendritic morphology and altered melanosome distribution. Proc Natl Acad Sci USA 1996; 93 : 14554–8. 7. Pastural E, Barrat FJ, Dufourcq-Lagelouse R, et al. Griscelli disease maps to chromosome15q21 and is associated with mutations in the myosine-Va gene. Nat Genet 1997; 16 : 289–92. 8. Reck-Peterson S, Provance W, Mooseker M, Mercer J. Class V myosins. Biochim Biophys Acta 2000; 1496 : 36–51. 9. Wu X, Bowers B, Wei Q, Kocher B, Hammer J. Myosin V associates with melanosomes in mouse melanocytes: evidence that myosin V is an organelle motor. J Cell Sci 1997; 110 : 847–59. 10. Nascimento A, Amaral R, Bizario J, Larson R, Espreafico E. Subcellular localization of myosin-V in the B16 melanoma cells, a wild type cell line for the dilute gene. Mol Biol Cell 1997; 8 : 1971–88. 11. Lambert J, Onderwater J, Van der Haeghen Y, et al. Myosin V colocalizes with melanosomes and subcortical actin bundles not associated with stress fibers in human epidermal melanocytes. J Invest Dermatol 1998; 111 : 835–40. 12. Vancoillie G, Lambert J, Mulder A, et al. Kinesin and kinectin can associate with the melanosomal surface and form a link with microtubules in normal human melanocytes. J Invest Dermatol 2000; 114 : 421–9. 13. Hara M, Yaar M, Byers HR, et al. Kinesin participates in melanosomal movement along melanocyte dendrites. J Invest Dermatol 2000; 114 : 438–43. 14. Byers HR, Yaar M, Eller MS, Jalbert NL, Gilchrest BA. Role of cytoplasmic dynein in melanosome transport in human melanocytes. J Invest Dermatol 2000; 114 : 990–7. 15. Wu X, Bowers B, Rao K, Wei Q, Hammer J. Visualization of melanosome dynamics within Wild-type and dilute melanocytes suggests a paradigm for myosin V function in vivo. J Cell Biol 1998; 143 : 1899–918. 16. Menasché G, Pastural E, Feldmann J, et al. Mutations in RAB27A cause Griscelli syndrome associated with hemophagocytic syndrome. Nat Genet 2000; 25 : 173–6. 17. Wilson S, Yip R, Swing D, et al. A mutation in Rab27a causes the vesicle transport observed in ashen mice. Proc Natl Acad Sci USA 2000; 97 : 7933–8. 18. Silvers WK. Beige, silver, greying with age, and other determinants. In: Silvers WK, ed. The coat colors of mice. New York : Springer-Verlag, 1979 : 125–138. 19. Stinchcombe J, Barral D, Mules E, et al. Rab27a is required for regulated secretion in cytotoxic T-lymphocytes. J Cell Biol 2001; 152 : 825–33. 20. Haddad E, Xufeng W, Hammer J, Henkart P. Defective granule exocytosis in Rab27adeficient lymphocytes from ashen mice. J Cell Biol 2001; 152 : 835–41. 21. Bahadoran P, Aberdam E, Mantoux F, et al. Rab27a: a key to melanosome transport in human melanocytes. J Cell Biol 2001; 152 : 843–9. 22. Wu X, Rao K, Bowers B, Copeland N, Jenkins N, Hammer J. Rab27a enables myosin Va-dependent melanosome capture by recruiting the myosin to the organelle. J Cell Sci 2001; 114 : 1091–100. 23. Hume A, Collinson L, Rapak A, Gommes A, Hopkins C, Seabra M. Rab27a regulates the peripheral distribution of melanosomes in melanocytes. J Cell Biol 2001; 152 : 795–808. 24. Segev N. Ypt and Rab GTPases: insight into functions through novel interactions. J Cell Sci 2001; 13 : 500–11. 25. Bahadoran P, Ballotti R, Ortonne JP, de Saint-Basile G. Comment on Elejalde Syndrome and relationship with Griscelli syndrome. Am J Med Genet 2002 (sous presse).
26.
Chen D, Guo J, Miki T, Tachibana M, Gahl G. Molecular cloning and characterization of Rab27a and Rab27b, novel human proteins shared by melanocytes and platelets. Biochem Mol Med 1997; 60 : 27–37. 27. Matesic LE, Yip R, Reuss AE, et al. Mutations in Mlph, encoding a member of the Rab effector family, cause the melanosome transport defects observed in ashen mice. Proc Natl Acad Sci USA 2001; 98 : 10238–43. |