L’hématopoïèse qui se développe dans les corps embryonnaires (EB) dérivés des cellules souches embryonnaires (cellules ES) de souris récapitule l’hématopoïèse embryonnaire du sac vitellin. Comme les cellules souches du sac vitellin, les cellules hématopoïétiques dérivées des cellules ES ont longtemps été considérées comme incapables de reconstituer à long terme le tissu hématopoïétique d’une souris irradiée, incompétence attribuée soit à l’immaturité de ces cellules, soit à des anomalies dans leur adressage à la moelle osseuse [1, 2]. Les tentatives ont toujours donné lieu à des reconstitutions lymphoïdes et/ou myéloïdes partielles et éphémères [1–4]. En aucun cas, une reconstitution hématopoïétique de receveurs secondaires par la moelle des receveurs primaires n’a été observée. Cela signe l’absence, ou la faible concentration, dans la moelle primaire, de cellules primitives répondant aux critères de définition de la cellule souche hématopoïétique (CSH), autorenouvellement et multipotentialité.
Les mécanismes moléculaires contrôlant le passage de l’hématopoïèse primitive à l’hématopoïèse définitive sont très mal connus. On sait cependant que plusieurs homéogènes sont exprimés dans les CSH définitives, à l’inverse de celles du sac vitellin. Il s’agit de HoxB3, B4, A4 et A5 [5]. Ainsi, HoxB4 apparaissait comme un bon candidat pour promouvoir l’hématopoïèse définitive. On savait par ailleurs que : (1) l’introduction d’HoxB4 dans la moelle osseuse adulte induit une stimulation de la capacité de repopulation de cette dernière sans interférer avec la différenciation [6] ; (2) HoxB4 est impliqué dans l’autorenouvellement des CSH définitives [6] ; (3) HoxB4 stimule la production de colonies hématopoïétiques mixtes (contenant des cellules de plusieurs lignées) à partir des cellules ES [7]. Une étude parue au mois d’avril 2002 dans la revue Cell montre que l’expression ectopique du gène HoxB4 dans les cellules ES, associée à leur co-culture avec une lignée stromale, induit la commutation de l’hématopoïèse primitive dérivée de cellules ES à l’hématopoïèse définitive et permet la reconstitution lympho-myéloïde à long terme de receveurs primaires et secondaires [8]. Les cellules du sac vitellin acquièrent les mêmes propriétés en subissant le même traitement.
L’expression d’HoxB4 dans les cellules de sacs vitellins prélevés avant la mise en circulation du sang (stade E8,25) est obtenue à l’aide d’un rétrovirus co-exprimant la GFP, protéine fluorescente qui permet la sélection des cellules infectées, puis leur identification et leur tri dans la moelle des souris receveuses. Une phase de culture des cellules transduites avec la lignée stromale murine Op9, qui permet le développement des progéniteurs hématopoïétiques dérivés des cellules ES [9] est introduite dans le protocole avant injection à des souris adultes irradiées létalement. Ces receveurs présentent une reconstitution myélo-lymphoïde de type donneur (GFP+) importante : 15, 34, 26 et 5 % de cellules de moelle sont respectivement Gr1+ (granuleux), Mac-1+ (macrophages), B220+ (lymphocytes B) et CD8+ (lymphocytes T). La moelle de ces receveurs primaires est capable de reconstituer des receveurs secondaires jusqu’à cinq mois au moins après la greffe : à ce stade, le sang périphérique de ces derniers contient, parmi les cellules dérivées de la moelle primaire (GFP+), 80 % de cellules positives pour GR-1, 8 % pour B220 et 9 % pour CD4 ou CD8. L’expression d’HoxB4 dans les précurseurs primitifs du sac vitellin induit donc un potentiel de CSH définitives.
L’expression d’HoxB4 au cours de la différenciation des cellules ES a été réalisée grâce à l’introduction dans les cellules ES d’un transgène dans lequel la séquence d’HoxB4 est placée sous le contrôle d’un promoteur inductible par la doxycycline (Figure 1). L’expression d’HoxB4 est induite au 4e jour de différenciation des cellules ES en corps embryonnaires et ceci pendant 48 heures. Cette période de différenciation a été choisie car elle correspond probablement à l’étape au cours de laquelle l’hémangioblaste dérivé des cellules ES (→) s’engage dans la différenciation vers la CSH primitive. La culture en méthylcellulose des cellules d’EB à l’issue de la période de surexpression du gène HoxB4 montre que celle-ci induit une stimulation très marquée des progéniteurs les plus primitifs détectables par ce test, les CFU-GEMM (colony-forming unit granulocyte-erythroid-macrophage-megakaryocyte), alors que les CFU-GEMM produites par les cellules d’EB non transfectées sont rares et ont un potentiel érythroïde très limité. Les colonies dérivées des EB exprimant HoxB4 sont, comme celles de la moelle, de plus grande taille, très denses et majoritairement érythroïdes. Les cellules d’EBs sont ensuite cultivées sur la lignée Op9 en présence de cytokines et en maintenant l’induction d’HoxB4 par la doxycycline. Des colonies semi-adhérentes de type blastique se développent, majoritairement composées de cellules exprimant des marqueurs caractéristiques de la CSH définitive, c-kit (81 % des cellules) et CD31 (78 %). Une plus faible proportion de cellules exprime les marqueurs de différenciation macrophagique (Mac-1 : 21 %) et granulocytaire (Gr-1 : 6 %). Les marqueurs érythroïde (Ter119) et lymphocytaire (B220) sont encore plus minoritaires (0,7 et 0,6 %). La culture des cellules surexprimant HoxB4 aboutit donc à la formation d’une population de CSH primitives qui semblent s’autorenouveler mais se différencier. Cette population, peu analysée par RT-PCR, exprime la globine β majeure, suggérant que l’expression d’HoxB4 et la lignée Op9 éteignent l’érythropoïèse embryonnaire. Un autre élément important est l’activation de l’expression du récepteur de la chimiokine SDF-1, CXCR-4, dont la présence est requise pour l’adressage des cellules souches à la moelle osseuse [9, 10] et celle du gène Tel, impliquée dans la transition de l’hématopoïèse du foie fœtal à celle de la moelle osseuse [11] prouvant que l’expression d’HoxB4, combinée à une phase d’expansion cellulaire sur la lignée Op9, confère l’apparition des marqueurs de l’hématopoïèse définitive à des cellules dérivées de cellules embryonnaires. La capacité des cellules ES de reconstituer l’hématopoïèse à long terme, prouvant la présence de CSH primitives, est clairement montrée. Cinq à 32 % de cellules d’origine du greffon (GFP+) sont retrouvées dans la moelle des receveurs irradiés 2 semaines après la greffe. Quinze semaines plus tard, une reconstitution substantielle de tous les lignages est observée : reconstitution myéloïde GR-1+(71 %), Mac-1, et lymphoïde (B220+ : 30 %, CD4+ : 22 % et CD8+ : 5 %). Les marqueurs des CSH, c-kit, Sca-1 et AA4-1 sont aussi détectés sur les cellules GFP+ de la moelle des receveurs. L’induction d’HoxB4 in vivo n’est pas nécessaire pour obtenir la prise de greffe, suggérant que l’expression d’HoxB4 pendant la phase de culture suffit à conférer le potentiel de reconstitution de l’hématopoïèse définitive aux cellules dérivées des cellules ES. Ces cellules ont la capacité de reconstituer des receveurs secondaires pendant au moins 5 mois, montrant sans aucune ambiguïté que l’induction transitoire d’HoxB4 dans les cellules dérivées des cellules ES a permis l’émergence d’une CSH dotée de la potentialité de reconstituer l’hématopoïèse adulte. On ne sait pas aujourd’hui si HoxB4 détermine l’acquisition de cette potentialité chez l’embryon. De même, compte tenu de la redondance des gènes, il est possible que d’autres gènes de la famille Hox, notamment HoxA4, soient capables de provoquer l’émergence de la CSH définitive. Néanmoins, les résultats convaincants que décrit cet article sont de première importance dans le contexte de l’aptitude des cellules ES humaines à se différencier en cellules hématopoïétiques [12] et de l’intérêt croissant pour la thérapie cellulaire en médecine réparatrice. Il faut enfin signaler que ce modèle a permis la correction d’une anomalie génétique de la souris en combinant transplantation nucléaire, thérapie génique et cellulaire [13] (→→).
(→) m/s 1999, n°2, p. 292
(→→) m/s 2002, n°6-7, p. 651
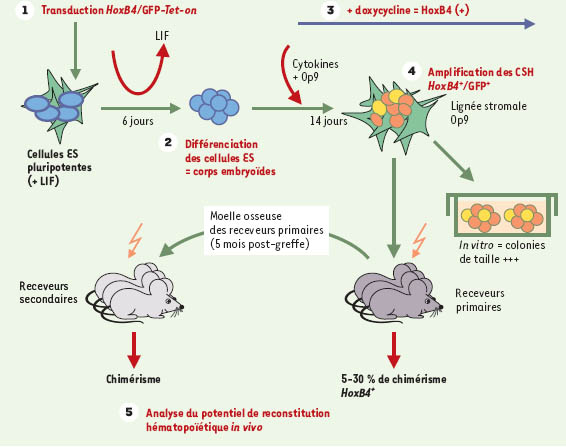
| Figure 1.
Induction d’un potentiel de cellule souche hématopoïétique définitive dans les cellules ES. Les cellules ES, maintenues à l’état pluripotent en présence d’une source de LIF (leukemia inhibiting factor), sont transduites avec un rétrovirus codant pour HoxB4 sous contrôle d’un promoteur inductible par la doxocycline. Les cellules ES sont sevrées de LIF, ce qui entraîne leur différenciation en corps embryoïdes. Ceux-ci sont exposés 48 heures à la doxocycline pour induire HoxB4 et transférés pendant 14 jours en présence de cytokines et de la lignée stromale Op9. L’ajout de doxocycline est prolongé. Le potentiel des cellules obtenues après cette phase d’amplification cellulaire est analysé in vitro (test de colonies) et in vivo dans un système de transplantation hématopoïétique à des receveurs irradiés. La moelle et le sang des receveurs sont analysés pour la présence de cellules d’origine de donneur, et la moelle est injectée à des receveurs secondaires irradiés afin de tester la présence, chez le receveur primaire, de cellules souches hématopoïétiques. Il faut noter que l’ajout de doxocycline n’est pas maintenu in vivo, mais est limité aux 14 jours de culture in vitro. |