En transplantation, d’importants progrès ont été notés depuis la commercialisation des inhibiteurs de la calcineurine (ICN). Les ICN (ciclosporine A et tacrolimus) réduisent l’activation des lymphocytes T alloréactifs (LT) en inhibant le premier signal d’activation, calcium-dépendant. Malheureusement, les ICN ont une toxicité rénale importante [ 1]. En effet, les malades transplantés d’organes autres que le rein (foie, cœur, intestin, poumon…) développent une insuffisance rénale chronique (IRC) après une dizaine d’années de traitement [ 2]. En transplantation rénale, les lésions liées à l’utilisation des ICN sont également observées et sont responsables fréquemment de la perte du greffon. L’enjeu actuel est de réduire, voire d’arrêter les ICN. Les nouvelles approches reposent sur la compréhension des mécanismes d’activation des LT et la mise en évidence du second signal d’activation du LT (Figure 1). Cette voie d’activation est nécessaire, mais non suffisante pour l’activation du lymphocyte T, et vient compléter les signaux transmis lors du premier signal. Ce second signal est principalement sous la dépendance de CD28 qui interagit avec deux protéines, CD80 et CD86, exprimées à la surface de la cellule présentatrice d’antigène [ 3]. L’absence du second signal rend le LT anergique. Au cours de l’activation lymphocytaire, un mécanisme de rétrocontrôle négatif est secondairement produit. Il implique la protéine CTLA4, synthétisée secondairement à l’activation par les LT, dont le domaine extracellulaire est homologue à CD28. CTLA4 interagit, avec une avidité supérieure à CD28, avec CD80/86. CTLA4 transmet alors un signal négatif au LT, permettant l’inhibition de la réponse immune. Une nouvelle stratégie est de bloquer le deuxième signal d’activation lymphocytaire en produisant une protéine recombinante humaine composée du domaine extracellulaire de CTLA4 conjugué aux domaines constants d’une IgG1 (CTLA4-Ig) [3] (Figure 2). Deux mutations ponctuelles dans le domaine extracellulaire de CTLA4 ont été identifiées permettant une meilleure avidité pour CD80/86. La protéine recombinante engendrée (Belatacept®) diminue in vitro la prolifération lymphocytaire [3] en dissociant l’interaction CD28-CD80/86. In vivo, dans différents modèles murins, un traitement par CTLA4-Ig associé à un anticorps dirigé contre CD40L induit la survie illimitée des greffons [ 4– 6]. Chez les primates non humains, Belatacept® réduit la survenue de rejet aigu de greffon allogénique et augmente la durée de vie du greffon [ 7, 8].
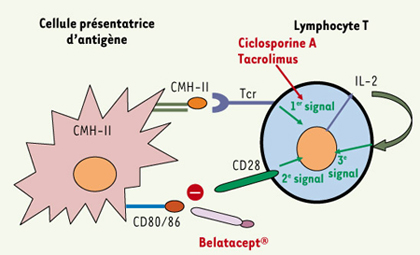
| Figure 1.
Activation des lymphocytes T. Le premier signal d’activation dépend de l’interaction des molécules de classe II (CMH-II) de la cellule présentatrice d’antigène avec le récepteur T (Tcr) du lymphocyte T CD4 positif. Ce premier signal induit une pré-activation du lymphocyte T via un flux calcique et l’activation de la phosphatase, la calcineurine. Ce premier signal est partiellement inhibé par la ciclosporine A et le tacrolimus. Le second signal ou signal de co-activation est nécessaire pour l’activation du lymphocyte T et dépend de l’interaction de CD80/86 avec la molécule CD28. Cette interaction peut être inhibée par la molécule recombinante (Belatacept®). Lors d’une activation complète (1er et 2e signaux), le lymphocyte T synthétise de nombreuses cytokines dont l’IL-2 qui a une action autocrine (3e signal) et permet l’expansion clonale des lymphocytes T. |
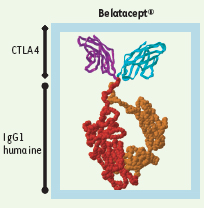
| Figure 2.
Représentation schématique du Belatacept®. L’extrémité amino-terminale est composée de l’ectodomaine de CTLA4, dans lequel deux mutations ponctuelles ont été introduites pour augmenter son avidité pour CD80/86, et la partie carboxy-terminale des deux domaines constants d’une immunoglobuline G1 humaine. La protéine représentée est un dimère de 2 chaînes. |
Une étude originale de phase II multicentrique randomisée (22 centres, États-Unis, Canada, Europe) a été menée chez 228 malades recevant une greffe rénale [ 9]. Les malades étaient randomisés en trois groupes. Le groupe I (GI) était traité par ciclosporine (n = 73) ; le groupe II (GII) par Belatacept® à dose élevée (n = 71), et le groupe III (GIII) par Belatacept® à plus faible dose (n = 73). Seuls les malades du GI recevaient un ICN. Les malades des groupes GII et GIII n’avaient pas d’ICN et étaient traités pour la première fois par un inhibiteur du second signal. L’ensemble des malades recevait un traitement par mycophénolate mofétil et corticoïdes. Après randomisation, la population était identique dans les trois groupes. L’incidence des rejets aigus a été comparable dans les trois groupes (GI = 8 %, GII = 7 %, GIII = 6 %) de même que celle des rejets aigus cortico-résistants. Les rejets infracliniques (prouvés histologiquement sans modification de la créatinémie à un an) étaient cependant plus fréquents dans le groupe Belatacept® faible dose (20 %) (GIII) que dans le groupe Belatacept® forte dose (9 %) ou ciclosporine (11 %). En revanche, la fonction rénale était significativement meilleure dans les groupes traités par Belatacept® que dans le groupe traité ciclosporine. De plus, la survenue d’une néphropathie chronique était plus rare chez les malades traités par Belatacept® que dans le groupe traité par ciclosporine (GI 44 %, GII 29 %, GIII 20 %). Le traitement par Belatacept® réduit également les facteurs de risque cardiovasculaire associés à la transplantation. À un an, le taux de cholestérol total et de LDL cholestérol était identique dans les trois groupes mais les malades traités par Belatacept® consommaient moins d’hypolipémiants (GI 53 %, GII 36 %, GIII 32 %, p = 0,003). La pression artérielle systolique était plus élevée dans le groupe traité par ciclosporine que dans les deux groupes traités par Belatacept®. En revanche, la fréquence de complications infectieuses et cancéreuses était identique dans les trois groupes. Cette étude montre pour la première fois que Belatacept® est aussi efficace que la ciclosporine pour la prévention du rejet aigu et que cette molécule améliore la fonction rénale, réduit la néphropathie chronique du greffon et les facteurs de risque cardiovasculaires sans induire plus de complications infectieuses. Cette molécule ouvre donc de nombreux espoirs en transplantation et devrait être associée à un allongement de la survie des greffons. En raison de sa moindre toxicité rénale, elle devrait pouvoir être choisie lorsque des greffons rénaux sub-optimaux sont utilisés et permettre également de réduire l’incidence d’IRC chez les malades ayant une transplantation d’un autre organe. Son indication ne se limite pas à la prévention des rejets de greffes. Le Belatacept® ou une molécule homologue (CTLA4-Ig) pourra être utilisée pour le traitement de maladies auto-immunes. Enfin, ce traitement administré par perfusion mensuelle devrait faciliter l’observance thérapeutique et limiter le risque d’oubli des médicaments immunosuppresseurs fréquemment associé à des échecs de la greffe.