| |
| Med Sci (Paris). 2007 April; 23(4): 409–416. Published online 2007 April 15. doi: 10.1051/medsci/2007234409.Recommandations et politiques vaccinales
mondiales : le rôle de l’OMS Philippe Duclos1* and Jean-Marie Okwo-Bele2* 1Senior Health Adviser 2Director, Immunization, Vaccines and Biologicals, World Health Organization, 20, avenue Appia, CH-1211 Geneva 27, Suisse |
La vaccination, comme les progrès en matière d’hygiène et d’assainissement, a révolutionné la santé de l’enfant dans le monde en évitant des millions de décès depuis le lancement par l’OMS en 1974 du Programme élargi de vaccination (PEV). La variole a été éradiquée en 1979 et, à ce jour, la poliomyélite a déjà été éliminée dans la majorité des pays [
1]. Cependant, tous les enfants ne bénéficient pas pleinement des avantages de la vaccination. Dans nombre de pays en développement, l’accès aux services assurant les vaccinations n’est pas le même que dans les pays plus riches. Parfois, le manque d’engagement politique et la précarité des systèmes de santé en sont la cause. Les enfants les plus pauvres ont généralement accès à un éventail plus réduit de vaccins. Selon les évaluations de l’OMS et de l’UNICEF en 2005, au moins 28 millions de nourrissons n’avaient pas été vaccinés avec trois doses de vaccin DTC (diphtérie, tétanos, coqueluche) malgré une couverture globale de 78 % [
2]. Nous faisons le point dans cet article sur le rôle normatif de l’OMS au niveau mondial en matière de vaccins, son importance, ses limites et les changements afférents survenus au cours des dernières années et ceux à venir. Des informations plus complètes sur les mécanismes consultatifs incluant les attributs des principaux comités, les produits et recommandations de l’OMS sont disponibles sur le site Web de l’OMS (http://www.who.int/immunization/en/). |
Mandat et objectifs de l’OMS : défis et évolution des besoins Rôle et mandat de l’OMS L’OMS est l’organisme responsable au niveau mondial de l’établissement de standards et de la formulation de politiques et de recommandations pour les vaccins et la vaccination. Le rôle de l’organisation est à la fois reconnu et attendu, et ancré dans sa constitution - signée par les 193 états membres - qui reconnaît l’OMS comme une institution spécialisée (article 57 de la Charte des Nations-Unies) dont l’objectif est d’amener tous les peuples au niveau de santé le plus élevé possible [
3]. L’article 2 de cette constitution indique que dans ce but, l’organisation doit agir en tant qu’autorité directrice et coordonnatrice des travaux qui, dans le domaine de la santé, ont un caractère international ; elle doit établir et maintenir une collaboration effective avec les Nations-Unies, les institutions spécialisées, les administrations gouvernementales de la santé, les groupes professionnels, ainsi que tout autre organisation qui paraîtrait indiquée. Par ailleurs, l’article 2 insiste sur la nécessité : (1) de favoriser la coopération entre les groupes scientifiques et professionnels qui contribuent au progrès de la santé ; (2) de fournir toute information, donner tout conseil et toute assistance dans le domaine de la santé ; (3) d’aider les peuples à acquérir une opinion éclairée en ce qui concerne la santé ; et (4) de développer, établir et encourager l’adoption de normes internationales en ce qui concerne les aliments, les produits biologiques, pharmaceutiques et assimilés. Ces différents points s’appliquent évidemment à la vaccination et requièrent la mise en place d’un système adéquat pour l’établissement de politiques, recommandations, normes et standards en matière de vaccination, fondés sur un consensus établi à partir de preuves scientifiques, de plates-formes de discussion, et d’échanges avec l’industrie et tout autre intervenant que représente l’OMS. Ce rôle est une des priorités stratégiques de l’OMS [
4,
5]. Défis et évolution des besoins Disponibilité des vaccins Avec la création du PEV (programme élargi de vaccination), l’OMS a défini des orientations thématiques en matière de vaccination, destinées aux pays en développement, sur la façon de concevoir, mettre en place et gérer efficacement l’accès aux vaccins indispensables. Ce programme s’est fort justement concentré initialement sur la vaccination des nourrissons et des femmes enceintes, sélectionnant un nombre limité de vaccins alors disponibles (BCG, rougeole, coqueluche, diphtérie, tétanos, poliomyélite) et permettant une rapide amélioration de la couverture vaccinale mondiale. Le but était d’obtenir, grâce aux outils vaccinaux disponibles, l’impact maximal sur la mortalité évitable. L’action menée dans les années 1980 pour instaurer la vaccination universelle des enfants s’est traduite par une hausse rapide de la couverture vaccinale [ 1]. Pendant les années 1990, une couverture vaccinale globale de plus de 70 % a été maintenue avec les vaccins de base du PEV, mais ce succès cachait de grandes disparités entre les pays et à l’intérieur des pays. Si dans certains pays en développement, les taux de vaccination ont sensiblement progressé, ailleurs, notamment en Afrique subsaharienne, ils ont chuté et des millions d’enfants ont ainsi été exposés sans protection à des maladies de l’enfance potentiellement mortelles [ 1]. La dernière décennie a été le témoin de changements considérables dans le domaine des vaccinations. Face aux enjeux d’un monde en pleine mutation et dans lequel les pays deviennent de plus en plus interdépendants, l’OMS et l’UNICEF ont conçu ensemble pour la période 2006-2015 une stratégie intitulée « la vaccination dans le monde : vision et stratégie » [
6]. L’objectif en est de protéger un plus grand nombre de personnes contre davantage de maladies en faisant bénéficier de la vaccination tous ceux qui peuvent y prétendre, et en veillant à ce que la vaccination figure en bonne place dans tous les programmes de santé. L’objectif de cette stratégie est d’augmenter, ou au moins de maintenir, la couverture vaccinale à un niveau très élevé, y compris dans d’autres classes d’âge que celle des nourrissons, à adopter de nouveaux vaccins, et à associer la vaccination à d’autres interventions. La vaccination et les interventions apparentées envisagées dans cette stratégie contribueront dans une large mesure à la réalisation des objectifs du Millénaire pour le développement [
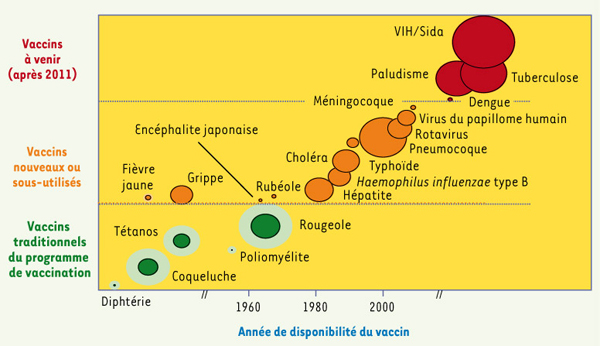
7]. L’élaboration de cette stratégie mondiale a tenu compte de l’augmentation de la demande en vaccins, des progrès rapides dans la mise au point de nouveaux vaccins et de nouvelles technologies, du développement continu du secteur de la santé, de la plus grande vulnérabilité aux pandémies et à d’autres urgences sanitaires, ainsi que des nombreuses possibilités de partenariat. En attendant la mise au point de nouveaux vaccins contre des maladies infectieuses de première importance (VIH/Sida, paludisme et tuberculose), d’autres, qui ciblent d’autres agents pathogènes (rotavirus, pneumocoque, virus du papillome humain), ont déjà été homologués et sont disponibles. D’autres enfin ne sont pas assez utilisés (par exemple contre l’encéphalite japonaise, la fièvre jaune, Haemophilus influenzae type b [Hib]). La Figure 1 (adaptée de [5]) représente de façon imagée la mortalité évitable par l’optimisation de l’utilisation des vaccins existant ou l’introduction de nouveaux vaccins.  | Figure 1.
Impact potentiel estimé des vaccins sur la mortalité. La taille des pastilles schématise approximativement le fardeau comparatif estimé pour 2002 de chacune des maladies listées (à titre d’exemple, le fardeau résiduel estimé de la rougeole était alors de 610 000 décès). Zone vert clair : mortalité évitée. |
Investissement financier L’ensemble des vaccins du PEV utilisés dans le contexte des calendriers recommandés par l’OMS ne coûtait guère plus de 1 dollar. Le coût d’une seule dose du vaccin Hib, malgré sa diminution importante, est encore de plus de deux dollars. Quant au coût des nouveaux vaccins distribués dans les pays industrialisés, il excède 100 dollars par dose, alors que le produit national brut (PNB) par habitant des 72 pays éligibles pour le fond de l’Alliance GAVI 1, est de moins de 1000 dollars US (moins de 300 dollars US pour les plus pauvres d’entre eux). Un fossé s’est creusé au fil des ans entre pays pauvres et pays riches en termes d’utilisation des vaccins dans les programmes de routine à mesure qu’ont été commercialisés de nouveaux vaccins susceptibles de sauver des vies - à des prix inabordables pour la plupart des pays à faible revenu [ 1]. Cependant, le coût n’est qu’un aspect du problème car il faut aussi des mécanismes garantissant la viabilité financière à long terme des nouveaux vaccins. Dans certains pays, l’inadéquation des systèmes de surveillance et de déclaration des maladies a entravé l’évaluation de la charge de morbidité et de la rentabilité potentielle des nouveaux vaccins comparée à d’autres priorités de santé publique. Or, une demande initiale faible ou incertaine peut avoir un impact à long terme sur l’offre et sur le prix d’un nouveau vaccin, et dans les pays en développement, face à une demande faible et/ou incertaine, les fabricants limiteront le volume de production en conséquence. Une fois la taille de l’usine décidée, le coût d’une augmentation ultérieure de la production est très important, expliquant le maintien de prix relativement élevés pour de faibles volumes de production [1,
8]. Au cours des 10 prochaines années, les pays se verront proposer un éventail sans précédent de technologies et de vaccins nouveaux pouvant s’intégrer dans les programmes de vaccination. Cela concerne des vaccins contre des maladies pour lesquelles d’autres interventions de santé préventives ou curatives sont disponibles, obligeant les pays à faire un choix. Le manque de connaissances dans les domaines de la sécurité des vaccins et des affaires réglementaires, et les insuffisances des études coût-efficacité de différentes stratégies de vaccination doivent être comblés avant que les pays puissent prendre des décisions rationnelles fondées sur les preuves. Il faudra également décider, à la lumière de données probantes, si la réduction de la morbidité justifie l’investissement financier que représente tel ou tel vaccin et lequel de ces produits constitue le meilleur investissement compte tenu de ressources nationales limitées, en particulier lequel sera le plus facile à intégrer dans les systèmes de vaccination et aura les plus grandes retombées pour la santé publique. Deux nouvelles initiatives de financement, le dispositif international de financement de la vaccination (IFFIm) et les engagements d’achat à terme, viennent s’ajouter aux financements de l’Alliance GAVI et représentent un potentiel d’aide de plusieurs milliards pour le développement, l’achat et l’introduction de nouveaux vaccins [1,
9]. Un processus clair et robuste d’établissement des politiques au niveau mondial permettra de définir les priorités mondiales en termes de développement, d’investissement par les donateurs comme l’Alliance GAVI, et de fabrication pour les firmes, afin de faire porter les efforts sur les produits opportuns. Des manquements à ces niveaux pourraient engendrer des erreurs coûteuses et des retards préjudiciables. |
Objectifs et nature des recommandations émises par l’OMS L’OMS fournit des normes, standards et produits de référence pour la fabrication et le contrôle des vaccins. Ces normes s’adressent aux fabricants, aux autorités nationales de contrôle et servent de base au processus de pré-qualification [
10]. Ce dernier processus est un service fourni par l’OMS à l’UNICEF et aux autres agences des Nations-Unies pour déterminer l’acceptabilité de principe de différents vaccins, qui ensuite pourront faire l’objet d’approvisionnement via ces agences. Le but est de s’assurer de l’innocuité et de l’efficacité de ces vaccins [10]. Les recommandations de l’OMS à propos de l’utilisation des vaccins s’adressent en premier lieu aux gouvernements des états membres et en particulier aux organismes d’état chargés de la prise de décision, de la mise en œuvre des programmes de vaccination, de la surveillance des maladies évitables par la vaccination et de la sécurité et de l’homologation des vaccins, ainsi qu’aux comités consultatifs nationaux. Ces recommandations sont aussi utiles pour aider les donateurs et partenaires principaux d’un programme de vaccination - qu’il s’agisse de l’UNICEF et l’Alliance GAVI, d’organismes à but non lucratif, d’associations professionnelles internationales, et de partenaires bilatéraux ou multilatéraux - à ajuster leurs programmes et leur soutien aux pays incluant l’achat de vaccins. Les recommandations sont aussi utiles à l’industrie pharmaceutique pour établir leur stratégie d’investissement ainsi qu’aux organismes de recherche et au personnel de l’OMS. Ces recommandations peuvent être particulièrement utiles dans le cadre d’une stratégie mondiale - nécessairement coordonnée - de contrôle ou d’éradication des maladies, par exemple pour le programme d’éradication de la poliomyélite ou du tétanos néonatal, ou de l’initiative de réduction de la mortalité due à la rougeole. L’impact de la vaccination est à la fois individuel et collectif par le biais de l’immunité de groupe qui conduit à la protection d’un certain nombre de personnes non vaccinées, voire de la population dans son ensemble, lorsqu’un taux de couverture suffisant (variable d’une maladie à une autre) a été atteint. Les faibles taux de vaccination dans certains pays, et la survenue d’épidémies, mettent en danger les enfants et les adultes non vaccinés de tous les pays. Le développement rapide des voyages internationaux et les mouvements importants de population augmentent les risques de contagion. Conséquence de l’interdépendance sanitaire croissante des pays, l’état de la vaccination dans un pays peut influencer l’incidence d’une maladie dans un autre. Ainsi, au début des années 1990, une crise sanitaire de proportions internationales a été déclarée en Europe orientale, lorsque des faibles taux de vaccination et une crise économique ont entraîné une grave épidémie de diphtérie qui a fait près de 30 000 morts. Avant que l’épidémie n’ait pu être maîtrisée, la maladie avait gagné l’Allemagne, la Finlande, la Norvège et la Pologne [1]. Plus récemment, l’absence de progrès dans la vaccination des enfants contre la poliomyélite dans les quatre derniers pays dans lesquels la maladie sévit à l’état endémique, en particulier au Nigéria, représente une menace pour l’éradication de la poliomyélite. En 2005-2006, le virus polio a été exporté à partir du Nigéria dans 23 pays de la région Africaine mais aussi en Indonésie [9]. Les conclusions et recommandations de l’OMS servent aussi à confirmer la sécurité et l’efficacité des vaccins lorsque la nécessité s’en fait sentir en particulier dans les pays disposant de peu de moyens et où les autorités nationales de contrôle des produits médicamenteux et vaccins ne sont pas encore pleinement fonctionnelles. Les vaccins pouvant désormais être introduits directement dans des pays en développement sans être utilisés dans des pays industrialisés, la mise en place d’outils pour évaluer leur sécurité n’en est que plus importante, particulièrement dans un contexte où les questionnements et allégations relatifs à la sécurité des vaccins abondent. |
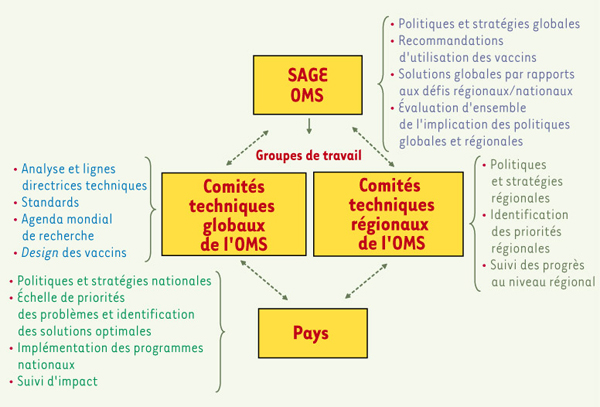
Processus d’élaboration des recommandations Élaboration des recommandations - Défis et processus L’OMS reçoit des recommandations de comités consultatifs externes composés de panels d’experts et de groupes scientifiques de haut niveau d’origine géographique et institutionnelle variée (universités, gouvernements, organismes de recherche…). Les travaux de ces comités sont émis sous forme de recommandations au directeur général de l’OMS ou à son délégué qui utilisent ces informations pour établir les politiques de l’organisation en matière de vaccination. Les experts interviennent en leur nom et non pas en celui du pays ou de l’organisation auxquels ils appartiennent. Les avis de ces organisations et leur contribution sont bien sûr sollicités, mais la prise de décision finale doit rester libre de tout conflit d’intérêt. Pour être efficace cette information doit être compréhensible par les utilisateurs et d’un accès facile. Dans un souci d’ajustement, l’OMS a entrepris une révision des processus à partir desquels ses recommandations sont émises, mettant l’accent sur la nécessaire prise en compte des conflits d’intérêt potentiels, sur l’établissement d’un multiculturalisme et d’une représentation géographique adéquate. L’indépendance par rapport aux donateurs et aux fonctions de sensibilisation de l’organisation, et la transparence du processus de décision doivent aussi être garanties. L’un des défis essentiels est la rapidité de mise en place des processus et de la diffusion des recommandations et conclusions afin d’éviter tout retard dans l’utilisation à grande échelle des nouveaux produits et de permettre l’ajustement rapide des programmes en fonction des besoins. Un autre défi est d’assurer la coordination des politiques vaccinales de l’OMS dans le cadre plus large des autres interventions préventives possibles et des politiques de lutte contre les maladies. Cela devrait être le cas par exemple pour la vaccination contre le virus du papillome humain et la vaccination à venir contre le paludisme. Cadre pour le développement des politiques Au niveau mondial, l’OMS fournit des recommandations via trois principaux groupes génériques : (1) le groupe stratégique consultatif d’experts sur la vaccination (SAGE) ; (2) le comité consultatif mondial de la sécurité vaccinale (GACVS) ; et (3) le comité d’experts de la standardisation biologique (ECBS) ( voir plus loin la description de ces instances). D’autres groupes techniques plus spécifiques évoluent aussi au sein de l’OMS ; certains sont pérennes, d’autres sont des comités ad hoc ponctuels. Un autre comité, l’Advisory Forum de l’initiative de l’OMS/UNAIDS pour la recherche vaccinale, a en particulier pour but de revoir la stratégie de recherche d’un point de vue scientifique et technique et de définir des priorités. De plus, un groupe consultatif technique régional existe pour chacune des six régions de l’OMS - Afrique, Amériques, Méditerranée orientale, Europe, Asie du Sud-Est et Pacifique occidental. Ils ont pour mission d’émettre des avis techniques relatifs aux priorités et aux stratégies de vaccination prenant en compte les spécificités épidémiologiques et sociales régionales. Ces avis sont transmis aux directeurs régionaux de l’OMS auxquels incombe l’adaptation des politiques et recommandations mondiales au niveau régional. La Figure 2 présente le cadre fonctionnel des comités consultatifs.  | Figure 2.
Cadre fonctionnel des comités consultatifs en matière de vaccination.
|
|
Principaux groupes consultatifs de l’OMS dans le domaine normatif SAGE (Strategic Advisory Group of Experts) Établi en 1999, SAGE est le groupe consultatif principal de l’OMS en matière de vaccination. Il fournit des recommandations au Directeur général dans des domaines allant de la recherche et du développement à l’administration des vaccins et à l’articulation avec les autres interventions de santé. SAGE a été récemment ajusté en fonction des besoins suscités par l’établissement de la « nouvelle vision et stratégie en matière de vaccination » de l’OMS citée ci-dessus [ 6], et son domaine de compétence s’étend, au-delà de la vaccination de l’enfant, à tous les groupes d’âge et à toutes les maladies évitables par la vaccination [
11]. Il fonde son travail sur des revues systématiques menées par des groupes d’experts scientifiques et techniques. Les débats sont ouverts aux partenaires et aux observateurs et les conclusions et recommandations du groupe sont rapidement publiées (en français et en anglais) dans le relevé épidémiologique hebdomadaire de l’OMS (WER, weekly epidemiologic report), et sur le site Web sur lequel apparaissent aussi les attributs et règles de fonctionnement du groupe SAGE http://www.who.int/immunization/sage/en/index.html. Comité d’experts de la standardisation biologique Établi en 1947, l’ECBS établit des normes et critères mondiaux qui contribuent à garantir la qualité des vaccins et autres produits biologiques. Les normes sont rédigées à l’issue d’un processus mondial de concertation. Le comité met au point et diffuse également des préparations de référence, étalons valables à l’échelle mondiale qui servent de références aux fabricants et aux autorités responsables de la réglementation. Ces préparations sont utilisées pour calibrer les standards régionaux et nationaux ou ceux des fabricants et forment souvent la base du processus d’homologation et de libération des lots. Le laboratoire international de standardisation biologique situé au National Institute for Biological Standards and Control (NIBSC) au Royaume-Uni sert de laboratoire de référence à l’OMS pour établir ces préparations de référence [ 9]. Historiquement, les standards étaient établis une fois le nouveau vaccin homologué, mais dans le contexte actuel, ECBS doit opérer de manière plus proactive, et à un stade initial du cycle de production. Les recommandations de l’ECBS sont publiées dans le WHO Technical Report Series ( http://www.who.int/biologicals/publications/trs/areas/vaccines/en/index.html). Plus d’informations sur le comité sont également disponibles à l’adresse suivante : http://www.who.int/biologicals/expert_committee/en/. Le Comité consultatif mondial de la sécurité vaccinale Le GACVS a été établi en 1999 pour réagir rapidement aux problèmes de sécurité vaccinale pouvant avoir un impact mondial. Il donne un avis scientifique en matière de sécurité qui peut susciter une révision des politiques de vaccination mais il n’établit pas directement ces politiques [
12,
13]. Le Comité effectue cette évaluation scientifique des questions de sécurité vaccinale en procédant à un examen rigoureux des connaissances les plus actuelles dans les domaines des sciences fondamentales, de l’épidémiologie et de la pratique clinique. Tous les aspects de la sécurité vaccinale sont envisagés, qu’ils soient d’intérêt national ou mondial, et ce en étroite collaboration avec toutes les parties intéressées, notamment les spécialistes des administrations nationales, des établissements d’enseignement et du secteur pharmaceutique. Le comité a la possibilité de demander, contrôler et évaluer la mise en place d’études spécifiques visant à explorer un lien supposé entre des vaccins ou leur composants et des manifestations indésirables. La neutralité du groupe est essentielle et explique que sa mission soit distincte de celle du SAGE. Ainsi, le Comité a tantôt conclu que les allégations concernant la nocivité de certains vaccins étaient infondées, tantôt reconnu sans hésiter, quand elle était réelle, l’association entre un vaccin et une manifestation indésirable [ 9]. Outre les rapports publiés dans le Relevé Épidémiologique Hebdomadaire, l’accent a été mis sur la mise à disposition d’informations sur le site Web où figurent les conclusions du comité sur l’ensemble des sujets dont il a traité ( http://www.who.int/vaccine_safety/fr/index.html). |
Notes de synthèse sur les vaccins L’OMS publie des notes de synthèse régulièrement mises à jour sur les vaccins et les associations vaccinales importantes pour la santé publique internationale, et utilisés dans les programmes de vaccination à grande échelle. Ces notes synthétisent les informations de base disponibles sur les maladies et leurs vaccins et informent de la position actuelle de l’OMS concernant l’utilisation de ces vaccins dans le contexte mondial. Ces documents font l’objet d’un important processus de consultation et de révision par divers groupes d’intérêt et experts du domaine au sein et à l’extérieur de l’OMS et, depuis avril 2006, ils sont revus et approuvés par le SAGE [
14]. SAGE participe également à la définition des priorités pour le développement de nouvelles notes de synthèse et leur mise à jour. Ces notes de synthèse sont principalement destinées aux responsables nationaux de la santé publique et aux directeurs des programmes de vaccination. Elles peuvent cependant également intéresser les organismes internationaux de financement, les laboratoires fabriquant les vaccins, la communauté médicale et les médias scientifiques. Les notes d’information sont publiées dans le Relevé Épidémiologique Hebdomadaire et sont disponibles sur le Web (http://www.who.int/immunization/documents/positionpapers_intro/en/index.html). |
Impact des recommandations Mesure de l’impact des recommandations S’il n’est pas facile d’évaluer précisément l’impact des politiques et recommandations de l’OMS dont l’application dépend de facteurs additionnels, celui-ci est cependant indéniable comme en témoignent plusieurs faits. L’adoption des vaccins et calendriers du PEV par un grand nombre de pays en développement et l’extension des programmes de vaccination dans les années 1980 [1] sont peut-être les témoins les plus évidents de l’impact des recommandations globales. Les recommandations globales d’utilisation d’une dose de vaccin anti-rougeoleux dans le cadre d’un programme de vaccination en routine, complétée par une deuxième opportunité de vaccination (dans le cadre de vaccinations de routine ou lors de campagnes de vaccinations supplémentaires à grande échelle), ont permis d’obtenir avec succès une réduction de la mortalité rougeoleuse. Les progrès de cette stratégie viennent récemment d’être salués par la communauté internationale puisque la mortalité due à la rougeole a reculé de 60 % dans le monde depuis 1999 dépassant même l’objectif fixé par les Nations-Unies qui était une réduction de moitié de la mortalité rougeoleuse entre 1999 et 2005 [
15]. Le paysage est moins satisfaisant pour les vaccins d’introduction plus récente. À la fin de 2005, seulement 136 (87 %) des 156 pays en développement ou dont l’économie est en transition, avaient inclus le vaccin anti-hépatite B dans leur calendrier national de vaccination [2] malgré la recommandation de l’OMS plaidant depuis 1991 pour une vaccination universelle, et malgré la disponibilité du vaccin pour les pays riches depuis 1982 [1,
16]. Dans les pays industrialisés, l’usage généralisé depuis plus de 15 ans des vaccins contre Haemophilus influenzae de type b (Hib) a presque éliminé les maladies dues à Hib au cours des dernières années. Malgré une note de synthèse de 1988 recommandant son utilisation [
17], seuls 65 des 156 pays non industrialisés (42 %) avaient adopté ce vaccin à la fin de 2005 [2]. Dans les pays à faible revenu, l’adoption de ces nouveaux vaccins a été grandement facilitée par l’appui reçu récemment de l’Alliance GAVI et du Fonds pour les vaccins. La reconnaissance du fardeau de la maladie dans les pays, les coûts du vaccin, et, dans le cas du vaccin contre l’hépatite B, les craintes d’effets indésirables dont on sait maintenant qu’elles étaient sans fondement, ont limité la progression de l’introduction de ces vaccins. Au vu des données récentes, le SAGE a renforcé la recommandation d’utilisation [11] et le texte actuel de la note de synthèse qui traduit cette recommandation devrait permettre de faciliter le processus d’introduction de ce vaccin : « Compte tenu de leur innocuité et de leur efficacité attestées, les vaccins anti-Hib conjugués devraient faire partie de tous les programmes de vaccination systématique des nourrissons. Le manque de données relatives à la surveillance locale ne devrait pas retarder l’introduction de ces vaccins » [14]. Les recommandations doivent aussi être adaptées à chaque pays, et leur but n’est pas d’œuvrer pour l’harmonisation de principe des calendriers vaccinaux en fixant des calendriers de vaccination rigides, mais de proposer un cadre dont les pays sauront s’accommoder en fonction des calendriers déjà existants et des pratiques et données épidémiologiques locales. Inversement, il est aussi possible de déterminer si des pays vont à l’encontre des recommandations de l’OMS. Un exemple est l’administration de doses de rappels de BCG. Cette pratique n’est pas recommandée par l’OMS [
18], mais continuait fin 2005 d’être utilisée par 22 pays [2], dont 15 en Europe. Un autre exemple est l’arrêt, recommandé par l’OMS, de l’utilisation de la souche ourlienne Rubini pour la vaccination compte tenu de sa faible efficacité [
19]. Au contraire la souche Urabe AM9, bien que son utilisation ait été suspendue dans les pays de l’Union Européenne, continue d’être utilisée avec succès dans les programmes de vaccination de routine d’un certain nombre de pays en développement. Il est probable que sans le soutien des recommandations et compte tenu de la pression médiatique, les vaccins contenant la souche Urabe auraient été abandonnés avec le risque de coupures d’approvisionnements en raison du coût d’autres souches. SAGE a récemment adopté une recommandation préconisant l’utilisation globale du vaccin conjugué heptavalent contre le pneumocoque [9] et une recommandation régionale d’utilisation des deux vaccins nouvellement homologués contre le rotavirus [11]. Ces recommandations ont facilité l’acceptation, par le comité d’administration de l’Alliance GAVI, d’un investissement pour l’achat de ces deux vaccins, ce qui permettra leur utilisation dans les pays les plus pauvres. Certains faits viennent étayer l’impact important des recommandations de l’OMS concernant l’utilisation des normes et standards, bien que cette dernière ne fasse pas l’objet d’un suivi étroit. Les lignes directrices sur l’utilisation des substrats cellulaires ont été adoptées par la conférence internationale sur l’harmonisation comme faisant partie du processus d’homologation [
20]. Des lignes directrices relatives au bio-confinement des vaccins antigrippaux, et finalisées récemment [
21], sont déjà en voie d’application dans sept pays. Les recommandations de l’ECBS pour la production et le contrôle des vaccins antirabiques, excluant ceux qui seraient produits à partir de tissus nerveux de mammifères [21], ont eu un impact majeur, même si certains vaccins sont encore produits sur des encéphales de moutons. Il faut aussi noter que dans le cadre de l’initiative globale de réduction de la mortalité due à la rougeole, les standards de l’OMS et le processus de pré-qualification dans son ensemble ont permis de mettre des vaccins efficaces et sans danger à la disposition des pays dans lesquels la mortalité rougeoleuse est la plus importante, et dont les autorités nationales n’étaient pas à même d’assurer les contrôles nécessaires. Toutes les recommandations n’ont pas la même utilité ni le même impact dans tous les pays. Ainsi les pays industrialisés disposant de processus élaborés et adaptés à leur situation pour la mise en place de recommandations vaccinales prêteront moins d’attention aux notes de synthèse, mais seront en revanche demandeurs de connaître la position du GACVS sur des questions de sécurité. C’est alors surtout la neutralité et la crédibilité de l’OMS qui sont recherchées. À ce titre, les énoncés du GACVS sont de plus en plus cités comme référence et utilisés pour combattre les rumeurs et ils font l’objet d’une utilisation directe par les autorités de contrôle y compris dans les pays industrialisés [
22]. Améliorer la communication pour améliorer l’impact L’utilisation des recommandations (SAGE et notes d’information de l’OMS publiées dans le WER, relevé épidémiologique hebdomadaire) par les pays dépend non seulement de leur crédibilité mais bien sûr de leur accessibilité. Une enquête récente (non publiée) réalisée auprès d’un groupe de décideurs dans les domaines de la vaccination indique qu’au maximum 12 % d’entre eux avaient eu accès à certaines des notes de synthèse et rapports du GACVS ou du SAGE. Une évaluation externe des comités a, elle aussi, révélé des lacunes en termes d’accessibilité et de diffusion de l’information sur les recommandations de l’OMS. L’amélioration de la communication des politiques de l’OMS apparaît donc comme une priorité essentielle. C’est dans ce but qu’œuvre le département des vaccins et produits biologiques en prenant en compte les besoins (par exemple des efforts de traduction) et en utilisant les méthodes les plus efficaces de dissémination de l’information. Ainsi, les rapports de SAGE et du GACVS, ainsi que les notes de synthèse sur les vaccins seront traduits dans les six langues officielles de l’OMS (arabe, chinois, anglais, français, russe et espagnol). |
Les auteurs tiennent à remercier les collègues du Département de l’immunisation vaccins et produits biologiques de l’OMS pour leur contribution, et tout particulièrement Alison Brunier et Mario Condé pour leurs conseils dans la rédaction du manuscrit.
|
Footnotes |
7. Le Fonds des Nations Unies pour l’enfance (UNICEF). The States of the World’s Children 2006. New York : UNICEF, 2005 : 144 p. ISBN 13 : 978-92-806-3917-9. www.unicef.org/sowc06/
9. Réunion du Groupe stratégique consultative d’experts sur la vaccination. Genève, novembre 2006 : conclusions et recommandations. Weekly Epidemiol Rec 2007; 82 : 1–16. 10. Procedure for assessing the acceptability, in principle, of vaccines for purchase by the United Nations agencies. Geneva : immunization, vaccines and biologicals. Geneva : World Health Organization, 2006. WHO/IVB/05.19. www.who.int/vaccines-documents/DocsPDF06/812.pdf
11. Conclusions et recommandations du Groupe stratégique d’experts sur la vaccination. Weekly Epidemiol Rec 2006; 81 : 1–12. 12. Folb PI, Bernatowska E, Chen R, et al. A global perspective on vaccine safety and public health : the global advisory committee on vaccine safety. Am J Pub Health 2004; 94 : 1926–31. 13. Comité consultatif mondial de la sécurité vaccinale, 29-30 novembre 2006. Weekly Epidemiol Rec 2007; 82 : 18–24 14. Note de synthèse. Position de l’OMS sur les vaccins conjugués anti-Haemophilus influenzae type b. Weekly Epidemiol Rec 2006; 81 : 445–52. 15. Wolfson LJ, Strebel PM, Gacic-Dobo M, et al., for the Measles initiative. Has the 2005 measles mortality reduction goal been achieved ? A natural history modelling study. Lancet 2007; 369 : 191–200. 16. Vaccins anti-hépatite B. Note de synthèse : position de l’OMS. Weekly Epidemiol Rec 2004; 79 : 255–63. 17. Programme mondial des vaccins et vaccinations (GPV). Note de synthèse. Position de l’OMS sur les vaccins conjugués anti-Haemophilus influenzae type b. Weekly Epidemiol Rec 1998; 73 : 64–68. 18. Vaccin BCG. Note de synthèse. Position de l’OMS. Weekly Epidemiol Rec 2004; 79 : 27–38. 19. Vaccins anti-ourliens. Note d’information de l’OMS. Weekly Epidemiol Rec 2001; 76 : 346–55. 20. WHO expert committee on biological standardization. Requirements for the use of animal cells as in vitro substrates for the production of biologicals. Annex 1. WHO Technical Report Series. Geneva : World Health Organization, 1998; 878 : 19–56. 21. WHO expert committee on biological standardization. WHO biosafety guidelines for the production and quality control of human influenza pandemic vaccine strains. WHO Technical Report Series. Geneva : World Health Organization, 2007; 941 (sous presse). 22. WHO expert committee on biological standardization. Recommendations for rabies vaccines. WHO Technical Report Series. Geneva : World Health Organization, 2007; 941 (sous presse). 23. Avis du comité technique des vaccinations et du conseil supérieur d’hygiène publique de France. Section maladies transmissibles concernant la vaccination contre l’hépatite virale B (séance du CTV du 14 septembre 2004) (séance du CSHPF du 26 septembre 2004). http://agmed.sante.gouv.fr/htm/10/hepatite/bhernan.pdf
|