| |
| Med Sci (Paris). 2008 December; 24(12): 1043–1048. Published online 2008 December 15. doi: 10.1051/medsci/200824121043.L’embryogenèse précoce des mammifères Premières différenciations cellulaires et cellules souches Claire Chazaud* GReD (Génétique, Reproduction et Développement), CNRS, UMR 6247, Inserm, U931, Clermont Université, Faculté de médecine, 28, place H. Dunant, BP38, 63001 Clermont-Ferrand, France |
Chez les modèles de vertébrés tels que le poisson-zèbre ou le xénope, des asymétries moléculaires sont déjà observées dans l’œuf fécondé [
49]. Elles vont se transmettre différemment aux cellules filles au cours des divisions et déterminer ainsi leur future identité. Au contraire, chez les mammifères et notamment chez la souris, aucun déterminant cellulaire n’a été localisé de manière asymétrique dans le zygote. D’autres mécanismes interviennent donc pour amorcer les premières différenciations cellulaires. Grâce à l’évolution de techniques plus sensibles et plus résolutives, l’embryon de souris avant son implantation ne mesurant qu’environ cent microns, de nombreuses interactions géniques ont été identifiées ces dernières années, permettant de mieux comprendre les mécanismes de différenciation cellulaire au niveau moléculaire. |
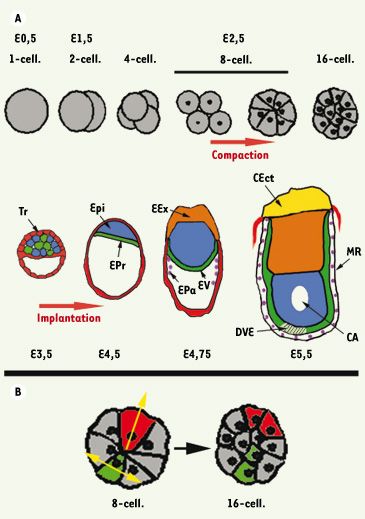
De la fécondation à l’implantation chez la souris : morphologie de l’embryon Après la fécondation, l’œuf, tout en gardant le même volume, se divise en deux, quatre, puis huit cellules - ou blastomères - identiques. Au stade 8 cellules, les blastomères, qui étaient jusqu’alors arrondis et de forme symétrique, se polarisent en renforçant les contacts avec leurs voisins et en applatissant leur surface externe [
1,
2,
50] (Figure 1A). C’est la phase de compaction qui donne à l’embryon une forme de petite mûre appelée morula. Jusqu’à ce stade, les blastomères sont homogènes et ont tous la capacité de donner à la fois des tissus embryonnaires et extra-embryonnaires ; cependant, la compaction va entraîner la production de deux populations de cellules différentes au cours des cycles de division suivants. En effet, une fois polarisées, les cellules vont se diviser soit symétriquement, le long de l’axe interne/externe et donner deux cellules polarisées, soit asymétriquement le long d’un axe perpendiculaire à l’axe interne/externe pour produire une cellule externe polarisée et une cellule interne non polarisée (Figure 1B). Ainsi, au stade 16 cellules, l’embryon est formé de deux types cellulaires différant par leur position interne ou externe. Une nouvelle vague de divisions symétriques et asymétriques conduit au stade de 32 cellules. Des expériences de traçage cellulaire ont montré qu’à partir de ce stade, les cellules externes commencent à acquérir leur identité définitive d’appartenance à la lignée trophoblastique [1]. Après le stade 32 cellules, une cavité se forme à l’intérieur de l’embryon. Ainsi, au stade de blastocyste à 3,5 jours (E3,5), l’embryon est formé d’une couche externe de trophoblastes renfermant la cavité blastocélique et la masse cellulaire interne (MCI). Au cours des heures suivantes, la MCI va produire deux tissus distincts : une masse de cellules formant l’épiblaste (Epi), recouverte d’un épithélium d’endoderme primitif (EPr). Donc, au moment de l’implantation à E4,5 chez la souris, l’embryon est formé de trois tissus : les trophoblastes (Tr) qui participeront plus tard à la formation du placenta, l’EPr qui formera une partie du sac vitellin et l’Epi qui participera à la formation des annexes embryonnaires et produira également toutes les cellules de l’embryon, y compris les cellules germinales qui portent la perpétuation de l’espèce.  | Figure 1.
Chronologie de formation des premières étapes embryonnaires. A. Les différentes étapes de formation de l’embryon de souris du stade 1 cellule (cell.) au stade E5,5. Entre le stade 1 et 4 cell., les embryons sont représentés en entier alors que du stade 8 cell. à E5,5 il sont schématisés sous forme de sections. B. Production de cellules internes ou externes par division asymétrique (vert) ou symétrique (rouge) entre les stades 8 et 16 cellules. CA, cavité amniotique ; CEct, cône ectoplacentaire ; DVE (hachuré), endoderme viscéral distal ; EEx, ectoderme extra-embryonnaire ; EPa, endoderme pariétal ; Epi, épiblaste ; EPr, endoderme primitif ; EV, endoderme viscéral ; MR, membrane de Reichert ; Tr, trophoblastes. |
|
Cellules souches issues du blastocyste Aux trois lignages cellulaires présents à l’implantation, l’Epi, le Tr et l’EPr, correspondent trois modèles in vitro de cellules souches [
3]. Les trois types de cellules souches sont isolés à partir de blastocystes (E3,5). Les plus étudiées sont les cellules souches embryonnaires (ES) qui ont des caractéristiques épiblastiques [
4,
5]. Les cellules souches trophoblastiques (TS) [
6] et Xen [
7] ont été isolées plus récemment et représentent les lignées trophoblastiques et de l’EPr respectivement. Pour chacune de ces trois lignées, le caractère « souche » a été validé par la production d’embryons chimères, c’est-à-dire en greffant ces cellules à des embryons de stade 8 cellules ou à des blastocystes. Les embryons ou les souris adultes analysés par la suite ont montré une colonisation spécifique de chaque lignage cellulaire et ont ainsi permis de démontrer l’identité et le potentiel de chacune de ces lignées de cellules souches in vivo. Les cellules ES sont largement utilisées en transgenèse puisqu’elles peuvent être manipulées génétiquement in vitro pour être réintroduites dans un animal. De nombreux modèles animaux de maladies génétiques humaines ont été produits ainsi [
8]. Le grand intérêt que ces cellules suscitent depuis quelques années a été provoqué par leur isolement chez l’homme [
9], rendant envisageable de nombreuses thérapies cellulaires, puisque ces cellules ont la capacité de se différencier en tous les types cellulaires fœtaux et adultes [
10,
11,
51]. Les cellules souches sont des outils indispensables pour comprendre les propriétés et les mécanismes de différenciation des lignages cellulaires, mais elles possèdent cependant des caractéristiques propres à leur environnement in vitro, divergeant des lignages cellulaires in vivo de l’embryon dont elles sont issues. |
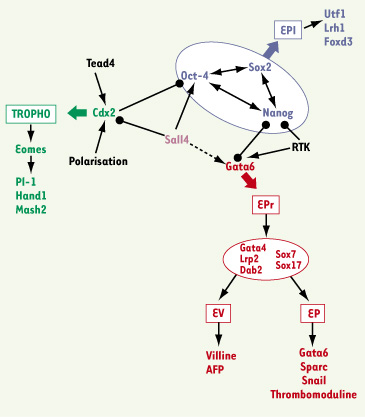
Détermination et différenciation des premières lignées cellulaires Spécification trophoblastes/masse cellulaire interne (MCI) La différenciation des cellules trophoblastiques par rapport à la MCI dépend de leur structure polarisée ainsi que de leur position externe dans l’embryon, qui résultent des divisions symétriques et asymétriques [ 1]. La répartition entre ces cellules est contrôlée par des molécules impliquées dans l’adhésion et/ou la polarité cellulaire : la E-cadhérine, l’Ezrine, des protéines Par ou certaines isoformes de la PKC (protéine kinase C). L’héritage par les cellules filles de ces molécules au cours des divisions symétriques et asymétriques ainsi que leur localisation baso-latérale ou apicale maintiennent la polarité des cellules externes [ 2, 3]. Par exemple, lorsque l’aPKC ou ParD3, exprimées au pôle apical des cellules polarisées, sont inactivées dans certaines cellules, ces cellules ont tendance à se localiser à l’intérieur de l’embryon [
12]. Ces protéines impliquées dans la polarité cellulaire influencent donc la position de la cellule dans l’embryon, mais cependant ne lui donnent pas une identité définitive. L’identité trophoblastique est fixée entre les stades 32 et 64 cellules (début de la formation du blastocyste) et peut être visualisée grâce à l’expression sélective du facteur de transcription Cdx2 dans les cellules externes [
13–
16]. À l’inverse, celle des gènes de pluripotence tels que Oct-4, Sox2 et Nanog est restreinte aux cellules internes du blastocyste. Il est intéressant de noter que ces protéines, spécifiques soit des trophoblastes, soit de la MCI, sont co-exprimées dans tous les blastomères jusqu’au stade 16 cellules, montrant la complexité des mécanismes de régulation. L’analyse des embryons mutants pour Cdx2 a ainsi montré que ce facteur de transcription est requis pour le maintien de l’identité des trophoblastes, et qu’il réprime des gènes spécifiques de la MCI tels que Oct-4 ou Nanog [13,
14] (Figure 2). Les mécanismes de cette répression ont été clarifiés in vitro ; elle résulte de la liaison d’un complexe répresseur Oct-4/Cdx2 au promoteur d’Oct-4 dans les cellules trophoblastiques [16].  | Figure 2.
Spécification cellulaire dans l’embryon. Interactions génétiques intervenant dans l’induction des trois lignages cellulaires, l’épiblaste (bleu), les trophoblastes (vert) et l’endoderme primitif (rouge). Les informations sont basées sur des résultats obtenus avec des embryons ou des cellules souches. Les inductions sont représentées par des flèches alors que les inhibitions sont représentées par des ronds. Les cercles symbolisent des groupes de gènes qui agissent ensemble sur des gènes cibles. |
En revanche, Cdx2 n’a aucune influence sur la position ou la polarité des cellules lors de la formation du blastocyste. En effet, les embryons mutants pour Cdx2 peuvent former des cellules polarisées externes qui ont les caractéristiques morphologiques des trophoblastes jusqu’au début de la formation du blastocyste. Des résultats récents ont mis en évidence que la restriction de l’expression de Cdx2 dans les cellules externes de la morula tardive (une vingtaine de cellules) serait une conséquence de la polarisation des cellules [14,
15]. Ainsi, Cdx2 ne serait induit que dans les cellules externes. Aussi, il a été montré que le facteur de transcription TEAD4 est requis pour l’induction de Cdx2 dès le stade de morula. L’invalidation de Tead4 produit un phénotype plus sévère que celui produit par l’invalidation de Cdx2, puique les embryons Tead4−/−
ne forment pas de blastocyste [
17,
18]. Néanmoins, l’expression de Tead4 est ubiquitaire pendant la préimplantation et doit donc être combinée à d’autres signaux issus de la polarisation des cellules pour induire Cdx2. Ainsi, les cellules de la MCI seraient spécifiées d’abord par l’absence d’expression de facteurs trophoblastiques, notament de Cdx2. L’identité de la MCI est caractérisée par l’expression de facteurs de transcription exprimés dans toutes les cellules internes du blastocyste, comme Oct-4 ou Sox2. Ces protéines sont impliquées dans le maintien de l’identité épiblastique puisque leur élimination provoque une transdétermination des cellules qui adoptent un destin trophoblastique [3] (Figure 2). De même, le facteur Sall4, de la famille des Spalt, est enrichi dans la MCI [
19] et son inactivation induit l’expression de Cdx2 dans la MCI [
20]. Chez la drosophile, Spalt est impliqué dans la polarisation puis la différenciation cellulaires [
21] et il serait intéressant de déterminer si le rôle de Sall4 dans la détermination de la MCI est directement lié à la polarisation cellulaire et/ou aux divisions asymétriques. |
Spécification précoce en épiblaste et endoderme primitif Hétérogénéité des cellules de la MCI La différenciation entre l’Epi et l’EPr est morphologiquement visible au jour 4,5 sous la forme d’un épithélium à l’interface de la cavité blastocélique et des cellules plus internes, formant désormais l’Epi (Figure 1A). Des expériences récentes ont montré que les cellules précurseurs de l’EPr proviennent non seulement de la surface mais aussi de l’intérieur de la MCI. En effet, il a été montré in situ que la MCI d’un blastocyste de 3,5 jours est composée de cellules exprimant soit Nanog, marqueur de l’Epi [
22,
23], soit Gata6, marqueur de l’EPr [
24,
25], mélangées en « poivre et sel » [
26]. Ces résultats ont été confirmés par l’analyse de banques d’ADNc produites à partir de cellules uniques de la MCI montrant qu’il existe deux catégories de cellules exprimant des gènes différents [
27]. Différentes expériences de traçage cellulaire ont montré qu’une cellule de la MCI à E3,5 est déjà déterminée en Epi ou en EPr [ 26]. Ainsi l’ensemble de ces travaux met en évidence que la MCI d’un blastocyste de 3,5 jours n’est pas homogène mais est déjà composée de précurseurs épiblastiques (pré-Epi) et de précurseurs endodermiques (pré-EPr). Dans l’embryon, ces deux lignages cellulaires sont définitivement séparés, alors qu’il est possible de différencier in vitro des cellules ES en cellules EPr, notamment lors de la formation de corps embryonnaires. Mécanismes de spécification en épiblaste et endoderme primitif Les mécanismes d’induction de ces deux lignées cellulaires restent inconnus bien que des expériences réalisées à partir d’embryons et de cellules ES commencent à en élucider les processus (Figure 2). La surexpression des gènes Gata4 ou Gata6 dans les cellules ES induit leur différenciation en EPr [
28,
29], montrant que ces gènes ont un impact fort dans l’induction de ce lignage. Dans ces expériences, l’expression des marqueurs de pluripotence diminue rapidement, suggérant des mécanismes de répression active. De plus, dans les embryons mutants pour la protéine Grb2, un adaptateur de la voie de signalisation des récepteurs à activité tyrosine-kinase (RTK), Gata6, n’est pas exprimé alors que Nanog est présente dans toutes les cellules de la MCI [26]. Ainsi, toutes les cellules de la MCI ont une identité épiblastique, montrant que la voie des RTK est requise pour l’induction de l’EPr, soit en activant Gata6 soit en inhibant Nanog. À l’inverse, les embryons mutants pour Nanog semblent ne donner que des cellules endodermiques [23] ; toutefois, ces mutants ont été analysés longtemps après la formation du blastocyste et des expériences réalisées à des stades plus précoces (E3,5) seront nécessaires. L’analyse de l’inactivation de Nanog dans les cellules ES révèle que ce gène n’est pas absolument nécessaire au maintien de ces cellules dans leur état pluripotent mais serait plutôt requis pour induire l’identité initiale de ces cellules [
30]. L’ensemble de ces résultats montre que la voie de signalisation RTK, couplée à Gata6, et Nanog ont des effets antagonistes et réciproques. Cependant, les mécanismes d’induction et de régulation de l’expression de Nanog et Gata6 ne sont pas aussi simples puisque ces protéines sont coexprimées dans l’ensemble des blastomères entre le stade 8 cellules et celui de la formation du blastocyste (C.C., F. Gerbe et S. Frankenberg, résultats non publiés). La voie de signalisation RTK responsable de l’activation de l’EPr semblerait être celle du FGF (fibroblast growth factor) étant donné que les embryons mutants pour FGF4 ou certains de ses récepteurs ne forment pas d’EPr [
31,
32]. Cependant, d’autres RTK sont présents au niveau de l’EPr comme le PDGFRa (platelet derived growth factor receptor a) [27,
33] et leur implication reste à élucider. Des études sur la différenciation des cellules EC (issues de carcinome embryonnaire et proches des cellules ES) et des cellules ES ont mis en évidence un rôle des gènes Sox dans la formation de l’EPr et de ses dérivés. Sox7 serait en amont de la cascade d’induction et activerait Gata6 [
34], alors que Sox17 serait en aval et permettrait la transition de l’EPr en endoderme viscéral et en endoderme pariétal [
35]. Néanmoins, aucun phénotype n’a été décrit avant l’implantation dans les embryons mutants. Le gène Sall4, impliqué dans la ségrégation trophoblastes/MCI est aussi requis au niveau de l’Epr, mais sa place dans la cascade d’induction des lignages cellulaires n’a pas été déterminée [19, 20]. D’autres facteurs tels que LRH-1, UTF-1, Notchless ou FoxD3 [
36–
39] sont requis dans l’Epi et les cellules ES mais interviendraient plutôt dans le maintien de l’état pluripotent et non dans son induction, et préviendraient une différenciation trop hâtive en tissu neural ou mésendodermique. |
Formation de l’épithélium de l’EPr Les cellules pré-Epi et pré-EPr sont mélangées en « poivre et sel » dans la MCI à E3,5 [3,
40]. Un jour plus tard, ces types cellulaires forment deux tissus bien séparés, l’épithélium de l’EPr recouvrant la masse de cellules épiblastiques. Le tri de ces cellules pourrait s’effectuer de manière active, impliquant une migration de certaines cellules, ou de manière passive grâce à des capacités d’adhésion différentes, les deux mécanismes pouvant être combinés. Les embryons mutants pour la Maspine (Serpinb5), une protéine impliquée dans la migration cellulaire et exprimée dans les dérivés de l’EPr, meurent au moment de l’implantation et l’on observe une dégénérescence de la MCI [
41]. L’analyse des corps embryonnaires Maspine−/− révèle que les cellules pré-EPr sont présentes puisqu’elles expriment Gata4. En revanche, ces cellules ne sont pas positionnées à la périphérie comme le sont celles des embryons sauvages mais disposées en « poivre et sel » [41], montrant que les cellules exprimant Gata4 n’ont pas pu atteindre la surface. Des phénotypes identiques ont été observés lorsque Dab2 [
42–
44] ou le gène codant pour la chaine γ1 de la laminine 111 (LamC1) [
45] sont inactivés. Dab2 est une protéine adaptatrice se liant, entre autres, aux intégrines qui sont des récepteurs des laminines. L’ensemble de ces résultats montre que des molécules impliquées dans l’adhésion et la migration cellulaires sont requises pour que les cellules pré-Epi et pré-EPr segrègent en deux tissus séparés. Les cellules déterminées en EPr non seulement ségrègent de l’Epi, mais vont aussi former un épithélium. Cet épithélium a très tôt une activité d’absorption pour alimenter l’épiblaste sous-jacent [
46,
47], possiblement dès sa formation. Or, à E3,5, les cellules pré-EPr commencent à se préparer à leur nouvelle fonction avant d’atteindre la surface de la cavité blastocélique. En effet, LRP2, un récepteur membranaire pour un grand nombre de ligands (lipoprotéines, protéases, plasminogène, albumine…) est exprimé dans certaines cellules pré-EPr à E3,5 [33]. Le nombre de cellules pré-EPr exprimant LRP2 augmente au cours des heures suivantes, témoin d’une maturation progressive des pré-EPr, sachant que toutes les cellules de l’EPr l’expriment à E4,5. La localisation sub-cellulaire de la protéine est aussi corrélée au degré de maturité de la cellule ainsi qu’à sa position. LRP2 est stockée à l’intérieur de la cellule, probablement dans le Golgi, lorsque la cellule est interne à la MCI, puis elle migre au pôle apical du futur épithélium lorsque la cellule a atteint la surface de la cavité blastocélique [33]. Cette localisation serait sous le contrôle de Dab2 [
43], qui est aussi exprimée au pôle apical des cellules, bordant la cavité blastocélique. Ainsi, la cellule prépare et stocke les protéines nécessaires à l’endocytose de nutriments, ou à la formation de la structure épithéliale comme le collagène IV, pour être prête et fonctionnelle le plus tôt possible. Il est intéressant d’observer que les cellules de l’EPr se polarisent dès qu’elles atteignent la surface et ce individuellement. D’autres travaux seront nécessaires pour déterminer comment les autres cellules vont s’intercaler à la surface et amorcer la formation de jonctions épithéliales avec leurs voisines déjà positionnées et polarisées. |
Ces dernières années, on a assisté à de grandes avancées dans la compréhension des mécanismes moléculaires régulant la différenciation des trois premiers lignages cellulaires de l’embryon. Néanmoins, de nombreuses questions restent en suspens concernant par exemple les mécanismes de restriction de l’expression de Cdx2 dans les cellules externes, ou les mécanismes qui conduisent à l’induction exclusive de Nanog et Gata6 dans la MCI. On ne sait pas non plus si les cellules de l’Epi et de l’EPr ont un précurseur commun distinct de la lignée trophoblastique, ou si la spécification des trois lignées cellulaires se produit simultanément. Par ailleurs, les régulations épigénétiques n’ont pas été abordées dans cette revue mais de plus en plus de travaux démontrent leur implication dans le maintien ou la différenciation des cellules, notament dans les cellules pluripotentes ES. La particularité de la régulation épigénétique des tissus extraembryonnaires (trophoblastes et EPr) (hypométhylation de l’ADN, inactivation du X paternel…) font de l’embryon précoce un outil d’étude excellent [51,
52]. Il faut aussi noter que de plus en plus d’indices montrent que l’induction des axes de l’embryon (antéro-postérieur, dorso-ventral) surviendrait autour du stade de l’implantation et dépendrait d’interactions entre les trois lignages cellulaires [
48]. Plus généralement, l’embryon produit deux épithéliums au cours de la préimplantation, mais met en jeu des mécanismes différents pour recruter les cellules épithéliales. Les trophoblastes sont induits grâce à leur position externe dans l’embryon, alors que les cellules de l’EPr sont d’abord induites avant de se positionner à la surface de la MCI. Ainsi, la compréhension des mécanismes fondamentaux contrôlant d’une part la formation d’épithélium et, d’autre part, la détermination cellulaire, apportera des réponses dans de nombreux domaines de la biologie. |
Merci à Bertrand Pain, Vincent Mirouse et Jean-Louis Couderc pour leurs commentaires sur le manuscrit et à Corinne Belville pour son aide sur la Figure 1A.
|
1. Johnson MH, McConnell JM. Lineage allocation and cell polarity during mouse embryogenesis. Semin Cell Dev Biol 2004; 15 : 583–97. 2. Dard N, Breuer M, Maro B, et al. Morphogenesis of the mammalian blastocyst. Mol Cell Endocrinol 2008; 282 : 70–7. 3. Yamanaka Y, Ralston A, Stephenson RO, et al. Cell and molecular regulation of the mouse blastocyst. Dev Dyn 2006; 235 : 2301–14. 4. Evans MJ, Kaufman MH. Establishment in culture of pluripotential cells from mouse embryos. Nature 1981; 292 : 154–6. 5. Martin GR. Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells. Proc Natl Acad Sci USA 1981; 78 : 7634–8. 6. Tanaka S, Kunath T, Hadjantonakis AK, et al. Promotion of trophoblast stem cell proliferation by FGF4. Science 1998; 282 : 2072–5. 7. Kunath T, Arnaud D, Uy GD, et al. Imprinted X-inactivation in extra-embryonic endoderm cell lines from mouse blastocysts. Development 2005; 132 : 1649–61. 8. Cohen-Tannoudji M. Prix Nobel de médecine 2007 à Mario Capecchi, Martin Evans et Oliver Smithies. Des souris mutantes à façon. Med Sci (Paris) 2007; 23 : 1159–61. 9. Thomson JA, Itskovitz-Eldor J, Shapiro SS, et al. Embryonic stem cell lines derived from human blastocysts. Science 1998; 282 : 1145–7. 10. Keller G. Embryonic stem cell differentiation: emergence of a new era in biology and medicine. Genes Dev 2005; 19 : 1129–55. 11. Peschanski M. Cellules souches : l’heure venue du changement d’Échelle. Med Sci (Paris) 2008; 24 : 335–8. 12. Plusa B, Frankenberg S, Chalmers A, et al. Downregulation of Par3 and aPKC function directs cells towards the ICM in the preimplantation mouse embryo. J Cell Sci 2005; 118 : 505–15. 13. Strumpf D, Mao CA, Yamanaka Y, et al. Cdx2 is required for correct cell fate specification and differentiation of trophectoderm in the mouse blastocyst. Development 2005; 132 : 2093–102. 14. Ralston A, Rossant J. Cdx2 acts downstream of cell polarization to cell-autonomously promote trophectoderm fate in the early mouse embryo. Dev Biol 2008; 313 : 614–29. 15. Dietrich JE, Hiiragi T. Stochastic patterning in the mouse pre-implantation embryo. Development 2007; 134 : 4219–31. 16. Niwa H, Toyooka Y, Shimosato D, et al. Interaction between Oct3/4 and Cdx2 determines trophectoderm differentiation. Cell 2005; 123 : 917–29. 17. Yagi R, Kohn MJ, Karavanova I, et al. Transcription factor TEAD4 specifies the trophectoderm lineage at the beginning of mammalian development. Development 2007; 134 : 3827–36. 18. Nishioka N, Yamamoto S, Kiyonari H, et al. Tead4 is required for specification of trophectoderm in pre-implantation mouse embryos. Mech Dev 2008; 125 : 270–83. 19. Elling U, Klasen C, Eisenberger T, et al. Murine inner cell mass-derived lineages depend on Sall4 function. Proc Natl Acad Sci USA 2006; 103 : 16319–24. 20. Zhang J, Tam WL, Tong GQ, et al. Sall4 modulates embryonic stem cell pluripotency and early embryonic development by the transcriptional regulation of Pou5f1. Nat Cell Biol 2006; 8 : 1114–23. 21. Domingos PM, Mlodzik M, Mendes CS, et al. Spalt transcription factors are required for R3/R4 specification and establishment of planar cell polarity in the Drosophila eye. Development 2004; 131 : 5695–702. 22. Chambers I, Colby D, Robertson M, et al. Functional expression cloning of Nanog, a pluripotency sustaining factor in embryonic stem cells. Cell 2003; 113 : 643–55. 23. Mitsui K, Tokuzawa Y, Itoh H, et al. The homeoprotein Nanog is required for maintenance of pluripotency in mouse epiblast and ES cells. Cell 2003; 113 : 631–42. 24. Koutsourakis M, Langeveld A, Patient R, et al. The transcription factor GATA6 is essential for early extraembryonic development. Development 1999; 126 : 723–32. 25. Morrisey EE, Tang Z, Sigrist K, et al. GATA6 regulates HNF4 and is required for differentiation of visceral endoderm in the mouse embryo. Genes Dev 1998; 12 : 3579–90. 26. Chazaud C, Yamanaka Y, Pawson T, et al. Early lineage segregation between epiblast and primitive endoderm in mouse blastocysts through the Grb2-MAPK pathway. Dev Cell 2006; 10 : 615–24. 27. Kurimoto K, Yabuta Y, Ohinata Y, et al. An improved single-cell cDNA amplification method for efficient high-density oligonucleotide microarray analysis. Nucleic Acids Res 2006; 34 : e42. 28. Fujikura J, Yamato E, Yonemura S, et al. Differentiation of embryonic stem cells is induced by GATA factors. Genes Dev 2002; 16 : 784–9. 29. Shimosato D, Shiki M, Niwa H. Extra-embryonic endoderm cells derived from ES cells induced by GATA factors acquire the character of XEN cells. BMC Dev Biol 2007; 7 : 80. 30. Chambers I, Silva J, Colby D, et al. Nanog safeguards pluripotency and mediates germline development. Nature 2007; 450 : 1230–4. 31. Feldman B, Poueymirou W, Papaioannou VE, et al. Requirement of FGF-4 for postimplantation mouse development. Science 1995; 267 : 246–9. 32. Arman E, Haffner-Krausz R, Chen Y, et al. Targeted disruption of fibroblast growth factor (FGF) receptor 2 suggests a role for FGF signaling in pregastrulation mammalian development. Proc Natl Acad Sci USA 1998; 95 : 5082–7. 33. Gerbe F, Cox B, Rossant J, et al. Dynamic expression of Lrp2 pathway members reveals progressive epithelial differentiation of primitive endoderm in mouse blastocyst. Dev Biol 2008; 313 : 594–602. 34. Futaki S, Hayashi Y, Emoto T, et al. Sox7 plays crucial roles in parietal endoderm differentiation in F9 embryonal carcinoma cells through regulating Gata-4 and Gata-6 expression. Mol Cell Biol 2004; 24 : 10492–503. 35. Shimoda M, Kanai-Azuma M, Hara K, et al. Sox17 plays a substantial role in late-stage differentiation of the extraembryonic endoderm in vitro. J Cell Sci 2007; 120 : 3859–9. 36. Gu P, Goodwin B, Chung AC, et al. Orphan nuclear receptor LRH-1 is required to maintain Oct4 expression at the epiblast stage of embryonic development. Mol Cell Biol 2005; 25 : 3492–505. 37. Van den Boom V, Kooistra SM, Boesjes M, et al. UTF1 is a chromatin-associated protein involved in ES cell differentiation. J Cell Biol 2007; 178 : 913–24. 38. Cormier S, Le Bras S, Souilhol C, et al. The murine ortholog of notchless, a direct regulator of the notch pathway in Drosophila melanogaster, is essential for survival of inner cell mass cells. Mol Cell Biol 2006; 26 : 3541–9. 39. Hanna LA, Foreman RK, Tarasenko IA, et al. Requirement for Foxd3 in maintaining pluripotent cells of the early mouse embryo. Genes Dev 2002; 16 : 2650–61. 40. Chazaud C, Rossant J. Disruption of early proximodistal patterning and AVE formation in Apc mutants. Development 2006; 133 : 3379–87. 41. Gao F, Shi HY, Daughty C, et al. Maspin plays an essential role in early embryonic development. Development 2004; 131 : 1479–89. 42. Yang DH, Smith ER, Roland IH, et al. Disabled-2 is essential for endodermal cell positioning and structure formation during mouse embryogenesis. Dev Biol 2002; 251 : 27–44. 43. Yang DH, Cai KQ, Roland IH, et al. Disabled-2 is an epithelial surface positioning gene. J Biol Chem 2007; 282 : 13114–22. 44. Rula ME, Cai KQ, Moore R, et al. Cell autonomous sorting and surface positioning in the formation of primitive endoderm in embryoid bodies. Genesis 2007; 45 : 327–38. 45. Smyth N, Vatansever HS, Murray P, et al. Absence of basement membranes after targeting the LAMC1 gene results in embryonic lethality due to failure of endoderm differentiation. J Cell Biol 1999; 144 : 151–60. 46. Assemat E, Vinot S, Gofflot F, et al. Expression and role of cubilin in the internalization of nutrients during the peri-implantation development of the rodent embryo. Biol Reprod 2005; 72 : 1079–86. 47. Maurer ME, Cooper JA. Endocytosis of megalin by visceral endoderm cells requires the Dab2 adaptor protein. J Cell Sci 2005; 118 : 5345–55. 48. Tam PP, Loebel DA. Gene function in mouse embryogenesis: get set for gastrulation. Nat Rev Genet 2007; 8 : 368–81. 49. Prodon F, Prulière G, Chenevert J, Sardet C. Établissement et expression des axes embryonnaires : comparaisons entre différents organismes modèles. Med Sci (Paris) 2004; 20 : 526–38. 50. Collignon J, Perea-Gomez A. Régulation épigénétique de la pluripotence chez l’embryon de souris. Med Sci (Paris) 2007; 23 : 679–81. 51. Fluckiger AC, Dehay C, Savatier P. Cellules souches embryonnaires et thérapies cellulaires du système nerveux. Med Sci (Paris) 2003; 19 : 699–708. 52. Henckel A, Feil R. Asymétrie des génomes parentaux : implications en pathologie. Med Sci (Paris) 2008 24 : 747–52. |