| |
| Med Sci (Paris). 2009 April; 25(4): 391–397. Published online 2009 April 15. doi: 10.1051/medsci/2009254391.Canaux potassiques et physiologie de l’épithélium respiratoire Olivier Bardou, Nguyen Thu Ngan Trinh, and Emmanuelle Brochiero* Centre de recherche, Centre hospitalier de l’Université de Montréal (CRCHUM), Hôtel-Dieu, 3840, St-Urbain, Montréal, Québec H2W 1T8 Canada Département de médecine, Université de Montréal, Montréal, Québec, Canada |
L’épithélium respiratoire recouvre les alvéoles et les voies aériennes, des bronchioles aux fosses nasales. Sa fonction principale est de procéder aux échanges gazeux d’O2 et de CO2. Toutefois, les cellules de l’épithélium respiratoire remplissent plusieurs autres fonctions essentielles dans la physiologie du poumon : elles synthétisent et sécrètent le surfactant [
1], elles forment une barrière contre les agressions extérieures grâce à la fonction des cellules ciliées [
2], et à leur capacité à réparer des lésions épithéliales [
3] ou à participer à la réponse inflammatoire [
4] ; enfin, elles régulent le volume et la composition des fluides recouvrant les voies aériennes et les alvéoles par le transport ionique et liquidien. Dans les voies aériennes, l’équilibre entre la réabsorption de Na+ et la sécrétion de Cl− permet de maintenir un volume périciliaire adéquat à la fonction ciliaire [
5]. Un déséquilibre de ces transports, comme chez les patients atteints de fibrose kystique (Fk), entraîne une réduction du volume périciliaire et un épaississement du mucus favorisant les infections et inflammations chroniques. Dans les alvéoles, la réabsorption de Na+ et de Cl− est essentielle à la clairance des fluides alvéolaires au moment de la naissance ou à la résolution de l’œdème pulmonaire chez l’adulte [
6]. Compte tenu du rôle crucial du transport de Na+ et de Cl− dans la physiologie et les pathologies pulmonaires, les canaux Na+ et Cl− font l’objet de multiples études. En revanche, le rôle des canaux K+ dans la physiologie épithéliale pulmonaire est relativement peu étudié. À ce jour cependant, près de 40 types de canaux K+ y ont été détectés. La fonction physiologique de beaucoup d’entre eux reste inconnue, mais plusieurs semblent participer à des processus essentiels au fonctionnement du système respiratoire. De façon générale, dans les épithéliums, les canaux K+ contrôlent le potentiel de membrane et créent un gradient électrochimique favorable au transport ionique et liquidien. Cette fonction, reconnue depuis longtemps dans le rein, ne commence que depuis peu à susciter un intérêt en physiologie pulmonaire et plus particulièrement dans l’étude des pathologies caractérisées par un dysfonctionnement du transport des ions. D’autre part, ces canaux semblent participer aux phénomènes d’adaptation au niveau d’oxygène ou de défense contre les agressions extérieures. Nous proposons donc ici de faire le point sur l’identité moléculaire des canaux K+ de l’épithélium pulmonaire et de discuter leur rôle physiologique. |
Diversité moléculaire des canaux K + de l’épithélium respiratoire Depuis le clonage en 1987 du gène codant pour le premier canal K+, le gène shaker de la drosophile [
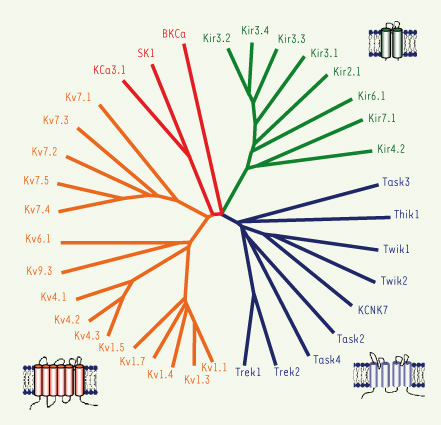
7], plus de 100 canaux K+ différents ont été détectés et regroupés en 3 classes selon leur nombre prédit de segments transmembranaires (STM). La première classe comprend les canaux à 6 STM, elle regroupe les canaux dépendant du voltage (Kv) et activés par le calcium (KCa) ; la seconde comprend les canaux à 4 STM et 2 pores ; la troisième est composée des canaux à 2 STM et rectification entrante (Kir). Dans l’épithélium respiratoire plus de 30 canaux K+ sont exprimés et répartis dans ces 3 classes (Figure 1 et Tableau 1).  | Figure 1.
Arbre phylogénique des canaux K+ de l’épithélium respiratoire. Les séquences en acides aminés des canaux K+ détectés dans les cellules épithéliales des voies aériennes et alvéolaires ont été alignées à l’aide du logiciel ClustalW. L’arbre phylogénique a ensuite été préparé grâce au site http://www.phylogeny.fr/
(«treeviewers », DrawTree). La couleur des branches distingue les différentes classes de canaux K+ : à 2 STM (canaux à rectification entrante, en vert), à 4 STM (canaux à 2 pores, en bleu) et à 6 STM (canaux Kv en orange et KCa en rouge). Les représentations schématiques de la topologie transmembranaire de ces différentes classes sont également représentées. Il faut noter que le canal BKCa, bien que communément intégré parmi les canaux KCa à 6 STM, serait en réalité composé de 7 STM. |
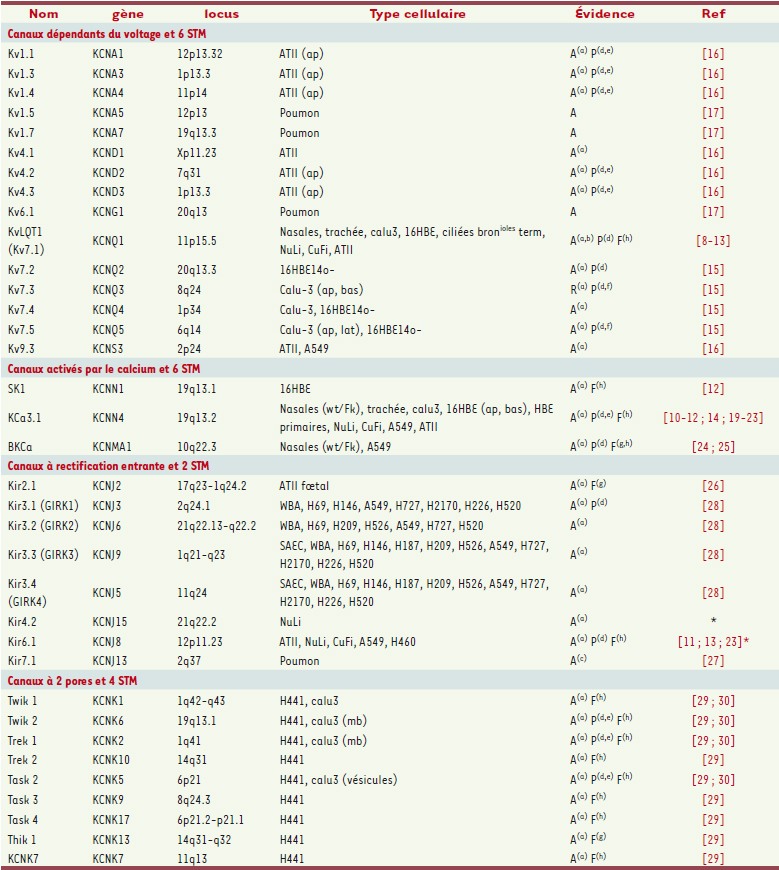
 | Tableau I.
Identification des canaux K+ détectés dans les cellules épithéliales des voies aériennes et du poumon. Les canaux K+ sont regroupés par classe en fonction du nombre prédit de STM : à 6 STM, dépendant du voltage et activés par le calcium ; à 2 STM (à rectification entrante) et à 4 STM (à deux pores). Le nom du canal, du gène, la localisation sur le chromosome (locus), les types cellulaires dans lesquels le canal a été identifié sont indiqués. La mise en évidence au niveau génique (A), protéique (P) et/ou fonctionnel (F) et l’approche expérimentale employée sont également précisées : (a) : PCR ; (b) : hybridation in situ ; (c) : Northern blot ; (d) : immunoblot ; (e) : immunohistochimie ; (f) : immunofluorescence ; (g) : patch-clamp ; (h) : ussing. * : résultats non publiés ; (ap) : membrane apicale, (bas) : membrane basolatérale, mb : membrane ; bronioles resp. : bronchioles respiratoires ; ciliées bronioles term. : cellules ciliées des bronchioles terminales ; wt/Fk : cellules normales et Fk ; lat : membranes latérales ; fibrose kystique (Fk). |
Parmi les canaux Kv à 6 STM, seul le canal KvLQT1 a été clairement caractérisé à l’échelle génique, protéique et fonctionnelle. Il est exprimé tout le long des voies aériennes [
8–
12], ainsi que dans les cellules alvéolaires [
13,
14]. Ce canal serait associé à des sous-unités β MiRP [
10] exprimées dans le poumon. Ce canal de petite conductance (< 3pS, pS pour picosiemens), activé par l’AMPc, participe pour une large part au courant K+ basolatéral mesuré en chambre de Ussing [
11, 13], mais il pourrait également être exprimé à la membrane apicale [
15]. On retrouve plusieurs autres canaux Kv, dont Kv1.1, 1.3, 1.4, 1.5, 1.7, 4.1, 4.2, 4.3, 6.1, 7.2, 7.3, 7.4, 7.5 et 9.3, pour la plupart localisés à la membrane apicale et possiblement impliqués dans la sécrétion de K+, ainsi que les sous-unités régulatrices Kvβ1 et 2, KchIP-2 et −3 [15–
17]. Du point de vue fonctionnel, deux types de courants Kv ont été détectés dans les cellules ATII (cellules alvéolaires de type II). Le plus fréquent de type-n, à 12 pS, sensible à la 4-aminopyridine, est activé par des potentiels de −40 à −20 mV. Le second de type-l, activé par des potentiels plus élevés (− 20 à − 10 mV), est probablement peu actif au potentiel de repos des cellules épithéliales (− 40 mV) [
18]. Deux canaux KCa fonctionnels, soit KCa3.1 et BKCa, ont été mis en évidence. Le canal KCa3.1, à conductance intermédiaire, activé par les composés de type 1-EBIO (1-ethyl-2-benzylimidazolinone, channel opener), est présent depuis les cellules épithéliales nasales jusqu’aux alvéoles [10–12, 14,
19–
23]. Des courants BKCa, de large conductance, ont été également détectés dans les cellules A549 [
24] et nasales, saines ou provenant de patients atteints de Fk [
25]. Plusieurs canaux Kir à 2 STM sont exprimés dans l’épithélium respiratoire. Les identités géniques et protéiques et les propriétés fonctionnelles de deux d’entre eux, Kir6.1 et Kir2.1 ont été mises en évidence. Le Kir6.1, formant avec la sous-unité SUR2B [23] le canal KATP, est exprimé dans les cellules bronchiques (NuLi, CuFi) [11] et ATII [23], ainsi que dans les lignées A549 et H460 (carcinomes pulmonaires humains) (résultats non publiés). Le Kir2.1, lui, a été identifié dans les cellules ATII fœtales [
26]. Les transcrits de plusieurs autres canaux Kir ont été détectés, mais leur fonctionnalité n’a pas été établie : Kir4.2 (cellules NuLi, données non publiées), Kir7.1 (extrait de poumon total) [
27], ainsi que Kir3.1, 3.2, 3.3 et 3.4, aussi appelés GIRK1, 2, 3 et 4 (lignées tumorales pulmonaires) [
28]. Enfin, plusieurs canaux à 4 STM et 2 pores ont été détectés dans la lignée H441 : Twik1, −2, Trek1 (Twik1-related K+ channel), −2, Task2, −3, −4, Thik1 (tandem pore domain halothane-inhibited potassium channel 1) et KCNK7 [
29]. Leur localisation cellulaire a été étudiée dans les Calu3 (cellules sous-muqueuses des voies aériennes humaines) : Twik1, -2 et Trek1 semblent localisés à la membrane (Twik1 à la membrane apicale), tandis que Task2 serait localisé seulement dans des vésicules intracellulaires [
30]. Ainsi, plus de 30 sous-unités α différentes (formant les pores), auxquelles s’ajoutent plusieurs sous-unités β, sont exprimées dans l’épithélium respiratoire. Cette considérable diversité moléculaire des canaux K+ rend ardue leur étude fonctionnelle. Toutefois, les sections suivantes tentent d’analyser ce que l’on sait de leur rôle physiologique. |
Fonction des canaux K + dans la physiologie de l’épithélium respiratoire Échanges gazeux La fonction principale du système respiratoire est de permettre les échanges gazeux d’O 2 et de CO 2. Notre survie dépend donc de la capacité du poumon à s’adapter rapidement à des changements du niveau d’O 2. Les cellules neuro-épithéliales pulmonaires (NEB, localisées dans l’épithélium des voies aériennes), le corpuscule carotidien et le muscle vasculaire lisse sont les trois principaux systèmes de détection de la PO 2 [
31]. Or ces cellules expriment différents canaux K +, dont plusieurs types de canaux Kv [
32,
33], ainsi que Task [ 31] et BKCa [
34], sensibles au niveau d’O 2. À la suite d’une hypoxie, l’inhibition de ces canaux entraîne une dépolarisation membranaire, suivie d’un influx de Ca 2+, nécessaire à la sécrétion des transmetteurs [ 31, 33]. La nature exacte de l’élément responsable de la détection d’O 2 par les canaux K + n’est pas encore clairement définie. Il a été proposé que le canal BKCa détecte directement les changements d’O 2 [ 34]. Toutefois, la sensibilité à l’O 2 pourrait ne pas être intrinsèque au canal mais dépendre d’autres molécules telles que les espèces réactives de l’O 2 (ROS) produites par la NADPH oxydase et/ou la mitochondrie [ 31, 33]. Les canaux K + sensibles à l’O 2 pourraient donc contribuer à la fonction d’adaptation du poumon à son environnement et il a été proposé que leur altération participe à la pathophysiologie de l’hypertension pulmonaire [ 33]. Stabilité alvéolaire La sécrétion de surfactant par les cellules ATII est cruciale pour réduire la tension de surface dans les alvéoles, éviter que celles-ci collapsent à l’expiration et permettre une bonne compliance pulmonaire. Il a été montré que le processus d’exocytose du surfactant par les corps lamellaires des cellules ATII dépend fortement du signal Ca 2+ [
35]. Or, cet influx de Ca 2+ semble dépendant de deux mécanismes : le gradient de H + et le transport de K + par des canaux KCa [
36]. Les canaux K + pourraient donc participer au contrôle de la sécrétion du surfactant. Toutefois, cette hypothèse reste à vérifier, compte tenu du peu d’études sur ce sujet. Réparation épithéliale L’épithélium respiratoire est fréquemment exposé à des particules et à des agents pathogènes. La première défense contre ces agressions est assurée par le phénomène de clairance mucociliaire, qui permet d’évacuer ces particules piégées dans le mucus, et par l’action de molécules antimicrobiennes/immunitaires [
37]. Malgré cela, des infections et une réponse inflammatoire peuvent se développer, menant à des lésions épithéliales (Figure 2A). La réparation épithéliale, nécessaire afin de rétablir la fonction des poumons, fait appel à plusieurs processus dont l’étalement des cellules, une dédifférenciation, une migration des cellules saines vers le site de la lésion, puis une prolifération, suivie d’une redifférenciation cellulaire (Figure 2A, 2B). Certains facteurs de croissance, tels que les facteurs de croissance épidermique (EGF), transformant (TGF) et des kératinocytes (KGF) régulent ces phénomènes. Nous avons démontré que les canaux K + régulent également ces processus. En effet, la réparation, la migration et la prolifération cellulaires sont fortement dépendantes de l’activité des canaux KvLQT1, K ATP et/ou KCa3.1 alvéolaires et bronchiques [ 11, 13]. Nos résultats indiquent également que l’activité et/ou l’expression des canaux K +
(Figure 2C) est régulée par la signalisation de l’EGF [ 11, 13]. Un tel lien entre les canaux K + et l’EGF a été rapporté dans plusieurs types cellulaires. Le mécanisme de couplage n’est pas clairement identifié mais il a été proposé, par exemple, que l’augmentation de la probabilité d’ouverture des canaux Kv par l’EGF dans les cellules myéloblastiques passerait par une phosphorylation du canal dépendante de la protéine kinase A [
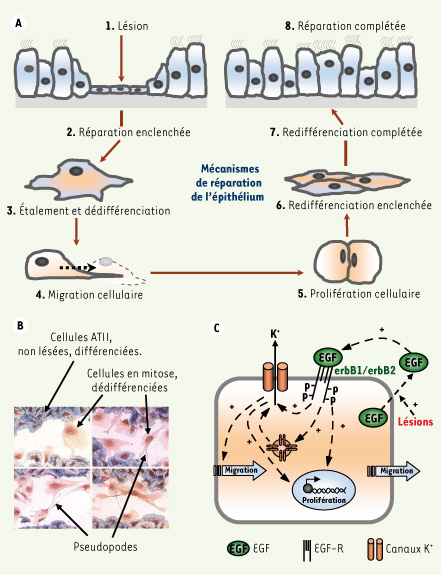
38]. Nous montrons également que les cellules provenant de patients atteints de fibrose kystique présentent des courants K + réduits et une expression diminuée de ces canaux, couplés à une signalisation EGF/EGFR déficiente, pouvant en partie expliquer leur défaut de régénération [ 11]. 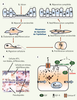 | Figure 2.
Processus de réparation de l’épithélium respiratoire et canaux K+. Les différentes étapes de la réparation de l’épithélium respiratoire consécutive à des lésions sont schématisées en A. La section B représente des photos de lésions mécaniques effectuées sur une monocouche de cellules alvéolaires en culture primaire. La monocouche intacte et différenciée est colorée en bleu (marquage démontrant une activité phosphatase alcaline dans les cellules ATII). Les cellules en train de réparer la plaie sont étalées, elles présentent des pseudopodes et sont dédifférenciées (absence de marquage bleu) ; certaines ont deux noyaux (en cours de mitose). C. Modèle schématique de réparation de l’épithélium pulmonaire, dépendante de l’EGF et des canaux K +, in vitro. Dans le modèle que nous avons proposé à partir de nos résultats [ 13], l’EGF sécrété par les cellules lésées se lie aux récepteurs EGF entraînant une stimulation des courants K +. La migration et la prolifération cellulaires, processus nécessaires à la réparation, sont largement dépendantes de l’activité des canaux K +, comme le montrent nos études [ 11, 13]. EGF : facteur de croissance épidermique, EGFR : récepteur de l’EGF, canaux K + : canaux KvLQT1, K ATP et/ou KCa3.1. |
Le mécanisme de contrôle de la migration et de la prolifération cellulaires par les canaux K+ n’est pas encore totalement élucidé. Toutefois, il semble que des changements du Ca2
i
+ et du volume cellulaire, secondaires aux efflux de K+, puissent être des signaux de prolifération [
39]. D’autre part, l’efflux de K+ suivant l’activation de canaux K+ a été identifié comme un des premiers événements du phénomène d’apoptose. La diminution du volume cellulaire, la déplétion en [K+]i et/ou l’activation de médiateurs pro-apoptotiques subséquents pourraient ensuite activer des caspases et endonucléases ; mais on ignore s’il existe un lien direct ou des facteurs intermédiaires entre ces phénomènes [39]. D’un autre côté, Schwab et al. proposent un modèle dans lequel l’efflux de K+ par les canaux KCa3.1 activés par une élévation du Ca2+
i, favorise la rétraction du pôle de la cellule en migration [
40]. Ainsi les canaux K+, engagés dans les processus de prolifération et migration, mais aussi d’apoptose, pourraient exercer un rôle très complexe dans l’équilibre entre ces phénomènes. Réponse inflammatoire La réponse inflammatoire présente dans plusieurs pathologies pulmonaires peut intervenir à la fois dans les processus lésionnels et de réparation. Or, il a été montré que l’inflammation pouvait moduler les canaux K +. Toutefois, son effet est variable : les courants K ATP (et l’expression de Kir6.1) sont stimulés dans le côlon enflammé [
41], tandis que la probabilité d’ouverture des canaux BKCa des cellules musculaires lisses est réduite à la suite d’une inflammation [
42]. Les médiateurs inflammatoires régulant les canaux K + ne sont pas clairement définis mais il a été établi que l’interleukine-13 (IL-13) stimule le courant KCa3.1 dans les cellules bronchiques NHBE [
22], tandis que le facteur de nécrose tumorale (TNF) augmente les efflux de K +
via le canal K ATP dans les cardiomyocytes [
43]. Inversement, les canaux K+ pourraient intervenir dans la réponse inflammatoire. En effet, leur inhibition réduit la production de TNF par les macrophages alvéolaires stimulés par les lipopolysaccharides bactériens (LPS) [
44]. D’autre part, le glibenclamide, un inhibiteur du KATP, diminue l’infiltration par les polycnucléaires neutrophiles et les niveaux de TNF et d’IL-6 dans l’intestin et le poumon dans un modèle d’ischémie-reperfusion [
45]. Cruse et al. ont également montré que l’inhibition des canaux KCa3.1 pourrait limiter l’infiltration des mastocytes, élément clef de la réponse inflammatoire chez les patients asthmatiques [
46]. Ainsi, un lien entre l’activité des canaux K+ et la réponse inflammatoire pourrait exister et mériterait d’être exploré. Contrôle du transport transépithélial ionique et liquidien L’épithélium pulmonaire exerce des fonctions de transport essentielles à la physiologie du poumon à tous les stades de la vie. En effet, les sécrétions de Cl − et liquidienne sont primordiales dans le développement du poumon fœtal [
47] alors que la réabsorption de Na + favorise la clairance du liquide alvéolaire au moment de la naissance. Ce phénomène est également primordial pour la résorption de l’œdème pulmonaire [ 6]. Dans les voies aériennes, le volume périciliaire nécessaire à la fonction ciliaire dépend d’un équilibre entre la sécrétion de Cl − et la réabsorption de Na +. Chez les patients Fk, une altération de la sécrétion de Cl − entraîne une réduction de la clairance mucociliaire et une accumulation de mucus (Figure 3B, Fk) favorisant les infections et les inflammations chroniques [
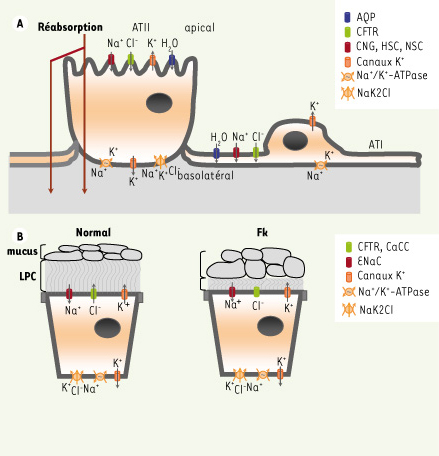
48]. Une régulation adéquate du transport ionique et liquidien est donc nécessaire à la physiologie du poumon. Or, comme nous le détaillons ci-dessous, il est maintenant clairement établi que les canaux K + jouent un rôle central dans le contrôle de la composition et du volume des liquides de surface alvéolaire et des voies aériennes. 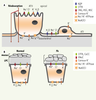 | Figure 3.
Modèles schématiques du transport transmembranaire par l’épithélium alvéolaire et des voies aériennes. A. Épithélium alvéolaire formé de pneumocytes de type I (ou cellules alvéolaires de type I, ATI) et de type II (ATII). B. Épithélium des voies aériennes normal ou de patients atteints de fibrose kystique (Fk). À la surface de l’épithélium Fk, la sécrétion de Cl− est défectueuse, le volume de liquide périciliaire (LPC) est réduit et l’on note une accumulation de mucus. Les principaux mécanismes de transport engagés dans le transport transépithélial dans les alvéoles (A) et les voies aériennes (B) sont représentés : aquaporine (AQP), canaux Cl− (CFTR et CaCC), canaux sodiques CNG (activés par les nucléotides cycliques), HSC (canaux hautement sélectifs, ENaC) et NSC (canaux non-sélectifs), canaux K+, pompe Na+/K+-ATPase, co-transporteur Na+-K+−2Cl−. |
Comme l’illustre le modèle schématique du transport alvéolaire (Figure 3A), les ions Na+ entrent passivement par les canaux Na+ apicaux (CNG, cyclic nucleotide-gated, HSC, highly selective cation et/ou NSC, nonselective cation) puis sont expulsés à la membrane basolatérale par la pompe Na+/K+-ATPase. Les ions K+ sont recyclés par des canaux K+, qui maintiennent le potentiel de membrane et un gradient électrochimique favorable au transport des ions et des fluides. Nous avons démontré que les canaux KvLQT1, KATP et KCa3.1 régulent le transport alvéolaire de Na+ et de Cl− [14, 23]. De façon intéressante, la modulation des canaux K+ régule l’expression des canaux ENaC et CFTR (cystic fibrosis transmembrane conductance regulator) et produit un effet physiologique sur la réabsorption liquidienne [14]. Nous ignorons la nature du mécanisme de couplage reliant l’activité des canaux K+ à l’expression d’ENaC et CFTR, mais des changements de Ca2+
i ou du rapport [Na+]i/[K+]i pourraient influencer leurs facteurs de transcription [14]. Nos résultats sont en accord avec les travaux de Sakuma et al. montrant que l’activation du canal KATP augmente la clairance alvéolaire dans le poumon humain ex vivo [
49]. Il serait maintenant intéressant d’évaluer la capacité des modulateurs des canaux K+ à faciliter la résorption d’un œdème pulmonaire. En ce qui concerne les voies aériennes, plusieurs mécanismes de transport ionique participent à la sécrétion de Cl−, tels que les canaux Cl− (dont CFTR), la pompe Na+/K+-ATPase, le cotransporteur Na+-K+−2Cl−
(Figure 3B). Les canaux KvLQT1 et KCa3.1 constituent aussi des éléments clefs du transport de Cl−. En effet, leur inhibition réduit fortement la sécrétion de Cl− par les cellules des voies aériennes [8, 10, 19,
21]. Inversement, l’activation des canaux KCa3.1, qui stimule la sécrétion de Cl− [19, 21], a été proposée comme une stratégie prometteuse pour favoriser le transport de Cl− dans les tissus Fk par des canaux CFTR résiduels ou des canaux Cl− alternatifs (Figure 3B, Fk). |
Parmi les 30 canaux K+ détectés, KvLQT1, KCa et KATP semblent occuper une place prépondérante dans la physiologie de l’épithélium pulmonaire, en régulant le transport des ions et des fluides ou la réparation épithéliale. Toutefois, le rôle des canaux K+ demeure sous-estimé ; ils pourraient participer à d’autres fonctions comme, par exemple, la réponse inflammatoire ou l’adaptation au niveau d’O2. De plus, la fonction de nombreux canaux K+ n’a pas encore été élucidée et, à notre avis, mériterait d’être plus amplement étudiée. |
Les auteurs remercient le Centre de recherche du CHUM (CRCHUM), le département et la faculté de Médecine de l’Université de Montréal, la Fondation canadienne de fibrose kystique (CCFF), ainsi que le Conseil de recherches en sciences naturelles et en génie du Canada (CRSNG) pour leur soutien.
|
1. Andreeva AV, Kutuzov MA, Voyno-Yasenetskaya TA. Regulation of surfactant secretion in alveolar type II cells. Am J Physiol Lung Cell Mol Physiol 2007; 293 : L259–71. 2. Chilvers MA, O’Callaghan C. Local mucociliary defence mechanisms. Paediatr Respir Rev 2000; 1 : 27–34. 3. Sacco O, Silvestri M, Sabatini F, et al. Epithelial cells and fibroblasts: structural repair and remodelling in the airways. Paediatr Respir Rev 2004; 5 (suppl A) : S35–40. 4. Tulik MK, Fiset PO, Muller O, Hamid Q. Cytokines and chemokines in asthma: an overview, chap. 39. In: Hamid Q, Shannon J, Martin J, eds. Physiologic basis of respiratory diseases. Hamilton, Canada : BC Becker, 2005 : 453–67. 5. Boucher RC. Regulation of airway surface liquid volume by human airway epithelia. Pflug Arch 2003; 445 : 495–8. 6. Berthiaume Y, Matthay MA. Alveolar edema fluid clearance and acute lung injury. Respir Physiol Neurobiol 2007; 159 : 350–9. 7. Papazian DM, Schwarz TL, Tempel BL, et al. Cloning of genomic and complementary DNA from Shaker, a putative potassium channel gene from Drosophila. Science 1987; 237 : 749–53. 8. Mall M, Wissner A, Schreiber R, et al. Role of K(V)LQT1 in cyclic adenosine monophosphate-mediated Cl− secretion in human airway epithelia. Am J Respir Cell Mol Biol 2000; 23 : 283–9. 9. Demolombe S, Franco D, de Boer P, et al. Differential expression of KvLQT1 and its regulator IsK in mouse epithelia. Am J Physiol Cell Physiol 2001; 280 : C359–72. 10. Cowley EA, Linsdell P. Characterization of basolateral K+ channels underlying anion secretion in the human airway cell line Calu-3. J Physiol 2002; 538 : 747–57. 11. Trinh NT, Prive A, Maille E, et al. Control of normal and cystic fibrosis bronchial epithelia repair by EGF and K+ channels activities. Am J Physiol Lung Cell Mol Physiol 2008; 295 : L866–80. 12. Bernard K, Bogliolo S, Soriani O, Ehrenfeld J. Modulation of calcium-dependent chloride secretion by basolateral SK4-like channels in a human bronchial cell line. J Membr Biol 2003; 196 : 15–31. 13. Trinh NT, Prive A, Kheir L, et al. Involvement of KATP and KvLQT1 K+ channels in EGF-stimulated alveolar epithelial cell repair processes. Am J Physiol Lung Cell
Mol Physiol 2007; 293 : L870–82. 14. Leroy C, Prive A, Bourret JC, et al. Regulation of ENaC and CFTR expression with K+ channel modulators and effect on fluid absorption across alveolar epithelial cells. Am J Physiol Lung Cell Mol Physiol 2006; 291 : L1207–19. 15. Moser SL, Harron SA, Crack J, et al. Multiple KCNQ potassium channel subtypes mediate basal anion secretion from the human airway epithelial cell line Calu-3. J Membr Biol 2008; 221 : 153–63. 16. O’Grady SM, Lee SY. Chloride and potassium channel function in alveolar epithelial cells. Am J Physiol Lung Cell Mol Physiol 2003; 284 : L689–700. 17. Coetzee WA, Amarillo Y, Chiu J, et al. Molecular diversity of K+ channels. Ann NY Acad Sci 1999; 868 : 233–85. 18. DeCoursey TE, Jacobs ER, Silver MR. Potassium currents in rat type II alveolar epithelial cells. J Physiol 1988; 395 : 487–505. 19. Mall M, Gonska T, Thomas J, et al. Modulation of Ca2+-activated Cl− secretion by basolateral K+ channels in human normal and cystic fibrosis airway epithelia. Pediatr Res 2003; 53 : 608–18. 20. Thompson-Vest N, Shimizu Y, Hunne B, Furness JB. The distribution of intermediate-conductance, calcium-activated, potassium (IK) channels in epithelial cells. J Anat 2006; 208 : 219–29. 21. Devor DC, Bridges RJ, Pilewski JM. Pharmacological modulation of ion transport across wild-type and DeltaF508 CFTR-expressing human bronchial epithelia. Am J Physiol Cell Physiol 2000; 279 : C461–79. 22. Dulong S, Bernard K, Ehrenfeld J. Enhancement of P2Y6-induced Cl− secretion by IL-13 and modulation of SK4 channels activity in human bronchial cells. Cell Physiol Biochem. 2007; 20 : 483–94. 23. Leroy C, Dagenais A, Berthiaume Y, Brochiero E. Molecular identity and function in transepithelial transport of K(ATP) channels in alveolar epithelial cells. Am J Physiol Lung Cell Mol Physiol 2004; 286 : L1027–37. 24. Ridge FP, Duszyk M, French AS. A large conductance, Ca2+-activated K+ channel in a human lung epithelial cell line (A549). Biochim Biophys Acta 1997; 1327 : 249–58. 25. Kunzelmann K, Pavenstadt H, Beck C, et al. Characterization of potassium channels in respiratory cells. I. General properties. Pflug Arch 1989; 414 : 291–6. 26. Monaghan AS, Baines DL, Kemp PJ, Olver RE. Inwardly rectifying K+ currents of alveolar type II cells isolated from fetal guinea-pig lung: regulation by G protein- and Mg2+-dependent pathways. Pflugers Arch. 1997; 433 : 294–303. 27. Doring F, Derst C, Wischmeyer E, et al. The epithelial inward rectifier channel Kir7.1 displays unusual K+ permeation properties. J Neurosci 1998; 18 : 8625–36. 28. Plummer HK III, Dhar MS, Cekanova M, Schuller HM. Expression of G-protein inwardly rectifying potassium channels (GIRKs) in lung cancer cell lines. BMC Cancer 2005; 5 : 104. 29. Inglis SK, Brown SG, Constable MJ, et al. A Ba2+-resistant, acid-sensitive K+ conductance in Na+-absorbing H441 human airway epithelial cells. Am J Physiol Lung Cell Mol. Physiol 2007; 292 : L1304–12. 30. Davis KA, Cowley EA. Two-pore-domain potassium channels support anion secretion from human airway Calu-3 epithelial cells. Pflug Arch 2006; 451 : 631–41. 31. Kemp PJ, Lewis A, Hartness ME, et al. Airway chemotransduction: from oxygen sensor to cellular effector. Am J Respir Crit Care Med 2002; 166 : S17–24. 32. O’Grady SM, Lee SY. Molecular diversity and function of voltage-gated (Kv) potassium channels in epithelial cells. Int J Biochem Cell Biol 2005; 37 : 1578–94. 33. Lopez-Barneo J, del Toro R, Levitsky KL, Chiara MD, Ortega-Saenz P. Regulation of oxygen sensing by ion channels. J Appl Physiol 2004; 96 : 1187–95. 34. Lewis A, Peers C, Ashford ML, Kemp PJ. Hypoxia inhibits human recombinant large conductance, Ca2+-activated K+ (maxi-K) channels by a mechanism which is membrane delimited and Ca2+ sensitive. J Physiol 2002; 540 : 771–80. 35. Haller T, Auktor K, Frick M, et al. Threshold calcium levels for lamellar body exocytosis in type II pneumocytes. Am J Physiol 1999; 277 : L893–900. 36. Wadsworth SJ, Chander A. H+-and K+-dependence of Ca2+ uptake in lung lamellar bodies. J Membr.Biol. 2000; 174 : 41–51. 37. Coraux C, Hajj R, Lesimple P, Puchelle E. Repair and regeneration of the airway epithelium. Med Sci (Paris) 2005; 21 : 1063–9. 38. Wang L, Xu B, White RE, Lu L. Growth factor-mediated K+ channel activity associated with human myeloblastic ML-1 cell proliferation. Am J Physiol 1997; 273 : C1657–65. 39. Wang Z. Roles of K+ channels in regulating tumour cell proliferation and apoptosis. Pflug Arch 2004; 448 : 274–86. 40. Schwab A, Nechyporuk-Zloy V, Fabian A, Stock C. Cells move when ions and water flow. Pflug Arch 2007; 453 : 421–32. 41. Jin X, Malykhina AP, Lupu F, Akbarali HI. Altered gene expression and increased bursting activity of colonic smooth muscle ATP-sensitive K+ channels in experimental colitis. Am J Physiol Gastrointest Liver Physiol 2004; 287 : G274–85. 42. Lu G, Mazet B, Sun C, et al. Inflammatory modulation of calcium-activated potassium channels in canine colonic circular smooth muscle cells. Gastroenterology 1999; 116 : 884–92. 43. El Ani D, Zimlichman R. TNF-alpha stimulated ATP-sensitive potassium channels and attenuated deoxyglucose and Ca uptake of H9c2 cardiomyocytes. Ann NY Acad Sci 2003; 1010 : 716–20. 44. Maruyama N, Kakuta Y, Yamauchi K, et al. Quinine inhibits production of tumor necrosis factor-alpha from human alveolar macrophages. Am J Respir Cell Mol Biol 1994; 10 : 514–20. 45. Pompermayer K, Amaral FA, Fagundes CT, et al. Effects of the treatment with glibenclamide, an ATP-sensitive potassium channel blocker, on intestinal ischemia and reperfusion injury. Eur J Pharmacol 2007; 556 : 215–22. 46. Cruse G, Duffy SM, Brightling CE, Bradding P. Functional KCa3.1 K+ channels are required for human lung mast cell migration. Thorax 2006; 61 : 880–5. 47. Olver RE, Walters DV, Wilson M. Developmental regulation of lung liquid transport. Annu. Rev Physiol 2004; 66 : 77–101. 48. Boucher RC. New concepts of the pathogenesis of cystic fibrosis lung disease. Eur. Respir. J 2004; 23 : 146–58. 49. Sakuma T, Takahashi K, Ohya N, Nakada T, Matthay MA. Effects of ATP-sensitive potassium channel opener on potassium transport and alveolar fluid clearance in the resected human lung. Pharmacol Toxicol 1998; 83 : 16–22. |