| |
| Med Sci (Paris). 2009 December; 25(12): 1141–1144. Published online 2009 December 15. doi: 10.1051/medsci/200925121141.Les anticorps EMABling®
De la prophylaxie de l’allo-immunisation fœto-maternelle au traitement de la leucémie lymphoïde chronique Rémi Urbain,1* Jean-Luc Teillaud,2 and Jean-François Prost1 1Laboratoire français du fractionnement et des biotechnologies (LFB), 3, avenue des Tropiques, 91958 Les Ulis Cedex, France 2Centre de recherche des Cordeliers/Inserm U872, Paris, France |
Lorsque le Laboratoire français du fractionnement et des biotechnologies (LFB) lança dès les années 1990 un programme de recherche sur un anticorps monoclonal (Acm) susceptible de se substituer à des immunoglobulines (Ig), il ne se doutait sans doute pas que ce programme allait l’amener en quelques années aux frontières de la recherche sur les Acm et à devenir un acteur industriel des biotechnologies… |
Une observation capitale : le rôle de la glycosylation dans les fonctions effectrices des Acm Tout a en effet commencé par la nécessité de substituer par un Acm anti-RhD1 les Ig polyclonales anti-RhD purifiées à partir de plasma humain et utilisées pour la prévention de l’allo-immunisation fœto-maternelle (incompatibilité rhésus). Pour ce faire, nul besoin de banques de phages ou de souris humanisées pour la production d’anticorps humains ! La situation particulière que représentait l’existence de donneurs hyper-immunisés contre l’antigène RhD avait permis en effet au LFB de sélectionner des Acm entièrement humains, de classe IgG1 ou IgG3, grâce à la transformation in vitro de lymphocytes B spécifiques de l’antigène RhD par le virus EBV (Epstein-Barr virus), puis de les produire [
1]. Cependant, malgré une sélection rigoureuse d’Acm spécifiques et de haute affinité, les résultats du premier essai clinique conduit par le LFB en 1995-1996 furent décevants. L’absence de tout modèle animal permettant d’évaluer in vivo la capacité des Acm testés à prévenir l’allo-immunisation anti-RhD conduisit alors le LFB à examiner in vitro les capacités de fixation de différents Acm anti-RhD aux récepteurs pour la région Fc des IgG (RFcγ), ceux-ci jouant un rôle majeur dans la clairance de globules rouges (GR) RhD+ recouverts d’IgG. L’évaluation de la cytotoxicité cellulaire dépendante d’anticorps (ADCC, pour antibody-dependent cellular cytotoxicity) dans les tests effectués avec des GR RhD+ et des cellules mononucléées du sang périphérique (PBMC), dans des conditions de compétition pour la fixation des Acm aux RFcγ (c’est-à-dire en présence de concentrations élevées d’Ig polyclonales), montra alors que tous les anticorps testés, bien que de même isotype (IgG1), ne se valaient pas : l’activité cytolytique de la majorité des Acm était totalement ou partiellement abolie, et seuls quelques rares Acm conservaient une excellente capacité de lyse des GR RhD+ en présence de concentrations élevées d’Ig polyvalentes plasmatiques [
2]. Cela conduisit à l’idée que la région Fc présentait des variations structurales post-traductionnelles expliquant cette variabilité. Cette hypothèse fut renforcée par une observation capitale : le même Acm IgG1 anti-RhD, produit par différentes lignées cellulaires transfectées avec l’ADNc codant ses chaînes lourdes et légères, avait une activité ADCC très différente en fonction du système d’expression [
3]. Le LFB montra alors que des différences importantes de glycosylation existaient pour le même Acm produit dans ces différentes cellules. Les IgG1 humaines présentent en effet un site de N-glycosylation sur l’Asp297 située dans le domaine CH2 de la région Fc (environ 10 % des IgG humaines ont, par ailleurs, un site additionnel de N-glycosylation dans le domaine VH ou VL en fonction de la séquence de ces domaines (→). Cette chaîne de carbohydrates montre une variabilité importante, même lorsqu’il s’agit d’un Acm commercialisé. Elle peut contenir ou non du fucose, du galactose, de l’acide sialique, ou un groupement N-acétyl-glucosamine (GlNac) intercalaire [
4]. Le LFB mit alors en évidence, à la suite du premier essai clinique de 1995-1996, que le taux de fucose de ses Acm anti-RhD variait considérablement et que ce taux était inversement corrélé, dans le cadre de proportions particulières de formes glycanniques, à leur activité ADCC. Ainsi, plus le taux de fucose était bas, plus l’activité ADCC était élevée, du fait d’une capacité accrue de fixation au RFcγIII activateur exprimé par les cellules effectrices NK (natural killer) notamment [
5]. Le LFB a alors engaga le développement d’une plate-forme technologique (EMABling®) fondée sur les propriétés d’une lignée cellulaire particulière permettant la production reproductible d’anticorps ayant un faible taux de fucose. (→) voir R. Abès et al., page 1011 ; A. Beck et al., page 1024
|
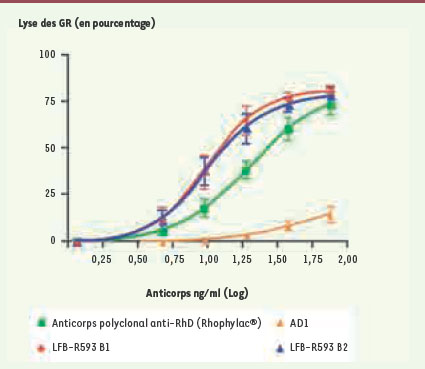
LFB-R593, un anticorps humain optimisé pour la prévention de l’allo-immunisation Parallèlement, le LFB a sélectionné le LFB-R593, un Acm présentant une excellente spécificité vis-à-vis de l’antigène RhD (99,6 % de reconnaissance, évaluée sur 12 500 prélèvements de sang de cordon de nouveau-nés RhD+ et plus de 100 000 prélèvements sanguins adultes),, une capacité élevée à se fixer aux différents RFcγ humains et induisant une forte ADCC contre les GR RhD+
(Figure 1). Une première génération de cet Acm testé dans un essai clinique de phase I induit une clairance dose-dépendante des GR RhD+ et plus rapide que celle induite par les Ig anti-RhD commercialisées [
6]. Cela constitue la première démonstration clinique qu’un Acm optimisé pour l’affinité de sa région Fc pour les RFcγ activateurs présente des potentialités thérapeutiques accrues. Aucun effet secondaire notable n’a été observé chez ces volontaires, et notamment aucune augmentation significative du taux sérique de cytokines pro-inflammatoires [6]. Désormais produit à l’échelle industrielle, le LFB-R593 est actuellement évalué dans un essai de phase I chez des volontaires sains RhD- pour déterminer sa pharmacocinétique et confirmer sa bonne tolérance. Un essai de phase II également en cours a pour objectif de confirmer l’efficacité du LFB-R593, administré par voie intraveineuse ou intramusculaire.  | Figure 1.
Augmentation de l’ADCC par les anticorps peu fucosylés. Lyse des globules rouges RhD+ en présence de cellules mononucléées circulantes humaines et d’IgG polyclonales anti-RhD (courbe verte), de l’Acm anti-RhD AD1 ayant une faible affinité pour le RFcγIII (courbe orange) et de deux lots (B1 et B2) de l’Acm anti-RhD LFB-R593 ayant une forte affinité pour le RFcγIII (courbes bleue et rouge). |
|
LFB-R603, un anticorps anti-CD20 hautement cytotoxique Tirant parti de son observation d’une capacité cytotoxique accrue d’Acm faiblement fucosylés, le LFB a entrepris le développement d’un Acm dirigé contre la molécule CD20, exprimée à la surface des lymphocytes B, et cible d’intérêt thérapeutique en onco-hématologie (→). Grâce à une stratégie analogue de criblage in vitro d’un Acm capable de fixer fortement le RFcγIII et d’induire une ADCC contre des cellules tumorales CD20+, le LFB a produit et sélectionné l’Acm anti-CD20 LFB-R603. Dans différentes expériences d’ADCC (utilisant comme cellules effectrices des cellules mononucléées du sang périphérique (PBMC), des cellules NK, ou des macrophages et comme cibles différentes cellules CD20+), cet Acm présente une capacité à lyser les cellules CD20+ supérieure à celle du rituximab, en particulier lorsque la densité de CD20 est faible, comme c’est le cas des cellules de patients souffrant de leucémie lymphoïde chronique (LLC) [
7]. Des données in vivo obtenues chez le singe cynomolgus montrent que LFB-R603 induit une déplétion dose-dépendante, profonde et prolongée, des cellules CD20+, non seulement dans le sang périphérique mais également dans les organes lymphoïdes, sans signe majeur de toxicité ou d’immunogénicité. Cet anticorps, produit en conditions GMP (good manufacturing practice) par la filiale du LFB, MAbgène, est actuellement testé dans un essai national multicentrique de phases I/II chez des patients présentant une LLC. (→) voir G. Cartron et J.F. Rossi, page 1085
Producteur de longue date d’Ig polyvalentes d’origine plasmatique (IVIg, Ig antitétanique, Ig anti-HBs), le LFB s’appuie désormais sur une plate-forme performante de génération et de production par culture cellulaire d’Acm recombinants hautement cytotoxiques (plate-forme EMABling®), et dispose par son alliance avec la société GTC BioTherapeutics d’un moyen de produire des Acm à bas coût et à haut rendement par transgenèse animale. Il a ainsi constitué un portefeuille varié d’Acm en développement qui trouveront certainement leur place dans les biothérapies de demain pour traiter des maladies graves ou rares, dans le respect de la mission de santé publique du LFB. |
Rémi Urbain et Jean-François Prost déclarent avoir des liens durables ou permanents avec l’entreprise LFB. Jean-Luc Teillaud déclare avoir participé à des interventions ponctuelles pour l’entreprise Laboratoire français du Fractionnement et des Biotechnologies (LFB).
|
Les auteurs remercient leurs collègues du LFB qui conduisent la recherche, la production et le développement des anticorps monoclonaux cités, et notamment les équipes-projet LFB-R603 et LFB-R593 (P. Azam, A. Bardet, C. Behrens, R. Béliard, A. Bellon, N. Bihoreau, D. Bourel, G. Chartier, S. Chtourou, I. Chwedura, L. Cohen-Tannoudji, C. de Romeuf, F. Dhainaut, N. Fernandez, B. Fournès, C. Gaucher, A. Glacet, P. Henno, S. Huille, S. Jorieux, O. Just, N. Khandoudi, Y. Kim, C. Kimmel, P. Klein, M. Ollivier, P. Pecquet, B. Perron, C. Plétan, D. Quagliaroli, M. Salcedo, A. Sadoun, L. Siret, M. Schlegel, F. Verhoeye, A. Yver) et de l’équipe 14 « Biotechnologie des Anticorps » du Centre de Recherche des Cordeliers (S. Sibéril, C.A. Dutertre, R. Abès), ainsi que le Directeur du Centre de recherche des Cordeliers/Inserm U872, le Professeur W.H. Fridman.
|
Footnotes |
1. Glacet A, Ducrot T, Béliard R, et al. Anti-Rh(D) monoclonal antibodies: study of their in vitro functional properties. Transfus Clin Biol 1996; 3 : 465–8. 2. Kumpel BM, Beliard R, Brossard Y, et al. Section 1C: assessment of the functional activity and IgG Fc receptor utilization of 64 IgG Rh monoclonal antibodies. Coordinator’s report. Transfus Clin Biol 2002; 9 : 45–53. 3. De Romeuf C, Gaucher C, Glacet A, et al. Expression of human anti Rh(D) monoclonal antibodies into different cell lines: influence on their functional properties. In : Subramanian G, ed. Antibodies, vol. 2. Novel technologies and therapeutic use. Amsterdam : Kluwer Academic Publishers, 2004. 4. Jefferis R. Glycosylation as a strategy to improve antibody-based therapeutics. Nat Rev Drug Discov 2009; 8 : 226–34. 5. Sibéril S, de Romeuf C, Bihoreau N, et al. Selection of a human anti-RhD monoclonal antibody for therapeutic use: impact of IgG glycosylation on activating and inhibitory Fc gamma R functions. Clin Immunol 2006; 118 : 170–9. 6. Béliard R, Waegemans T, Notelet D, et al. An anti-D monoclonal antibody selected for enhanced Fcgamma RIII engagement clears RhD-positive autologous red cells in human volunteers as efficiently as polyclonal anti-D antibodies. Br J Haematol 2008; 141 : 109–19. 7. De Romeuf C, Dutertre CA, Le Garff-Tavernier M, et al. Chronic lymphocytic leukaemia cells are efficiently killed by an anti-CD20 monoclonal antibody selected for improved engagement of Fcgamma RIIIA/CD16. Br J Haematol 2008; 140 : 635–43. |