| |
| Med Sci (Paris). 2015 May; 31(5): 506–514. Published online 2015 June 9. doi: 10.1051/medsci/20153105012.Latence et réactivation du virus de l’herpès simplex de type 1 (HSV-1) Une mise à jour Alejandro M. Aranda1 and Alberto L. Epstein1* 1UVSQ-Inserm U1179 - End-icap, Handicap Neuromusculaire - Physiopathologie, Biothérapie et Pharmacologie appliquées, UFR des sciences de la santé Simone Veil, Université de Versailles Saint-Quentin-en-Yvelines, 2, avenue de la source de la Bièvre, 78180Montigny-le-Bretonneux, France |
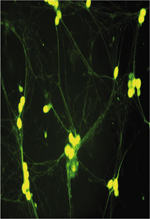
L’herpès simplex de type 1 (HSV-1 ou HHV-1, pour human herpesvirus 1) est un virus humain responsable de lésions vésiculeuses des muqueuses orale ou nasale, mais qui peut provoquer des maladies plus graves lorsqu’il infecte les yeux, le système nerveux central ou dans le cadre d’une infection disséminée, souvent associée à des déficits immunitaires. HSV-1 est transmis généralement par la salive et a une prévalence de 52 à 67 % dans l’Europe du Nord. La structure de la particule virale est schématisée dans la
Figure 1.
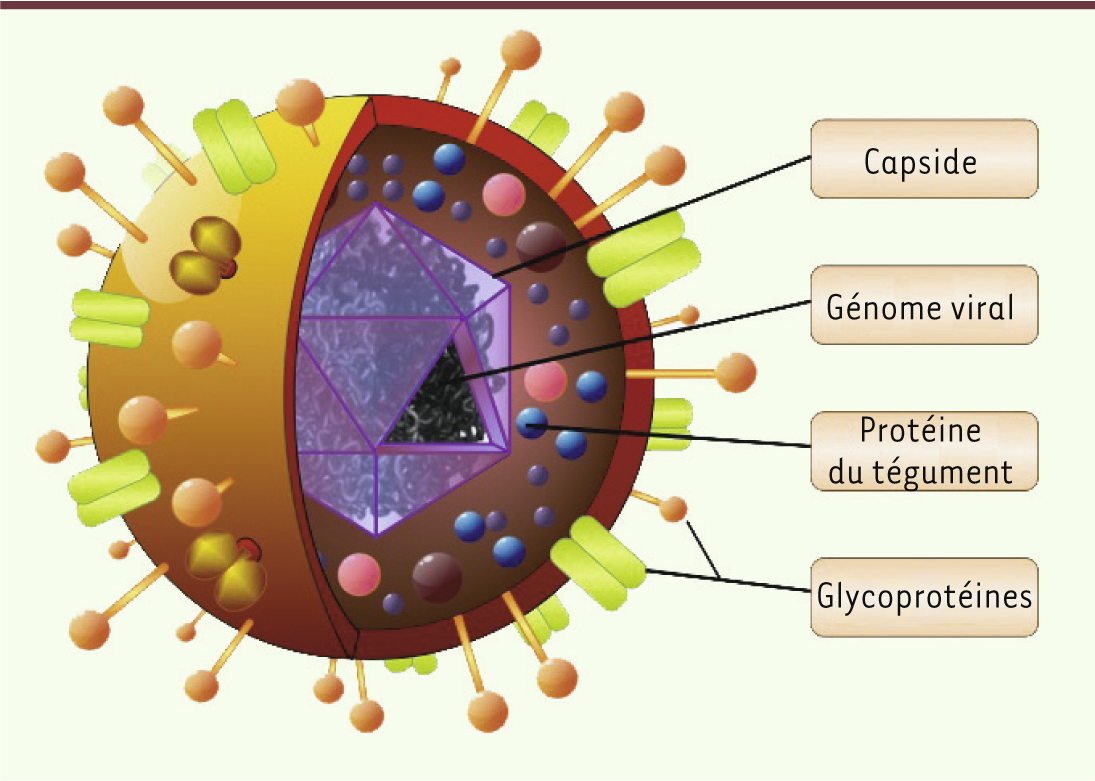
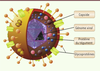 | Figure 1.
Structure de la particule d’HSV-1. La capside d’HSV-1 est une structure icosaédrique composée de 162 capsomères, mesurant environ 100 nm de diamètre. Elle contient le génome viral, une molécule d’ADN bicaténaire linéaire, qui n’est associée ni à des histones ni à aucune autre protéine. L’ADN viral a une taille d’environ 153 kb et code pour approximativement 90 protéines et au moins 16 microARN. Entourant la capside se trouve le tégument, une couche relativement amorphe de protéines qui jouent des rôles importants dans la morphogenèse de la particule et dans la régulation de la phase très précoce de l’infection, après la pénétration de la particule. Au moins 20 espèces de protéines différentes (représentées par des billes de différentes tailles et couleurs) sont présentes dans le tégument, incluant la protéine VP16. L’enveloppe virale entoure cet ensemble. C’est une membrane bilipidique d’origine cellulaire contenant près de 15 glycoprotéines et protéines de membrane codées par le génome viral (représentés par des spicules colorés). La particule virale mesure environ 200 nm et contient plus de 40 protéines qui sont, à quelques exceptions près, codées par des gènes tardifs. Elle est moins sphérique que dans ce schéma. |
Comme tous les virus de la famille herpesviridae, HSV-1 peut établir deux types d’interaction avec les cellules hôtes : une infection lytique et une infection latente. Dans le cas d’HSV-1, l’infection lytique a généralement lieu dans les cellules épithéliales de la muqueuse orale lors de la primo-infection, tandis que l’infection latente a lieu dans les neurones sensitifs innervant la région infectée, dont les corps cellulaires se trouvent dans les ganglions trijumeaux. Pendant la latence, le génome viral persiste dans le noyau de ces neurones de manière silencieuse, sans synthèse de protéines virales et sans toxicité, mais sous une configuration qui permet à tout moment, sous l’action de certains stimulus, sa réactivation et l’entrée dans un cycle lytique. Des particules virales sont transportées alors vers les tissus périphériques via les axones innervant ceux-ci, et y provoqueront des infections secondaires (aussi dites récurrentes), ce qui est le trait le plus caractéristique et le plus gênant de la pathogenèse de l’HSV-1 [1]. Si l’infection latente permet de préserver le génome viral dans l’organisme infecté, en échappant à l’action de l’immunité, la réactivation permet la transmission du virus à de nouveaux individus, pérennisant ainsi son maintien dans la population humaine [2]. Le virus peut développer ces deux types d’infection grâce à la coexistence dans son génome de deux programmes alternatifs d’expression génique. Dans les cellules épithéliales, c’est le programme d’expression génique associé à une infection lytique qui se met en place, alors que le programme génique de la latence s’exprimera dans les neurones sensitifs. Cependant, les neurones peuvent exprimer aussi des gènes d’infection lytique, surtout pendant les premiers jours de l’infection ou lors de la réactivation virale. Le démarrage de l’un ou de l’autre de ces programmes, ainsi que le passage de l’un à l’autre, sont contrôlés par des régulations épigénétiques au niveau du génome viral, et par les réponses innées du neurone à l’infection. Notre compréhension de la latence d’HSV-1 a considérablement progressé récemment. Cette revue a pour objectif de faire le point sur la perception que nous avons aujourd’hui de ce phénomène. Il convient pour cela de comparer les phases très précoces des infections lytique et latente - car c’est à ce niveau que se joue en grande partie l’avenir de l’infection - et d’analyser l’infection latente en trois phases : l’établissement, le maintien et la réactivation. |
Établissement de l’infection lytique L’HSV-1 pénètre dans les cellules par fusion entre l’enveloppe virale et la membrane cellulaire. Une fois dans le cytosol, la capside se dissocie des protéines du tégument1, et est transportée jusqu’aux pores nucléaires par des protéines motrices associées aux microtubules. Linéaire dans la capside, le génome viral est relâché dans le noyau où il prend une configuration circulaire [1]. Commence alors l’expression des gènes très précoces (codant essentiellement pour des protéines de régulation), suivie de celle des gènes précoces (codant notamment pour des protéines de l’appareil de réplication de l’ADN) et, après le démarrage de la synthèse d’ADN, de celle des gènes tardifs (codant pour les protéines de la capside, du tégument et de l’enveloppe virale) [3], aboutissant en quelques heures à la production de nouvelles particules infectieuses et à la mort cellulaire. Dès sa pénétration dans le noyau des cellules épithéliales, le génome viral interagit avec des histones, mais sans aboutir à une chromatinisation totale du génome [4]. L’interaction des histones et d’autres protéines répressives avec le génome viral est probablement une réponse cellulaire visant à inhiber l’expression génique. Mais le virus détourne cette réponse grâce à l’action de VP16, une protéine tégumentaire qui pénètre dans les noyaux et qui s’associe aux protéines cellulaires octamer binding protein 1 (OCT1) et host cell factor 1 (HCF1) [5]. L’interaction du complexe ternaire VP16/OCT1/HCF1 avec les promoteurs des gènes très précoces favorise l’association de ceux-ci avec des histone acétyltransférases (CBP/p300, CLOCK [circadian locomotor output cycles kaput]) [5, 6] et des lysine déméthylases (LSD1, lysine [K]-specific demethylase 1A) [7] ; celles-ci modifient ces histones de manière à favoriser la transcription et la synthèse des protéines très précoces (Figure 2).
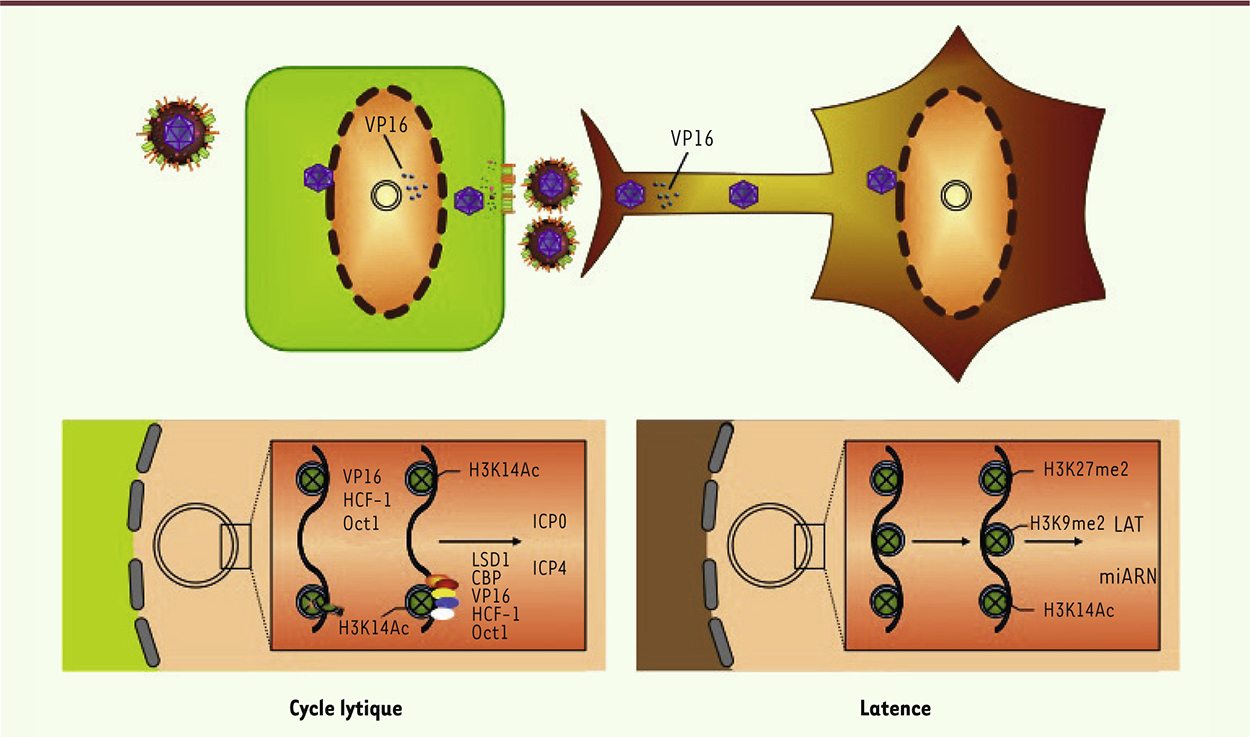
 | Figure 2.
Infection lytique et infection latente. Lorsque le virus infecte une cellule épithéliale, le génome viral pourra exprimer le programme d’expression lytique car le complexe ternaire VP16/HCF1/OCT1, associé à des histone acétyl-transférases (CBP) et des déméthylases (LSD1), interagit avec les promoteurs des gènes viraux très précoces, empêchant la formation d’hétérochromatine répressive et activant l’expression des protéines très précoces. L’action de ces protéines, en particulier ICP0 et ICP4, permettra ensuite la transcription des gènes précoces et tardifs et la progression du cycle viral lytique. Peu de nucléosomes sont associés au génome viral pendant le cycle lytique. En revanche, lorsque la particule pénètre dans les neurones sensitifs, le complexe VP16/HCF1/OCT1 ne peut pas se former, probablement parce que la protéine VP16 serait retenue ou dégradée dans les axones. Le génome viral s’associe alors à des nucléosomes pour devenir une structure chromatinienne classique compacte, dans laquelle les histones associées aux promoteurs des gènes lytiques sont dans une configuration répressive, empêchant l’expression des protéines très précoces. Seul le promoteur du locus LAT sera dans une configuration permissive, permettant la transcription des ARN LAT. Cette configuration épigénétique s’inversera pendant la réactivation. Les miARN dérivés de la région LAT (voir
Figure 3
) contribuent à la répression de l’expression des fonctions lytiques, et donc au maintien de la latence, en empêchant la synthèse d’ICP0 et de g34.5, deux protéines virales jouant un rôle d’inhibition des réponses innées cellulaires, ainsi que d’ICP4, un activateur de la transcription. |
Parmi les protéines très précoces, la protéine ICP0 (infected cell polypeptide 0) joue un rôle majeur dans la progression du cycle lytique. ICP0 est un activateur de la transcription qui interagit avec des protéines cellulaires et possède une activité E3 ubiquitine ligase qui conduit à la protéolyse de plusieurs d’entre elles [8]. ICP0 agit en inhibant des réponses antivirales, tant au niveau des voies de l’interféron (IFN) qu’au niveau des défenses intrinsèques présentes dans les noyaux avant l’infection [9]. Des mutants d’HSV-1 exprimant une protéine ICP0 inactive ont une moindre probabilité de déclencher une infection lytique, surtout à faible multiplicité [10]. Nous ne pouvons pas décrire ici en détail les multiples activités d’ICP0. Mais il est important de signaler que cette protéine empêche l’association du génome viral à des protéines nucléaires impliquées dans les défenses intrinsèques de la cellule, dont PML (promyelocytic leukaemia), Sp100, Daxx et ATRX (alpha thalassemia/mental retardation syndrome X-linked) [10, 11]. ICP0 interagit aussi avec des histones déacétylases [12] et induit la dégradation de plusieurs protéines centromériques [13], ainsi que celle de protéines participant à la réparation de l’ADN [14]. ICP0 déplacerait aussi la protéine CoREST (REST [RE1-silencing transcription factor] corepressor 1) du complexe répresseur REST/CoREST qui se déposerait sur les promoteurs précoces et tardifs du génome viral, favorisant ainsi la transcription de ces gènes [15]. ICP0 joue donc un rôle critique en tant qu’antagoniste des réponses cellulaires répressives, créant un environnement favorable à l’expression des gènes viraux et à la progression du cycle lytique. |
Établissement de l’infection latente Deux faits majeurs distinguent l’infection latente de l’infection lytique : l’absence d’expression des gènes lytiques et l’expression du gène LAT (latency associated transcripts), seul gène viral à s’exprimer pendant la latence [1, 2]. Dans les neurones sensitifs, VP16 n’est pas efficacement transportée le long des axones et n’arrive pas aux noyaux [16, 17]. De plus, dans les neurones, HCF1 est détectée seulement dans le cytoplasme et elle est incapable d’interagir avec VP16, car inaccessible [18]. Enfin, OCT1 n’est pas exprimée dans les neurones [19]. Il en résulte que le complexe VP16/OCT1/HCF1 ne se forme pas, ce qui se traduit par un déficit de l’expression des gènes très précoces (Figure 2). Une étude récente apporte une contribution majeure concernant le rôle de VP16 dans les étapes très précoces de l’infection latente [17] : des explants de ganglions trijumeaux ont été mis en culture dans un dispositif à deux compartiments, permettant de séparer les corps cellulaires (compartiment central) des terminaisons nerveuses (compartiment périphérique). En introduisant le virus dans l’un ou l’autre de ces compartiments, on constate que l’infection des corps cellulaires conduit à une infection lytique, alors que l’infection des terminaisons nerveuses mène presque toujours à une infection quiescente, caractérisée par une très faible expression des gènes lytiques et une forte transcription des gènes LAT. La surinfection du compartiment central avec un virus défectif, qui apporte VP16 dans son tégument, réactive l’expression des gènes lytiques. Ces résultats suggèrent que l’entrée du virus via les terminaisons nerveuses se traduit par l’absence de VP16 dans les noyaux, ce qui est déterminant pour l’induction de la latence. En l’absence de VP16, l’expression des protéines très précoces, dont ICP0, sera très limitée, favorisant la chromatinisation du génome viral sous une forme répressive. |
Ces résultats pourraient laisser croire que l’entrée en latence serait simplement la conséquence du défaut d’activité de VP16 et d’ICP0. Or, la situation est plus complexe, car dès que le génome viral pénètre et se circularise dans les noyaux des neurones sensitifs, l’expression du gène LAT, dont le promoteur possède des motifs neuro-spécifiques, démarre [20, 21]. La transcription du locus LAT produit un transcrit de 8,3 kb qui est épissé pour produire un intron atypique de 2,0 kb, dénommé LAT majeur parce qu’il est très stable et s’accumule dans les noyaux des neurones sensitifs [22] (Figure 3). L’exon de 6,3 kb qui résulte de l’excision de l’intron est, en revanche, très instable car rapidement dégradé, et entraîne la formation de plusieurs microARN (miARN) [23].
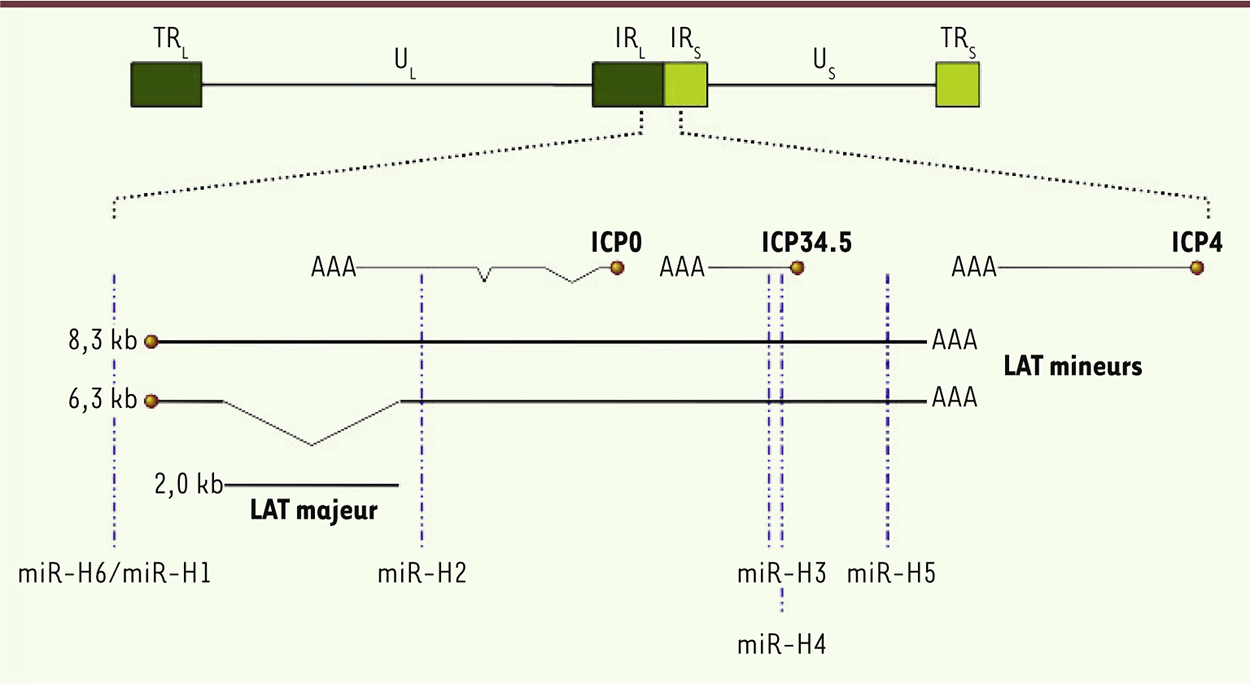
 | Figure 3.
Structure du génome viral et du locus LAT.
Le génome viral est composé de séquences uniques longues (UL) et courtes (US) entourées par des séquences répétées terminales et internes (TRL/IRL et IRS/TRS respectivement). Le génome viral est représenté ici dans sa configuration linéaire, tel qu’il se trouve dans la particule virale. Le locus LAT est localisé dans les séquences répétées TRL et IRL et il est donc diploïde. Ce locus exprime, sous le contrôle de séquences de régulation neurospécifiques, un ARN de 8,3 kb qui est rapidement épissé pour donner un intron de 2,0 kb et un exon de 6,3 kb, lequel est rapidement dégradé pour donner plusieurs miARN dénommés miR-H2, H3, H4, H5, H7 et H8. Les miARN miR-H1 et H6 sont, eux, localisés juste en amont du site d’initiation de la transcription des LAT et ils sont antisens l’un par rapport à l’autre. Les ARN de 8,3 et 6,3 kb sont appelés LAT mineurs car ils sont très instables et extrêmement difficiles à détecter. L’intron de 2,0 kb est appelé LAT majeur, car il est, en revanche, très stable et s’accumule dans les noyaux des neurones sensitifs. Les miR-H2 et miR-H4 inhibent la synthèse des protéines ICP0 et γ34.5 respectivement. Le miR-H6 inhibe la synthèse de la protéine ICP4, dont le gène est localisé juste en aval du locus LAT. Les ARN LAT sont transcrits en direction antisens par rapport aux gènes ICP0 et γ34.5, avec lesquels ils se chevauchent. Le transcrit primaire d’ICP0 contient deux introns. TRL et IRL : répétitions terminale et interne entourant la séquence unique ; IRS et TRS : répétitions terminale et interne entourant la séquence unique S. |
Deux fonctions majeures des LAT semblent aujourd’hui clairement établies. D’une part, ils répriment l’expression des gènes viraux lytiques, d’autre part, ils favorisent la survie des neurones infectés. L’expression des gènes très précoces dans les neurones est plus active en présence de mutants n’exprimant pas les LAT que lors de l’infection par un virus sauvage. Par ailleurs, la surexpression des LAT dans des cellules en culture se traduit par une diminution de l’expression des gènes très précoces. HSV-1 exprime au moins 16 miARN dont 8 (dénommés H1-H8) sont localisés dans la région LAT [23] et sont exprimés pendant la latence. Les miARN H2, H4 et H6 inhibent respectivement l’expression d’ICP0, de la protéine γ34.5 - qui joue un rôle critique dans l’inhibition des réponses cellulaires antivirales - et de la protéine ICP4 - un activateur de la transcription des gènes précoces et tardifs [23, 24] (Figure 3). Il paraît donc assez plausible que l’action de ces miARN explique, au moins en partie, le rôle répresseur des LAT. Une étude très récente montre l’existence d’au moins un miARN neurospécifique (miR-138) qui inhibe l’expression d’ICP0 et favorise l’entrée en latence du génome viral dans les neurones [25]. L’absence d’expression des gènes très précoces dans les neurones découlerait donc à la fois de l’absence de VP16 dans les noyaux et de l’action de miARN d’origines virale et cellulaire. La deuxième fonction proposée pour les LAT est la protection du neurone infecté. En effet, l’infection de souris avec des virus n’exprimant pas les LAT se traduit par une perte de neurones sensitifs plus importante que lors de l’infection par un virus sauvage. Certaines études suggèrent que les LAT auraient une action anti-apoptotique, en inhibant la mort cellulaire induite par l’infection herpétique [26]. Cependant, d’autres observations ne confirment pas l’existence d’un phénomène antiapoptotique et suggèrent que l’action protectrice des LAT serait simplement la conséquence de l’inhibition de l’expression des gènes lytiques [27]. |
On ne connaît pas en détail le déroulement de l’infection dans les ganglions sensitifs humains mais, lors de l’infection expérimentale chez la souris, HSV-1 développe pendant quelques jours une infection aiguë dans les ganglions innervant la région infectée, avant que l’infection ne devienne exclusivement latente. L’utilisation de certains mutants viraux incapables de se multiplier dans les neurones montre que l’établissement de la latence ne nécessite pas de multiplication du virus dans les ganglions sensitifs [28]. Cependant, elle est beaucoup plus fréquente lors de l’utilisation d’un virus sauvage, laissant la porte ouverte à la possibilité d’une entrée en latence après réplication du virus dans les ganglions. La question n’est pas tranchée. Quoi qu’il en soit, l’apparition, quelques jours après l’infection, d’une réponse immune spécifique coïncide avec l’arrêt de la multiplication du virus dans les ganglions sensitifs. À partir de ce moment, ces ganglions contiennent seulement des génomes viraux en latence [29]. On observe alors une forte expression des LAT et pas d’expression des gènes lytiques. Cependant, l’infection latente présente certaines caractéristiques qui sont extrêmement variables : d’abord, le nombre de neurones par ganglion contenant des génomes en latence peut varier en fonction de la multiplicité d’infection, de la souche virale et de la voie d’inoculation, mais, en tout état de cause, seule une fraction de neurones par ganglion contiennent des génomes viraux dans leurs noyaux, car la sensibilité des neurones sensitifs à l’infection n’est pas homogène. Ainsi, le génome HSV-1 s’établit en latence et exprime les LAT préférentiellement dans des neurones sensitifs identifiés par l’anticorps A5 (spécifique d’une sous-population de neurones exprimant le ganglioside Galβ14GlcNAc-R) et beaucoup moins dans ceux identifiés par l’anticorps KH10 (spécifique d’une autre sous-population de neurones ganglionnaires, exprimant le ganglioside Galα1-3Galβ14NAc-R) [30]. Ensuite, le nombre de génomes viraux par neurone est extrêmement variable. Certains neurones contiennent un petit nombre de génomes viraux (parfois seulement un génome), alors que la plupart contiennent entre 10 et 100 génomes, et que certains peuvent même en contenir des centaines [31, 32]. Enfin, la probabilité d’expression des LAT est également un caractère variable, plusieurs observations indiquant que le locus LAT est transcrit, au mieux, dans environ 30 % des neurones contenant des génomes viraux [32, 33]. En utilisant des techniques permettant de détecter simultanément les génomes viraux, les transcrits LAT et des protéines cellulaires, l’équipe de Patrick Lomonte a analysé récemment la distribution intranucléaire des génomes latents, leur interaction avec des domaines nucléaires (centromères et corps PML) et la relation entre cette association et la transcription des LAT, dans des neurones individuels à l’intérieur des ganglions sensitifs de la souris, à 6 jours et à 28 jours post-infection, c’est-à-dire en phase de réplication aiguë et de latence, respectivement [32]. Cette étude montre que les génomes en latence adoptent principalement deux patrons d’organisation intranucléaire, désignés Single et Multiple. Le patron Single est caractérisé par la présence d’un tout petit nombre de génomes viraux qui peuvent être visualisés par hybridation in situ (FISH) sous la forme d’un seul point fluorescent par neurone. Ces agrégats de génomes sont presque toujours entourés par les protéines PML, Daxx et ATRX, qui forment une sorte de coque autour d’eux. Dans cette configuration, l’expression des LAT est très limitée, voire nulle. La configuration Multiple montre plusieurs points fluorescents, dont la taille et la brillance sont hétérogènes. Chaque point contient un seul ou un petit nombre de génomes. Certains points sont associés à des corps PML ou à des centromères, mais d’autres points ne sont pas associés à ces domaines. La configuration Multiple favorise l’expression des LAT, mais seulement à partir des génomes viraux non associés aux centromères ou aux corps PML, indiquant le rôle répresseur de ces domaines. L’association entre les corps PML et les génomes viraux démarre tôt dans le processus menant à la latence, probablement pendant la phase aiguë de l’infection (elle est évidente à 6 jours post-infection), cette interaction jouant un rôle important dans la distribution intranucléaire des génomes viraux. L’étude de l’infection d’animaux dont l’expression de la protéine PML est abolie par invalidation génique confirme que les corps PML influencent le nombre de génomes viraux qui vont s’établir de manière latente et la formation des patrons intranucléaires adoptés par les génomes viraux. Dans les neurones dépourvus de PML, la transcription du locus LAT est significativement augmentée, confirmant que les corps PML contrôlent négativement l’expression des LAT [32, 47]. |
Régulation épigénétique de la latence Dans les neurones sensitifs, l’association du génome viral avec des histones conduit à la formation de nucléosomes [48] dans une configuration chromatinienne dense et classique. Le génome viral en latence est donc un minichromosome circulaire [34]. Le contrôle épigénétique de l’expression pendant la latence et la réactivation est assuré principalement par des modifications post-traductionnelles des histones. Ainsi, pendant la latence, les nucléosomes associés au promoteur du locus LAT sont enrichis en histones contenant des modifications post-traductionnelles permissives pour la transcription (H3K9ac et H3K14ac), alors que ces modifications post-traductionnelles sont absentes dans les histones entourant les promoteurs des gènes lytiques. Ceux-ci sont, en revanche, enrichis en histones contenant des marqueurs d’hétérochromatine facultative (H3K27met) ou constitutive (H3K9met), suggérant que les génomes viraux peuvent être réprimés de manière réversible ou irréversible [35, 36] (Figure 2). L’induction de la réactivation réduit l’association du promoteur LAT avec les histones contenant des modifications post-traductionnelles permissives, provoquant une diminution de l’expression des LAT, et une augmentation concomitante de l’association des marqueurs permissifs dans les histones associées aux promoteurs de gènes lytiques [37]. Après infection par des virus mutants n’exprimant pas les LAT, on observe une diminution de l’association de chromatine répressive avec les promoteurs des gènes lytiques. Cela indique que les LAT favorisent la répression de ces promoteurs. Cependant, on ne sait pas si un même génome en latence est associé simultanément à de l’hétérochromatine facultative et à de l’hétérochromatine constitutive, ou bien si certains génomes sont associés seulement à de l’hétérochromatine facultative (pouvant réactiver plus facilement), alors que d’autres le seraient à de l’hétérochromatine constitutive. |
Réactivation à partir de l’état de latence Chez l’homme, la réactivation peut être déclenchée par des stress émotionnels, la température, la ménorrhée, l’immunosuppression, ou par des traumatismes neurologiques. Dans les modèles animaux, les résultats des études de la réactivation varient en fonction du modèle utilisé. La plupart des études in vivo ont été réalisées chez la souris, espèce dans laquelle le taux de réactivation spontané d’HSV-1 est très bas. Dans ce cas, la réactivation est généralement obtenue par explantation des ganglions sensitifs qui sont dissociés et cocultivés avec des cellules permissives. Une approche alternative consiste à soumettre la souris à un stress, par exemple un court choc thermique, ce qui induit également la réactivation du génome viral. Cependant, dans ces conditions, la base moléculaire de l’événement déclencheur de la réactivation est difficile à déterminer, ce qui a encouragé des chercheurs à établir des modèles de latence utilisant des cultures de neurones primaires, plus accessibles à une approche expérimentale. Inducteurs de la réactivation du génome viral On sait aujourd’hui cultiver des neurones périphériques primaires (autonomes et sensitifs), ce qui permet d’établir efficacement des infections dont les caractéristiques moléculaires sont très proches de celles de la latence [ 38]. Cette approche a permis d’induire la réactivation en utilisant des stimulus bien définis, tels que la privation en facteur de croissance des cellules nerveuses (NGF), l’ajout de tricostatine A (TSA), de forskoline, de capsaïcine, de dexaméthasone, etc. En utilisant des inhibiteurs spécifiques des différentes étapes de la voie de signalisation du NGF, l’équipe de Ian Mohr [ 39, 40] a montré que pour maintenir la latence dans des cultures de neurones périphériques, le NGF doit agir en permanence sur le récepteur à activité tyrosine kinase TrkA, gardant ainsi active la voie de signalisation de la phosphoinositide 3-kinase (PI3K). L’activation de la PI3K induit le recrutement de la kinase PDK1 ( phosphoinositide-dependent kinase 1) à la membrane plasmique où elle phosphoryle la protéine kinase B (PKB, ou AKT). Après encore quelques étapes, cette voie de signalisation active le complexe mTORC1 ( mammalian target of rapamycin complex 1), centre névralgique cellulaire qui intègre des informations liées au stress, à l’état énergétique de la cellule, à la disponibilité de facteurs de croissance ou à l’intégrité du génome (Figure 4). Lorsqu’il est activé, le complexe mTORC1 phosphoryle (et donc inactive) une protéine inhibitrice de la traduction ( 4E-binding protein ou 4E-BP), sauvegardant ainsi le maintien de la synthèse de protéines cellulaires. Autrement dit, la privation de NGF ou l’inhibition de TrkA, de PI3K, de PDK1, de PKB, ou de mTORC1, ou encore l’inhibition de la synthèse de protéines, peuvent induire la réactivation du génome latent. Cette étude montre aussi que l’intensité et la durée de certaines de ces inhibitions peuvent jouer un rôle dans la réactivation. On ne sait pas encore comment l’arrêt de la synthèse protéique induit la réactivation, mais ces études montrent qu’un signal moléculaire qui a son origine dans les terminaisons nerveuses (l’absence de NGF) peut déclencher une chaîne de signaux qui atteignent les noyaux des neurones, induisant finalement la réactivation du génome viral. Il est intéressant de noter que la capsaïcine, une molécule irritante issue du piment et qui active des thermorécepteurs de type TRPV1 ( transient receptor potential vanilloid 1), peut, elle aussi, induire la réactivation du génome viral [ 41]. Cela pourrait expliquer pourquoi des stimulus comme la fièvre ou le choc thermique sont de puissants inducteurs de la réactivation. Ainsi, différents signaux environnementaux peuvent être perçus au niveau de récepteurs membranaires des neurones sensitifs, sont ensuite relayés le long des axones et, après plusieurs étapes, parviennent aux génomes viraux dont ils induisent la réactivation. D’autres inducteurs de la réactivation pourraient agir directement au niveau de mTOR (stress, privation en acides aminés) ou d’autres points de contrôle capables d’intégrer plusieurs types d’information, alors que d’autres encore (modulateurs épigénétiques) pourraient agir, à l’instar de la TSA, directement au niveau de la chromatine virale (Figure 4).
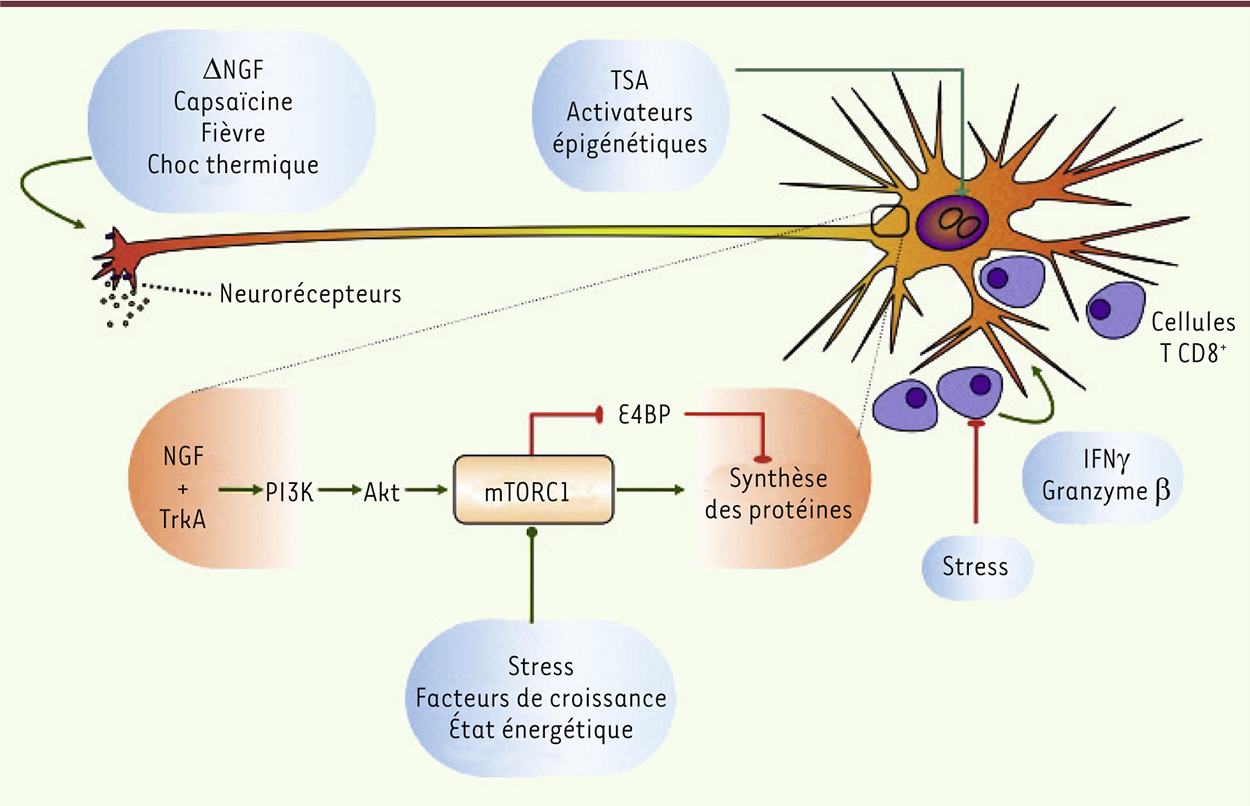
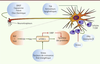 | Figure 4.
Multiples niveaux de contrôle de la réactivation. Cette figure illustre le fait que des stimulus capables de réactiver le génome latent peuvent agir à différents niveaux et sur différents types cellulaires. Certains stimulus (privation de NGF [nerve growth factor], capsaïcine, fièvre, choc thermique) agissent au niveau de récepteurs membranaires (pas nécessairement situés seulement au niveau des synapses), activant des voies de signalisation qui finissent par arriver au noyau et induisent la réactivation. Le bas du schéma (espace orange) résume la voie de signalisation du NGF, dont l’activation permanente du récepteur TrkA est nécessaire pour le maintien de la latence, et dont l’absence (ΔNGF) déclenche la réactivation. Dans cette voie de signalisation du NGF, l’activation de mTORC1 (mammalian target of rapamycin complex 1) est une étape particulièrement importante, compte tenu du rôle intégrateur de cette kinase. Il est possible que d’autres signaux activateurs (mais aussi inhibiteurs) de la réactivation (stress, déficit énergétique de la cellule, privation en facteurs de croissance, privation en acides aminés ou autres nutriments essentiels) puissent agir directement ou indirectement au niveau de mTORC1, ou au niveau d’autres molécules intégratrices de l’information, ou de la synthèse de protéines. Enfin, il est possible que d’autres stimulus puissent agir directement au niveau du génome viral, en modifiant sa configuration épigénétique, à l’instar de la tricostatine A (TSA) ou d’autres inhibiteurs des histone déacétylases. Les lymphocytes T CD8+, quant à eux, sont présents dans les ganglions sensitifs et jouent un rôle inhibiteur de la réactivation, que ce soit de manière directe ou via la sécrétion de l’IFNγ et du granzyme B. Le stress émotionnel pourrait avoir ainsi un double rôle, en tant qu’activateur direct de la réactivation et en tant que facteur immunosuppresseur. |
Étapes de la réactivation du génome viral Des données récentes indiquent que la réactivation du génome viral passe par au moins deux étapes [ 42, 43]. Lors de la première phase, on assiste à une transcription dérégulée, simultanée, des gènes très précoces, précoces et tardifs, et cela sans qu’il y ait de réplication de l’ADN viral. Cette observation, dont les bases moléculaires sont encore incomprises, contredit la théorie classique, qui veut que les gènes lytiques s’expriment de manière séquentielle et ordonnée, et que les gènes tardifs requièrent pour le faire la réplication de l’ADN, comme décrit précédemment. Cette première vague est suivie d’une diminution transitoire de la transcription des gènes lytiques, avant que ne démarre une deuxième phase d’expression, dépendante cette fois de l’activité de VP16 (synthétisée lors de la première phase) et qui prendra la forme d’une cascade régulée, similaire à celle qui prévaut au début de l’expression du programme lytique. Il est intéressant de noter que lors d’un stress inducteur, on observe également une migration de la protéine HCF1 vers le noyau des neurones sensitifs [ 44]. |
Même si la latence est un phénomène intrinsèque des neurones, comme le montrent les expériences in vitro, il est possible que certains stimulus inducteurs (ou répresseurs) de la réactivation n’agissent pas directement sur les neurones sensitifs, mais sur d’autres types cellulaires présents dans les ganglions. En effet, les ganglions sensitifs sont des tissus complexes contenant des cellules non neuronales, en particulier des cellules satellites et des lymphocytes T CD8+. La possibilité d’une action directe des cellules T pouvant entraver la réactivation en réponse à l’expression d’antigènes viraux [45] n’est pas exclue. Mais, des évidences suggèrent un rôle plus subtil de ces lymphocytes dans le maintien de la latence, via la sécrétion de molécules inhibitrices (granzyme B, IFNγ), capables de supprimer l’expression virale sans détruire le neurone [29, 46] (Figure 4). Des stress émotionnels, outre leur action comme inducteurs directs de la réactivation, pourraient également moduler l’immunité via la libération de peptides et d’hormones neuroendocrines. La puissance de l’inducteur que représente le stress pourrait donc s’expliquer par une double action, directe au niveau de la réactivation moléculaire, puis indirecte par la réduction des réponses défensives de l’hôte. |
Bien que des questions majeures restent encore sans réponse, les études réalisées récemment permettent de mettre en place les pièces qui composent un tableau compréhensible de la latence de HSV-1. Selon ce tableau, la latence et la réactivation ne sont pas des phénomènes de tout ou rien. Au contraire, notre perception actuelle indique que l’établissement, le maintien et la réactivation de la latence résultent de l’intégration d’un certain nombre de facteurs, favorables ou défavorables, informant à tout moment le génome viral de l’état général de l’hôte et de la cellule infectée, et permettant une réponse adéquate du virus, fruit d’une longue coévolution entre le virus et l’hôte. Ainsi, l’entrée ou le maintien du génome en latence, et donc la répression de la synthèse des protéines virales, seraient une adaptation permettant au virus d’échapper à la réponse immune spécifique de l’hôte ; la réactivation, quant à elle, serait une réponse adaptative permettant au génome de se propager à d’autres individus, lors de la reconnaissance d’une situation potentiellement dangereuse pour le neurone ou pour l’hôte, tels qu’un stress émotionnel, l’arrêt de la synthèse protéique cellulaire, ou la privation en facteurs de croissance. La phase de maintien elle-même n’est plus perçue comme une phase stable, mais plutôt comme une situation d’équilibre entre les forces favorisant le maintien de la latence et celles favorisant la réactivation, via le contrôle épigénétique de l’expression virale. Et il est possible que des stimulus de réactivation insuffisamment soutenus puissent induire un début de réactivation au niveau moléculaire, mais qui n’aboutira pas à la formation de particules infectieuses et qui serait réversible, le génome revenant à la situation de latence. La superposition de multiples niveaux de contrôle agissant à des étapes différentes (Figure 4) - incluant les réponses immunitaires innée et acquise - milite en faveur de cette hypothèse. D’où l’existence vraisemblable de plusieurs points de contrôle que le virus devra franchir avant de produire des nouvelles particules qui lui permettront de quitter l’hôte et de se propager. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
Footnotes |
1.
Roizman B, Knipe DM, Whitley RJ. Herpes simplex viruses . In : Knipe DM, Howley PM, eds. Fields virology. (5th ed.) , 5th ed. Philadelphia: : Lippincott Williams and Wilkins; , 2007 : :2501.–2602. 2.
Roizman B, Zhou G, Du T. Checkpoints in productive and latent infections with herpes simplex virus 1: conceptualization of the issues . J Neurovirol. 2011; ; 17 : :512.–517. 3.
Honess RW, Roizman B. Regulation of herpesvirus macromolecular synthesis. I. Cascade regulation of the synthesis of three groups of viral proteins . J Virol. 1974; ; 14 : :8.–19. 4.
Kent JR, Zeng PY, Atanasiu D, et al. During lytic infection herpes simplex virus type 1 is associated with histones bearing modifications that correlate with active transcription . J Virol. 2004; ; 78 : :10178.–10186. 5.
Herrera FJ, Triezemberg SJ. VP16-dependent association of chromatin–modifying coactivators and underrepresentation of histones at immediate-early gene promoters during herpes simplex virus infection . J Virol. 2004; ; 78 : :9689.–9696. 6.
Kalamvoki M, Roizman B. The histone acetyl transferase CLOCK is an essential component of the herpes simplex virus 1 transcriptome that includes TFIID, ICP4, ICP27 and ICP22 . J Virol. 2011; ; 85 : :9472.–9477. 7.
Liang Y, Vogel JL, Narayanan A, et al. Inhibition of the histone demethylase LSD1 blocks alpha-herpesvirus lytic replication and reactivation from latency . Nat Med. 2009; ; 15 : :1312.–1317. 8.
Boutell C, Sadis S, Everett RD. Herpes simplex virus type 1 immediate-early protein ICP0 and its isolated RING finger domain act as ubiquitin E3 ligases in vitro . J Virol. 2002; ; 76 : :841.–850. 9.
Boutell C, Everett RD. Regulation of alphaherpesvirus infection by the ICP0 family of proteins . J Gen Virol. 2013; ; 94 : :465.–481. 10.
Everett RD, Boutell C, Orr A. Phenotype of a herpes simplex virus type 1 mutant that fails to express immediate-early regulatory protein ICP0 . J Virol. 2004; ; 78 : :1763.–1774. 11.
Everett RD. The role of ICP0 in counteracting intrinsic cellular resistance to virus infection . In : Weller KS, ed. Alphaherpesviruses: molecular virology. Norfolk UK: : Caister Academic Press; , 2011 : :39.–50. 12.
Lomonte P, Thomas J, Texier P, et al. Functional interaction between class II histone deacetylases and ICP0 of herpes simplex virus type 1 . J Virol. 2004; ; 78 : :6744.–6757. 13.
Gross S, Catez F, Masumoto H, Lomonte P. Centromere architecture breakdown induced by the viral E3 ubiquitin ligase ICP0 protein of herpes simplex virus type 1 . PLoS One. 2012; ; 7 : :e44227.. 14.
Lilley CE, Chaurushiya M, Boutell C, et al. A viral E3 ligase targets RNF8 and RNF168 to control histone ubiquitination and DNA damage responses . EMBO J. 2010; ; 29 : :943.–955. 15.
Zhou G, Du T, Roizman B. The role of the CoREST/REST repressonr complex in herpes simplex virus A productive infection and in latency . Viruses. 2013; ; 5 : :1208.–1218. 16.
Roizman B, Sears AE. An inquiry into the mechanisms of herpes simplex virus latency . Annu Rev Microbiol. 1987; ; 41 : :543.–571. 17.
Hafezi W, Lorentzen EU, Eing BR, et al. Entry of herpes simplex virus type 1 (HSV-1) into the distal axons of trigeminal neurons favors the onset of nonproductive, silent infection . PLoS Pathog. 2012; ; 8 : :e1002679.. 18.
Kolb G, Kristie TM. Association of the cellular coactivator HCF1 with the Golgi apparatus in sensory neurons . J Virol. 2008; ; 82 : :9555.–9563. 19.
Lakin ND, Palmer R, Lillycrop KA, et al. Down-regulation of the octamer binding protein Oct1 during growth arrest and differentiation of a neuronal cell line . Brain Res Mol Brain Res. 1995; ; 28 : :47.–54. 20.
Stevens JG, Wagner EK, Devi-Rao GB, et al. RNA complementary to a herpesvirus alpha gene mRNA is prominent in latently infected neurons . Science. 1987; ; 235 : :1056.–1059. 21.
Wagner EK, Bloom DC. Experimental investigation of herpes simplex virus latency . Clin Microbiol Rev. 1997; ; 10 : :419.–433. 22.
Zabolotny JM, Krummenacher C, Frazer NW. The herpes simplex virus type 1 2.0-kilobase latency-associated transcript is a stable intron which branches at a guanosine . J Virol. 1997; ; 71 : :4199.–4208. 23.
Umbach JL, Kramer MF, Jurak I, et al. MicroRNAs expressed by herpes simplex virus 1 during latent infection regulate viral mRNAs . Nature. 2008; ; 454 : :780.–783. 24.
Tang S, Bertke AS, Patel A, et al. An acutely and latently expressed herpes simplex virus 2 viral microRNA inhibits expression of ICP34.5, a viral neurovirulence factor . Proc Natl Acad Sci USA. 2008; ; 105 : :10931.–10936. 25.
Pan D, Flores O, Umbach JL, et al. A neuron-specific host microRNA targets Herpes simplex virus-1 ICP0 expression and promotes latency . Cell Host Microbe. 2014; ; 15 : :446.–456. 26.
Perng GC, Jones C, Ciacci-Zanella J, et al. Virus-induced neuronal apoptosis blocked by the herpes simplex virus latency-associated transcript . Science. 2000; ; 287 : :1500.–1503. 27.
Thompson RL, Sawtell NM. Herpes simplex virus type 1 latency-associated transcript gene promotes neuronal survival . J Virol. 2001; ; 75 : :6660.–6675. 28.
Thompson RL, Sawtell NM. Replication of herpes simplex virus type 1 within trigeminal ganglia is required for high frequency but not high viral genome copy number latency . J Virol. 2000; ; 74 : :965.–974. 29.
Khanna KM, Lepisto AJ, Decman V, Hendricks RL. Immune control of herpes simplex virus during latency . Curr Opin Immunol. 2004; ; 16 : :463.–469. 30.
Margolis TP, Imai Y, Yang L, et al. Herpes simplex virus type 2 (HSV-2) establishes latent infection in a different population of ganglionic neurons than HSV-1: role of latency-associated transcripts . J Virol. 2007; ; 81 : :1872.–1878. 31.
Sawtell NM. Comprehensive quantification of herpes simplex virus latency at the single-cell level . J Virol. 1997; ; 71 : :5423.–5431. 32.
Catez F, Picard C, Held K, et al. HSV-1 genome subnuclear positioning and associations with host-cell PML-NBs and centromeres regulate LAT locus transcription during latency in neurons . PLoS Pathog. 2012; ; 8 : :e1002852.. 33.
Sawtell NM, Poon DK, Tansky CS, Thompson RL. The latent herpes simplex virus type 1 genome copy number in individual neurons is virus strain specific and correlates with reactivation . J Virol. 1998; ; 72 : :5343.–550. 34.
Deshmane SL, Frazer NM. During latency, herpes simplex virus type 1 DNA is associated with nucleosomes in a chromatine structure . J Virol. 1989; ; 63 : :943.–947. 35.
Kubat NJ, Amelio AL, Giordani NV, Bloom DC. The herpes silplex virus type 1 latency-associated transcript (LAT) enhancer/rcr is hyperacetylated during latency independently of LAT transcription . J Virol. 2004; ; 78 : :12508.–12518. 36.
Cliffe AR, Garber DA, Knipe DM. Transcription of the herpes simplex virus latency-associated transcript promotes the formation of facultative heterochromatin on lytic promoters . J Virol. 2009; ; 83 : :8182.–8190. 37.
Amelio AL, Giordani NV, Kubat NJ, et al. Deacetylation of the herpes simplex virus type 1 latency-associated transcript (LAT) enhancer and a decrease in LAT abundance precede an increase in ICP0 transcriptional permissiveness at early times postexplant . J Virol. 2006; ; 80 : :2063.–2068. 38.
Wilcox CL, Johnson EM. Characterisation of nerve growth factor-dependent herpes simplex virus latency in neurons in vitro . J Virol. 1988; ; 62 : :393.–399. 39.
Camarena V, Kobayashi M, Kim JY, et al. Nature and duration of growth factor signaling through receptor tyrosine kinases regulates HSV-1 latency in neurons . Cell Host Microbe. 2012; ; 8 : :320.–330. 40.
Kobayashi M, Wilson AC, Chao MV, et al. Control of viral latency in neurons by axonal mTOR signaling and the 4E-BP translation repressor . Genes Dev. 2012; ; 26 : :1527.–1532. 41.
Hunsperger EA, Wilcox CL. Capsaicin-induced reactivation of latent herpes simplex virus type 1 in sensory neurons in culture . J Gen Virol. 2003; ; 84 : :1071.–1078. 42.
Du Te, Zhou G, Roizman B. HSV-1 gene expression from reactivated ganglia is disordered and concurrent with suppression of latency-associated transcripts and miRNA . Proc Natl Acad Sci USA. 2011; ; 108 : :18820.–18824. 43.
Kim JY, Mandarino A, Chao MV, et al. Transient reversal of episome silencing precedes VP16-dependent transcription during reactivation of latent HSV-1 in neurons . PLoS Pathog. 2012; ; 8 : :e1002540.. 44.
Whitlow Z, Kristie TM. Recruitment of the transcriptional coactivator HCF-1 to viral immediate-early promoters during initiation of reactivation from latency of herpes simplex virus type 1 . J Virol. 2009; ; 83 : :9591.–9595. 45. St Leger AJ, Hendricks RL. CD8 T cells patrol HSV-1-infected trigeminal ganglia and prevent viral reactivation . J Neurovirol. 2011; ; 17 : :528.–534. 46.
Knickelbein JE, Khanna KM, Yee MB, et al. Noncytotoxic lytic granule-mediated CD8+T cell inhibition of HSV-1 reactivation from neuronal latency . Science. 2008; ; 322 : :268.–271. 47.
Maraoui MA, El Asmi F, Dutrieux, et al. Implication des corps nucléaires PML dans l’immunité intrinsèque et innée . Med Sci (Paris). 2014; ; 30 : :765.–771. 48.
Bertin A, Mangenot S. Structure et dynamique de la particule cœur de nucléosome . Med Sci (Paris). 2008; ; 24 : :715.–719. |