Activité physique : Prévention et traitement des maladies chroniques
2019
→ Aller vers ANALYSE
À tous les âges, chez les personnes en bonne santé ou atteintes de maladies chroniques, les bénéfices de la pratique d’une activité physique pour la prévention, le traitement des maladies chroniques et l’amélioration de la qualité de vie des personnes qui en sont atteintes, l’emportent sans conteste sur les risques encourus.
Ainsi, selon l’expertise de l’Anses 2016
1
Anses. Actualisation des repères du PNNS – Révisions des repères relatifs à l’activité physique et à la sédentarité. Avis de l’Anses, Rapport d’expertise collective, février 2016.
qui reprend les résultats de l’expertise Inserm 2008
2
Inserm. Activité physique. Contextes et effets sur la santé. Collection Expertise collective. Paris : Éditions Inserm, 2008.
qu’elle complète par une revue des publications depuis cette date, « une activité physique régulière et le suivi des recommandations sont associés à une diminution de la mortalité précoce comprise entre 29 et 41 % selon les études ».
Au cours des deux dernières décennies, dans les pays anglo-saxons notamment, la recherche a permis d’en identifier les avantages selon les types d’exercice physique (dimension cardiorespiratoire, force musculaire, souplesse et coordination, composante neuropsychologique) et les conditions de mise en œuvre au regard de l’état de santé des personnes et de leurs besoins. Des guides de prescription ont été élaborés et permettent aux professionnels de santé et aux professionnels du sport de proposer des programmes adaptés d’activité physique.
Dans la première partie de la synthèse, nous présenterons les enjeux de la pratique d’activité physique en analysant la progression des pathologies chroniques, la place de l’activité dans le parcours de soins et de santé des malades chroniques, les déterminants de l’adoption par les personnes atteintes de maladies chroniques d’un comportement actif, pérenne et inséré dans les habitudes de vie. Nous verrons enfin ce que peut apporter la compréhension des mécanismes moléculaires et cellulaires capables de rendre compte des bénéfices de l’activité physique. La seconde partie sera consacrée à l’évaluation du bénéfice/risque de la pratique d’activité physique et des programmes d’activité physique en fonction des différentes pathologies chroniques.
I. Enjeux de la pratique d’activité physique
dans les pathologies chroniques
La prévalence des maladies chroniques augmente partout dans le monde alors qu’une prévention est possible à tout moment de leur évolution
Selon le rapport 2014 de l’Organisation mondiale de la santé (OMS), les maladies chroniques non transmissibles sont responsables de 38 des 56 millions de morts en 2012 au niveau mondial, soit 68 %, dont 40 % d’entre elles étaient des décès prématurés (avant l’âge de 70 ans). Le nombre de décès dus aux maladies chroniques pourrait atteindre 52 millions en 2030. Les quatre maladies non transmissibles les plus fréquentes (pathologies cardiovasculaires, cancers, maladies respiratoires chroniques et diabètes) sont responsables de 82 % de cette mortalité. La charge associée à ces maladies et leurs complications mesurées en années de vie en incapacité montre également une très forte augmentation, 587,6 millions en 1990 et 764,8 millions en 2013 dans le monde, en relation avec l’accroissement de la population mondiale et son vieillissement.
L’augmentation de l’espérance de vie s’accompagne
d’une augmentation des années de vie en incapacité
En Europe, selon le rapport de l’OMS de 2012, « les maladies non transmissibles concourent à près de 86 % des décès et 77 % de la charge des maladies, et pèsent de plus en plus lourdement sur les systèmes de santé, le développement économique et le bien-être d’une grande partie de la population, en particulier chez les personnes âgées de 50 ans et plus ».
En France, la part des personnes âgées de 60 ans et plus devrait passer d’un quart en 2015 à un tiers de la population en 2040. Avec l’augmentation de l’espérance de vie, le nombre de personnes âgées atteintes par les pathologies chroniques ne cesse de progresser. Le nombre de personnes dépendantes passerait de 1,2 million en 2012 à 2,3 millions en 2060.
Le constat d’un accroissement important des maladies chroniques interpelle d’autant plus que, selon le rapport de l’OMS (2010) qui résume l’état des connaissances dans le domaine, un large pourcentage de ces maladies est accessible à la prévention par des actions sur quatre facteurs de risque principaux : consommation de tabac, inactivité physique
3
Dans le rapport de l’OMS, le facteur de risque « inactivité physique » inclut la sédentarité.
, consommation d’alcool et mauvaise nutrition. Ces actions de prévention peuvent être mises en œuvre en amont des maladies (prévention primaire) mais aussi à tout moment de l’évolution de ces maladies (prévention secondaire et tertiaire). Or, les maladies chroniques et leurs complications sont des contributeurs majeurs à l’état de dépendance. La prévention des récidives et des complications de ces maladies est de ce fait un enjeu central pour le maintien de l’autonomie notamment chez les personnes âgées.
Connaître et anticiper les évolutions des pathologies chroniques constituent un préalable dans le cadre de ce travail. Les principales pathologies retenues par l’OMS étudiées dans cette expertise sont les pathologies cardiovasculaires, les cancers, le diabète, les pathologies respiratoires chroniques. L’obésité en tant que déterminant de maladies chroniques et phénomène morbide en soi rentre aussi dans le cadre de cette expertise. Enfin, sont également prises en compte certaines maladies mentales : dépression et schizophrénie, ainsi que les troubles musculo-squelettiques (TMS)
4
Dans la bibliographie anglo-saxonne, les TMS regroupent la plupart du temps les troubles, les symptômes, les maladies musculaires et ostéoarticulaires. Lorsque cette bibliographie s’intéresse aux TMS liés à l’activité professionnelle, elle parle spécifiquement de « work related musculoskeletal disorders », ou de « musculoskeletal disorders of occupationnal medicine » alors qu’en France les TMS se réduisent la plupart du temps aux seuls TMS d’origine professionnelle. Ici c’est le sens large, anglo-saxon des TMS qui est retenu. Le chapitre spécifique concernant ces pathologies est d’ailleurs intitulé pathologies ostéo-articulaires.
et la multimorbidité.
On observe un fort accroissement de l’incidence de la plupart
des maladies chroniques avec l’âge mais une baisse importante
de la mortalité pour les maladies cardiovasculaires et la plupart
des cancers
À l’exception de quelques pathologies chroniques, telles que la schizophrénie ou l’asthme, l’incidence des maladies chroniques retenues dans le cadre de cette expertise augmente avec l’âge : les cardiopathies ischémiques, les accidents vasculaires cérébraux, l’insuffisance cardiaque, la bronchopneumopathie chronique obstructive, la plupart des cancers, le diabète, les maladies musculo-squelettiques et la multimorbidité. Avec le vieillissement de la population et l’allongement de l’espérance de vie, le nombre de personnes atteintes d’une ou plusieurs maladies chroniques ne cesse et ne va cesser de croître dans les prochaines décennies, occasionnant une augmentation de la proportion des personnes atteintes de limitations fonctionnelles et des activités quotidiennes ou essentielles et entraînant une dégradation de leur qualité de vie.
La mortalité de la plupart des maladies chroniques est en baisse depuis plusieurs décennies dans les pays à fort niveau de revenus. C’est le cas, en France, pour les pathologies qui sont responsables des deux plus grandes causes de mortalité : les maladies cardiovasculaires et les cancers. Les causes de cette décroissance relèvent à la fois d’une meilleure prévention et d’une meilleure prise en charge (détection plus précoce et traitements plus efficaces). C’est le cas pour les maladies cardiovasculaires. La mortalité par cardiopathies ischémiques a baissé de 52 % chez les femmes et de 48 % chez les hommes entre 2002 et 2012. Pour les accidents vasculaires cérébraux, cette baisse est de 42,6 % chez les femmes et de 40,1 % chez les hommes entre 2000 et 2013 et pour les insuffisances cardiaques, les taux de mortalité ont également décru régulièrement de 3 % par an entre 2000 et 2010. De même pour les cancers, leur mortalité globale a baissé entre 1980 et 2012 de 214,6 à 133,6 pour 100 000 chez les hommes et de 100,4 à 73,2 pour 100 000 chez les femmes. Cependant, une analyse plus fine montre que la mortalité de certains cancers est restée stable ou a augmenté comme c’est le cas du cancer du poumon chez la femme.
La mortalité de la bronchopneumopathie chronique obstructive ne montre qu’une faible décroissance chez les hommes (-1 % par an) entre 2000 et 2013 alors qu’elle augmente chez les femmes de 1 % par an sur cette période.
Si la mortalité toutes causes est en forte baisse, les taux d’hospitalisation, proxy
5
Variable qui est une approximation de l’incidence. Le taux d’hospitalisation est une variable qui approche l’incidence, de manière plus ou moins fiable selon la pathologie. Pour une pathologie dont les recommandations sont d’hospitaliser les patients (AVC par exemple), le taux d’hospitalisation sera une bonne approximation de l’incidence ; pour une maladie où cela n’est pas le cas, ce sera une moins bonne approximation et le taux d’hospitalisation sous-estimera l’incidence.
de l’incidence, montrent des évolutions différentielles selon les pathologies, les classes d’âge et le sexe. Ainsi, en France pour les infarctus du myocarde entre 2002 et 2008, la baisse nette des hospitalisations observée chez les plus de 65 ans (-23 % chez les hommes et les femmes) s’est nettement ralentie entre 2008 et 2013 (-1,7 % chez les hommes et -1,1 % chez les femmes). Chez les moins de 65 ans, ce taux d’hospitalisation est à la hausse : + 9,9 % pour les hommes et + 19,9 % pour les femmes. Des tendances similaires sont observées dans le cas des hospitalisations pour les accidents vasculaires cérébraux. Si une légère diminution des taux de personnes hospitalisées pour accidents vasculaires cérébraux a été observée entre 2002 et 2008 (-2,6 %), le taux entre 2008 et 2014 semble aujourd’hui plutôt stable (+ 1,6 %). Cependant, cette tendance globale recouvre des disparités importantes selon l’âge : après 65 ans, les taux standardisés sont restés stables entre 2008 et 2014 (± 1 %), mais avant 65 ans, ils ont augmenté de 8 %. L’évolution entre 2000 et 2014 a été marquée par une augmentation des taux standardisés d’hospitalisation pour exacerbation de bronchopneumopathie chronique obstructive chez les hommes (+ 2 % par an en moyenne) comme chez les femmes (+ 6 % par an). Les taux spécifiques d’hospitalisations croissent avec l’âge et sont, à âge égal, deux à trois fois supérieurs chez les hommes.
Ces dernières décennies, la prévalence de l’obésité et du diabète présente de très fortes augmentations même si elles semblent se ralentir voire, ces dernières années se stabiliser. À âge égal, plus la cohorte de naissance est récente plus l’indice de masse corporelle (IMC) est élevé chez les hommes comme chez les femmes. Selon les enquêtes ObÉpi, en 2012, 32,3 % des Français adultes de 18 ans et plus sont en surpoids (25 ≤ IMC < 30 kg/m2) et 15 % présentent une obésité (IMC ≥ 30 kg/m2). Le nombre de personnes obèses en 2012 est estimé à environ 6 922 000, ce qui correspond à 3 356 000 personnes supplémentaires par rapport au chiffre de 1997. En France, selon Santé publique France, la prévalence du diabète traité pharmacologiquement est estimée en 2013 à 4,7 % de la population. La prévalence du diabète ne cesse d’augmenter depuis les premières estimations établies en 2000 à partir des données de l’Assurance maladie. Toutefois, cette progression enregistre un ralentissement : le taux de croissance annuel est ainsi passé de 5,4 % sur la période 2006-2009 à 2,3 % sur la période 2009-2013.
Pour ce qui est des cancers, l’amélioration de la survie est générale, sauf quelques exceptions la plus notable étant le cancer du poumon, et les incidences de la plupart des cancers sont au mieux stables.
Des différences entre hommes et femmes qui s’amenuisent
L’incidence et la mortalité de la plupart des maladies chroniques sont plus importantes chez les hommes que chez les femmes. C’est le cas des maladies cardiovasculaires, de la bronchopneumopathie chronique obstructive, de nombreuses localisations de cancers, du diabète, mais l’écart se réduit. Depuis une décennie, on observe chez les femmes une réduction moindre ou une augmentation plus forte des facteurs de risque tels que le tabagisme et l’obésité qui sont des déterminants des maladies chroniques et qui expliqueraient le comblement de cet écart et surtout le regain de morbidité par maladies cardiovasculaires et accidents vasculaires cérébraux ainsi que d’incapacités observé entre 50 et 65 ans, regain beaucoup plus perceptible chez elles que chez les hommes.
Des inégalités sociales qui persistent pour la plupart des maladies chroniques
Les prévalences et les incidences de la plupart des maladies chroniques (maladies cardiovasculaires, certains cancers, diabète et obésité...) sont très corrélées au gradient social.
Ainsi par exemple et sans être exhaustif pour l’infarctus du myocarde, les taux standardisés d’hospitalisation sont 35 % supérieurs et les taux de mortalité 50 % supérieurs dans le quintile de la population la plus défavorisée socialement comparé au quintile de la population la plus favorisée. Pour les accidents vasculaires cérébraux, les taux d’hospitalisation et la mortalité sont respectivement de + 14 % et de + 35 % entre les deux quintiles extrêmes. Ce gradient existe également pour la bronchopneumopathie chronique obstructive où la mortalité varie de 50 décès pour 100 000 à 75 pour 100 000 dans ces quintiles opposés. Pour l’asthme, le différentiel est de 18,6 pour 100 000 chez les personnes bénéficiant de la CMU-C
6
Couverture maladie universelle complémentaire.
, mutuelle complémentaire des plus démunis, contre 7,6 pour 100 000 pour les personnes dont les ressources sont suffisamment élevées pour ne pas en bénéficier.
Ce gradient a été largement documenté pour l’obésité et le diabète, avec pour le diabète la particularité qu’il est plus prononcé chez les femmes que chez les hommes alors que c’est l’inverse pour les autres maladies.
La mise en œuvre de recommandations concernant l’activité physique chez les personnes atteintes devra donc veiller à ne pas aggraver les inégalités sociales de santé et si possible les réduire.
La multimorbidité s’accroît fortement car les maladies chroniques
ont des facteurs de risque communs
La surveillance épidémiologique de la multimorbidité comme un indicateur de l’état de santé de la population permet de compléter les informations apportées par la surveillance des maladies chroniques considérées séparément. En effet, les personnes souffrant de plusieurs maladies chroniques nécessitent des prises en charge globales et adaptées à leur état de santé. Les pathologies chroniques les plus fréquentes partagent un certain nombre de facteurs de risque communs : l’obésité, la consommation de tabac, la sédentarité et l’inactivité physique. La prévention dans ce contexte est un enjeu majeur et les actions de prévention sur ces facteurs communs auront un impact sur l’ensemble des maladies impactées par ces déterminants.
La mortalité par maladies chroniques est en forte baisse depuis plusieurs décennies. Les gains considérables d’espérance de vie du xxe et de ce début du xxie siècles qui ont été acquis en bonne santé se font aujourd’hui, au prix d’une augmentation de l’espérance de vie en incapacité. La forte hausse des prévalences des maladies chroniques pèse lourd en termes d’incapacité, de dépendance, de qualité de vie altérée pour les personnes qui en sont atteintes et de coûts directs et indirects pour la société. Dans ce contexte, les bénéfices multiples de l’activité physique chez les personnes atteintes de maladies chroniques doivent être pris en compte à toutes les étapes de leurs parcours de soins.
L’institutionnalisation de l’activité physique
dans les politiques publiques bouscule les pratiques
L’intervention en activité physique, aujourd’hui intégrée dans le parcours de soins, a acquis une légitimité scientifique et institutionnelle dans la prise en charge des maladies chroniques. Le nombre de travaux sociologiques sur cette intégration est encore limité mais on peut cependant en proposer une lecture synthétique en distinguant trois niveaux d’analyse auxquels correspondent les institutions, les organisations et les professions qui sont appréhendées dans le cadre d’écologies liées.
L’activité physique comme objet d’action publique : un processus long marqué par les rapprochements interministériels
Les maladies chroniques sont progressivement devenues un enjeu prioritaire des politiques et plans de santé publique. Parallèlement, l’éducation thérapeutique s’est développée à la fin des années 1990, puis s’est structurée pour prendre sa place dix ans plus tard dans la prise en charge médicale de ces maladies.
Au début des années 2000 émerge en France le Programme national nutrition santé (PNNS), qui fait de la lutte contre le surpoids et l’obésité une cause nationale et met progressivement l’accent sur la promotion de l’activité physique et la réduction de la sédentarité. Le travail de préparation d’un Plan national de prévention par les activités physiques ou sportives (PNAPS), porté par le ministère de la Santé, de la Jeunesse, des Sports et de la Vie associative constitue une étape importante dans la montée en puissance de la question de l’activité physique. Si le PNAPS n’a pas été suivi d’une mise en œuvre, l’activité physique devient un axe à part entière du troisième volet du PNNS (2011-2015), mettant définitivement en exergue le processus d’inclusion de l’activité physique dans les politiques publiques de santé, essentiellement en prévention primaire des pathologies chroniques. Mais c’est par le biais de la prévention tertiaire que s’institutionnalise véritablement l’activité physique dans le parcours de soins en France, à partir d’initiatives de terrain initialement portées par des équipes de soin, dans le cadre des dispositifs innovants des réseaux de santé ou des unités transversales d’éducation hospitalières. L’action publique en matière d’activité physique s’est ainsi progressivement construite à partir des années 2000 en s’appuyant sur les innovations professionnelles et la légitimation scientifique des bénéfices de l’intervention en activité physique auprès des personnes atteintes de maladies chroniques.
Le Plan national sport santé bien-être (SSBE), mis en place en 2012, constitue la première politique publique exclusivement centrée sur la promotion des activités physiques et sportives (APS). Il prolonge l’approche socio-sportive préalablement portée par les politiques locales, en visant les publics éloignés de la pratique sportive : publics avançant en âge, porteurs de maladies chroniques, handicapés ou précaires. Malgré les différents plans nationaux prenant en compte l’activité physique en tant qu’outil de prévention et de promotion de la santé (PNNS, Plan Obésité, Plan Bien-vieillir, Plan Cancer), constat est fait qu’une grande partie de la population n’accède pas réellement, ni durablement à la pratique d’activité physique, en particulier les publics les plus vulnérables.
Peu de travaux publiés ont jusqu’ici étudié la mise en place du Plan SSBE, mais les recherches en sciences sociales qui analysent les politiques de santé, insistent sur l’importance de sa gouvernance régionale, niveau d’application des plans nationaux jugé le plus pertinent, et sur l’importance des politiques de la ville à l’échelon local.
Le texte relatif à l’activité physique, promulgué dans la loi de modernisation du système de santé du 26 janvier 2016, a été adopté le 27 novembre 2015 à l’unanimité avec l’amendement 144 de l’article L. 1172-1. Il stipule que « dans le cadre du parcours de soins des patients atteints d’une affection de longue durée (ALD), le médecin traitant peut prescrire une activité physique adaptée à la pathologie, aux capacités physiques et au risque médical du patient. Les activités physiques adaptées sont dispensées dans des conditions prévues par décret ».
Après les débats qui ont suivi l’adoption de cet amendement, centrés autour de la prise en charge financière de ces prescriptions ainsi que sur les aptitudes des professionnels à accueillir les patients, un décret et une instruction précisent les conditions de mise en œuvre de l’article.
Le décret no 2016-1990 « relatif aux conditions de dispensation de l’activité physique adaptée prescrite par le médecin traitant à des patients atteints d’une affection de longue durée », est adopté le 30 décembre 2016 et publié au Journal officiel le lendemain pour entrer en vigueur le 1er mars 2017. Il précise notamment la liste des « limitations classées comme sévères pour les patients porteurs d’affections de longue durée au regard des altérations fonctionnelles, sensorielles, cérébrales et du niveau de douleur ressentie » au regard desquelles sont définis les professionnels (et bénévoles de l’encadrement sportif) aptes à intervenir.
Ce décret a enfin été suivi par une instruction aux agences régionales de santé (ARS) et aux directions régionales de la jeunesse, des sports et de la cohésion sociale (DRJSCS), validée le 3 mars 2017, destinée à faciliter la mise en œuvre et l’accessibilité du dispositif dans les territoires.
Les dispositifs d’intervention en activité physique portés
par les organisations : entre tradition et innovation
Les organisations qui développent une intervention en activité physique pour des personnes vivant avec une maladie chronique sont aujourd’hui multiples. Elles relèvent de l’hospitalisation publique et privée, des réseaux de santé, des communautés professionnelles regroupant des professionnels libéraux, mais également du secteur associatif comme du secteur commercial non médical. Ces organisations ne touchent pas les mêmes publics, ne mobilisent pas des professionnels identiques et s’inscrivent dans des logiques d’intervention diversifiées.
La cardiologie et la diabétologie se distinguent dans la littérature sociologique par leur rôle précurseur et complémentaire dans l’intégration de l’activité physique dans le monde médical.
La cardiologie a été l’une des premières spécialités à contribuer au développement des politiques de santé préventive à vocation populationnelle et à légitimer la promotion de l’activité physique dans le cadre de la promotion de la santé. Outre son impact sur la santé publique, la cardiologie a également participé à l’intégration d’interventions en activité physique dans le cadre des prises en charge curatives et éducatives des pathologies cardiaques, en particulier dans les consultations de dépistage, en soins de suite et de réadaptation et dans les Clubs cœur et santé pour accompagner les personnes malades dans leur réadaptation cardiaque. Le réentraînement et la réadaptation à l’effort par un exercice prescrit constituent des modèles de référence prioritaires de l’intervention en activité physique en cardiologie. Ils visent une reconstruction de l’autonomie des patients sous contrôle médical, tandis que la promotion de l’activité physique par l’information et l’éducation apparaissent comme des pratiques complémentaires plus ou moins juxtaposées à l’activité principale.
La diabétologie a quant à elle intégré l’activité physique dans un mouvement réformateur initié par une mise en doute de la capacité de l’approche médicale traditionnelle à traiter la maladie chronique. Elle a activement participé au développement de dispositifs innovants permettant un mode de travail transversal par la mobilisation et la coordination de l’ensemble des acteurs. Il s’agit de produire des soins de long terme, dans une proximité avec le lieu de vie du patient et en cohérence avec son projet personnel. Du point de vue de l’activité physique, la structure associative d’aide aux jeunes diabétiques (AJD), a joué un rôle important dans le déplacement du regard médical d’une contre-indication de la pratique sportive à son indication aux jeunes patients diabétiques vers la fin des années 1970. Ce déplacement s’est ensuite généralisé au monde adulte en tant que droit à une vie sportive, avant que l’activité physique ne devienne objet d’éducation thérapeutique pour les diabétiques de type 1, puis pour les diabétiques de type 2. L’intervention en activité physique adaptée a ainsi été portée par une dynamique collective pluridisciplinaire d’empowerment des patients.
Trois modèles d’intervention en activité physique ont pu être distingués dans les dispositifs initialement inventés par les équipes de coordination des réseaux de santé : 1) le modèle de la prescription de l’activité physique qui place le médecin au centre tandis que les professionnels du secteur paramédical et enseignants en activité physique adaptée (APA) se consacrent à des activités d’information-explication et de soutien de la motivation du patient ; 2) le modèle de l’incitation par une expérience pratique ponctuelle dont les objectifs sont de rassurer le patient sur ses capacités et de l’engager dans une pratique régulière autonome selon la technique du « pied dans la porte » ; 3) le modèle de l’éducation via l’expérience prolongée de situations d’enseignement en activité physique adaptée qui développent les ressources physiques, motrices, psychologiques et culturelles du patient. Les deux premiers modèles relèvent d’une conception spontanéiste de l’autonomie qui considère qu’il suffit que le patient soit informé des bénéfices de l’activité physique pour qu’il décide d’en pratiquer et qu’il change ses habitudes de vie. Le troisième modèle relève d’une conception interventionniste qui conçoit que l’autonomie en activité physique ne va pas de soi pour tous et qu’elle peut être (re)construite dans le cadre d’une intervention éducative.
Une seconde forme de réseaux spécifiquement dédiés au sport santé, comme les réseaux Efformip et Champagne-Ardenne, a commencé à se structurer en dehors des équipes pluridisciplinaires de soins, à partir de 2005. Le Plan SSBE a finalement contribué à une généralisation de ces modèles. Ils proposent une évaluation de la condition physique et de la motivation des patients et leur orientation vers des associations locales en réseau ou vers des ateliers passerelles, selon les résultats de l’évaluation.
Ils ont également inspiré une troisième forme de dispositifs moins médicalisés, portés par les politiques locales, comme celui expérimenté par la ville de Strasbourg intitulé « Sport santé sur ordonnance » (SSSO). Il vise à promouvoir la prescription de l’activité physique par les médecins généralistes à des personnes vivant avec une maladie chronique stabilisée, et à développer une offre locale de pratique de sport santé permettant de mettre en œuvre la prescription. Cette initiative entend « contrer les inégalités sociales et territoriales de santé ou d’accès à l’activité physique ».
Les premiers dispositifs sont développés dans des organisations sanitaires (réseaux et pôles de santé, services médicaux des établissements de santé, maisons pluridisciplinaires de santé) sous la forme d’une approche intégrée aux soins. Les suivants relèvent des politiques régionales et locales et soutiennent une forme de délégation du service d’intervention en activité physique sur prescription médicale.
Le rôle de la prescription dans la pratique d’une activité physique a été étudié en particulier au Danemark et en Nouvelle-Zélande. Une ordonnance écrite aurait en moyenne deux fois plus de chances d’être convertie en actes qu’un conseil oral. Les effets seraient encore multipliés dans le cadre de ce qu’ils dénomment la « green prescription » dont l’objectif et les modalités de l’activité physique sont discutés avec le patient et ancrés dans ses envies, ses motivations et son parcours de soin. Mais l’étude danoise souligne qu’une formation à la prescription d’activité physique pour les médecins généralistes est nécessaire si l’on veut améliorer l’observance et la durabilité de l’activité physique pratiquée. Cette compétence, qui n’est aujourd’hui que très peu prise en compte dans les facultés de médecine française, fait défaut aux médecins généralistes qui, en majorité, ne savent pas comment ni quoi prescrire.
Travail et dynamique des professions : émergence du groupe professionnel des professionnels de l’activité physique adaptée
Les interventions en activité physique se sont développées dans le cadre des nouvelles pratiques professionnelles interdisciplinaires d’éducation thérapeutique, portées par les équipes de coordination des réseaux de santé. Les informations et recommandations s’étant révélées très peu efficaces, l’intervention pratique auprès des patients a été jugée nécessaire. L’objectif ne pouvait pas être celui de faire faire de l’exercice. Il s’agissait au contraire de développer une pratique durable autonome qui ne se confonde pas avec celle de la rééducation, mais qui puisse lui succéder ou se développer en parallèle en fonction de l’évolution de la maladie. Il a donc été jugé utile de recruter des professionnels 1) spécialisés dans l’encadrement des APS (dans le respect du Code du sport) ; 2) formés à l’éducation et à l’enseignement pour développer les ressources et transformer les savoir-faire ; 3) compétents dans l’adaptation des contenus aux capacités, besoins et attentes des personnes fragilisées par la maladie, de manière à contrôler la balance risques-bénéfices des pratiques. Les discours consacrant l’émergence d’un nouveau groupe professionnel dans les réseaux de santé se sont structurés avec la création de l’Association des éducateurs médico-sportifs (ADEMS) en 2005. Ils ont été progressivement relayés par ceux de la Société française des professionnels de l’activité physique adaptée (SFP-APA) créée en 2008, soulignant l’ancrage historique de cette triple compétence dans les formations universitaires en activité physique adaptée et les recherches pluridisciplinaires en STAPS (Sciences et techniques des APS).
Entre diplômes nationaux, diplômes d’État et formations fédérales, les formations aux métiers de l’encadrement des APS tels qu’ils sont répertoriés dans le décret no 2016-1990 sont multiples et renvoient à des niveaux de formation et de qualification disparates. Tandis que la formation universitaire en activité physique adaptée (niveau de qualification II voire I) est ciblée sur l’intervention auprès de publics malades, vieillissants et/ou en situation de handicap, celle des éducateurs sportifs (niveau de qualification IV) n’est pas spécialisée sur un public à besoins spécifiques. Pour autant les professionnels de l’encadrement des APS sont invités par le décret à un travail de définition de territoire en fonction de la sévérité des limitations fonctionnelles des publics. Ces professionnels des APS introduits, aux côtés de professions paramédicales établies et réglementées dans le secteur sanitaire, se sont retrouvés confrontés à des conflits de juridiction. Lors de l’élaboration du décret, l’État devenu « auditoire » des groupes professionnels a produit une délimitation souple des territoires dont il sera intéressant d’évaluer l’impact sur les dynamiques engagées.
En plaçant la prescription du médecin généraliste au centre du dispositif d’intervention sur l’activité physique des personnes atteintes de maladies chroniques, la nouvelle loi de santé va-t-elle infléchir l’activité de travail, les dynamiques professionnelles et les dispositifs d’intervention ?
Les enjeux de l’intervention en activité physique adaptée : animer, entraîner ou enseigner ?
Les logiques d’intervention qui transparaissent dans la revue de littérature sociologique se caractérisent par une grande variabilité en fonction des organisations dans lesquelles elles s’exercent (établissements de santé, réseaux de santé, organisations sportives, associations de patients, organisations privées commerciales...), en fonction des niveaux d’échelle de l’intervention (échelle de l’État, politiques territoriales, collectivités locales) et en fonction des groupes professionnels impliqués, coordonnés ou non entre eux.
Dans les dispositifs de droit commun, les interventions tendent à se limiter à l’encadrement d’exercices plus ou moins en lien avec des APS. La réalisation des exercices est appréhendée comme bénéfique en soi, produisant spontanément santé, estime de soi, soutien social, qualité de vie... À ces temps de pratique sont parfois juxtaposés des temps d’information et de recommandations pour ériger l’exercice en norme de santé.
Dans les établissements de santé, les interventions tendent à dépasser le simple encadrement d’APS. Deux grandes logiques se distinguent dont nous avons pu étudier les ancrages historiques dans les spécialités médicales. La première, celle de l’entraînement, consiste à s’appuyer sur la recherche expérimentale pour définir la quantité et l’intensité de l’activité physique nécessaires pour un bénéfice sur la santé. Ces données définissent des situations d’entraînement que le patient est invité à suivre dans le cadre d’une thérapeutique non médicamenteuse. On lui apprend ainsi « par corps » l’exercice auquel il devra s’autocontraindre au nom de sa santé. En fin de prise en charge médicale, le professionnel procède alors par délégation de responsabilité. Le malade averti et instruit « n’a plus qu’à » reproduire l’exercice régulièrement en s’appuyant ou non sur des organisations comme les Clubs cœur et santé en cardiologie. Cette approche repose sur une vision fonctionnaliste du corps et sur la conception de l’homme libre de ses choix, rationnel dans ses décisions et réactif à la peur engendrée par le risque. Cette conception s’avère plus adaptée aux classes moyennes citadines prédisposées à intégrer dans la routine des activités quotidiennes les préconisations du programme d’exercice.
La seconde logique, celle de l’enseignement, repose sur une inversion totale du processus qui va d’abord viser l’engagement dans une pratique d’activité physique adaptée qui était initialement considérée comme improbable. Les questions de la durée et de l’intensité de l’exercice, si elles s’appuient sur les recommandations médicales, sont alors abordées à partir de l’expérience du sujet et construites avec lui. L’importance est donnée au développement de capabilités mobilisables à partir du libre arbitre de l’individu. Il ne s’agit donc pas d’animer pour faire bouger, mais d’enseigner dans le cadre de situations d’apprentissage et d’accompagner la construction d’un projet individuel qui s’appuie sur des pratiques culturelles partageables. Cette logique demande que l’intervention se déroule dans la durée (sur plusieurs mois) pour que le processus d’engagement puisse s’enclencher.
L’intervention sur le « bouger » en prévention tertiaire remet en question les conditionnements spatiotemporels qui organisent la place et la surveillance des corps dans l’espace social. Exiger d’un groupe qu’il se mette à bouger, c’est changer les règles de l’usage social des corps dans leur espace privé comme dans les espaces publics de déplacement, d’interaction sociale et de travail, où la mobilité est habituellement d’autant plus réduite que les publics sont malades et/ou âgés.
L’enjeu majeur de la pratique d’activité physique
chez les personnes atteintes de maladies chroniques
est la motivation et l’adhésion à une activité physique régulière
L’engagement des personnes atteintes de maladie chronique dans une activité physique régulière est principalement motivé par le plaisir et l’intérêt qu’elles y trouvent. Un autre facteur primordial d’engagement renvoie à leurs croyances en termes de bénéfices perçus, aussi bien pour leur santé physique que pour leur bien-être psychologique. À l’inverse, le manque de connaissances sur les effets positifs de la pratique de l’activité physique, ou des croyances défavorables selon lesquelles celle-ci serait inutile dans la gestion de leur pathologie, peuvent être à l’origine de l’absence d’initiation ou de maintien de sa pratique.
Les patients peuvent également être motivés par l’image de soi positive que leur renvoie le fait de pratiquer (ou la vision négative qu’ils auraient d’eux-mêmes en l’absence de pratique). Plus particulièrement, le fait de devoir se prendre en main pour faire face à sa pathologie est vécu par certains comme une responsabilité ou un devoir.
Les principales barrières à la pratique de l’activité physique sont liées à l’état de santé, en particulier à la douleur et à la fatigue ressenties, parfois en raison d’effets secondaires de certains traitements. Le fait de pratiquer non pour soi, mais pour faire plaisir à autrui, ou répondre à une pression sociale, est un facteur défavorable à long terme. De même, les risques perçus à ne pas pratiquer semblent avoir peu de lien avec l’adoption d’une activité physique.
Les croyances des individus en leurs capacités à pratiquer des activités physiques, en particulier dans des circonstances contraignantes, représentent un déterminant très important. Ces croyances peuvent être réduites chez les personnes atteintes de maladie chronique, du fait de leur état de santé, en raison des limites propres à leur environnement, ou parce que l’activité physique est susceptible d’entrer en concurrence avec d’autres activités et rôles qu’elles ont à assumer (responsabilités familiales et professionnelles).
L’environnement social peut influencer de façon plus ou moins favorable la motivation de ces personnes, en fonction des messages adressés et des comportements adoptés. Les personnes ayant potentiellement le plus d’impact sur la motivation et la pratique effective d’une activité physique dans cette population incluent le corps médical, les professionnels supervisant la pratique d’activité physique, les pairs (autres personnes atteintes de la même pathologie), et la famille.
Enfin, si les intentions et la planification sont le plus souvent une étape incontournable afin de permettre l’initiation de la pratique, la création de routines s’avère par la suite une nécessité pour que l’activité physique devienne un comportement adopté de façon habituelle.
La plupart de ces constats relatifs à la motivation s’appliquent de façon transversale aux personnes atteintes de différentes maladies chroniques, bien que certaines dimensions ou barrières s’expriment de façon plus ou moins marquée selon les individus (selon leur âge, leur niveau de revenu ou d’éducation, leur genre et leur pathologie).
Concernant les modalités de pratique, des différences inter-individuelles importantes ont été identifiées. Les personnes atteintes de maladie chronique témoignent de préférences très variées en matière d’activité physique réalisée, ou de contexte (pratique individuelle ou collective avec d’autres patients ou dans un groupe de pratiquants tout-venant).
Enfin, un certain nombre de techniques d’intervention ont été identifiées comme des leviers efficaces pour favoriser la motivation des personnes atteintes de maladies chroniques envers la pratique de l’activité physique, que ce soit en cours de réhabilitation, en post-réhabilitation ou dans le cadre des soins courants. Leur efficacité sur la motivation est plus importante lorsque plusieurs d’entre elles sont utilisées ensemble.
|
Techniques permettant d’agir sur la motivation
Information : donner et rappeler des informations sur les effets bénéfiques de l’activité physique, sur un ensemble de dimensions (biologiques, psychologiques et sociales), et les mettre en lien avec les situations vécues et changements constatés sur soi.
Opportunités : proposer différentes possibilités de pratique d’activité physique, permettant de prendre en compte les goûts individuels et les préférences personnelles (nature de l’activité, supervision ou pratique autonome, pratique conjointe avec d’autres patients ou non).
Anticipation et gestion des barrières : anticiper individuellement les barrières à l’activité physique, les conflits potentiels entre l’activité physique et les autres buts et activités, anticiper la possibilité que la personne ne pratique plus d’activité physique pendant certaines périodes ; prévoir la meilleure façon de faire face à ces événements pour l’individu.
Fixation d’objectifs : choix personnel de la nature, fréquence, intensité, durée de l’activité physique pratiquée ; rappel des objectifs fixés et des séances prévues ; mettre en place un système pour que les personnes reçoivent des feedback leur permettant d’évaluer leur évolution vers leurs objectifs et reçoivent des encouragements.
Monitoring : suivi de l’adoption du comportement d’activité physique, pouvant être réalisé par la personne (tenue d’un journal) ou un membre de son entourage ; parfois enregistré avec l’aide d’outils technologiques.
Rappel d’expérience : se remémorer une situation personnelle vécue comme une expérience positive de pratique d’activité physique, ou comme une réussite dans ses tentatives d’inscrire l’activité physique dans son nouveau style de vie, constitue une aide lors de phases de découragement.
Partage d’expérience : témoignage d’autres patients indiquant avoir rencontré les mêmes difficultés ou doutes vis-à-vis de la pratique d’activité physique, ayant constaté des bénéfices d’une pratique d’activité physique durable, ou ayant réussi à mettre en place le comportement de façon régulière.
Soutien social : soutien de la démarche et encouragements par les proches, voire pratique conjointe de l’activité physique. Inclut également le soutien de l’environnement médical et d’autres professionnels.
Réévaluation cognitive : travail sur les pensées récurrentes à l’égard de l’activité physique afin de favoriser une évolution d’un versant négatif – tourné sur les coûts et les risques vers des pensées positives – tournées vers les capacités et les bénéfices.
Entretien motivationnel : méthode clinique d’accompagnement du changement de comportement, basée sur une approche non directive et dans laquelle le processus s’appuie sur l’initiative du patient, la minimisation de la résistance au changement et la prise en compte de son ambivalence.
|
|
Connaître les mécanismes moléculaires et cellulaires en jeu dans le déconditionnement musculaire et dans l’activité physique permet de comprendre comment agit l’activité physique
Les pathologies chroniques entraînent un déconditionnement musculaire qui détériore la qualité de vie des patients, et qui peut être directement associé à une augmentation de la mortalité.
Chez l’humain, le maintien d’une fonction musculaire normale (homéostasie musculaire) est indispensable à la vie de relation et à l’autonomie fonctionnelle. Les pathologies chroniques vont être à l’origine d’un déconditionnement musculaire plus ou moins marqué. Celui-ci va contribuer à une réduction progressive des capacités fonctionnelles de l’organisme, une sédentarisation croissante, et une perte d’autonomie imposant une prise en charge institutionnelle des personnes affectées.
On peut identifier deux formes principales de déconditionnement musculaire, la sarcopénie et la cachexie. La sarcopénie est identifiée comme un syndrome gériatrique, alors que la cachexie est d’abord un syndrome métabolique. Ces processus sont caractérisés par une perte de force musculaire et de masse musculaire, mais la cachexie se caractérise par un développement plus rapide du déconditionnement musculaire. Généralement, la perte de force musculaire peut s’observer avant que la perte de masse musculaire ne soit décelable.
Les données de la littérature indiquent que toutes les pathologies chroniques envisagées dans le cadre de cette expertise s’accompagnent d’un déconditionnement musculaire. Celui-ci est particulièrement bien documenté pour la bronchopneumopathie chronique obstructive, les cancers, l’insuffisance cardiaque et jusqu’à un certain point pour le diabète de type 2 et l’accident vasculaire cérébral, alors que les données de la littérature sont beaucoup plus rares pour les maladies mentales et la polyarthrite rhumatoïde. Dans certaines pathologies chroniques (bronchopneumopathie chronique obstructive, cancer, insuffisance cardiaque), le déconditionnement musculaire est associé à une augmentation de la mortalité des patients, mettant clairement en évidence l’intérêt thérapeutique que peuvent constituer des approches visant à limiter ou prévenir le déconditionnement musculaire.
L’ampleur et les conséquences du déconditionnement musculaire dépendent aussi de l’existence ou non d’un terrain pathologique sous-jacent et de l’âge des personnes affectées par ce déconditionnement. Par exemple, l’évolution du déconditionnement musculaire associé à l’âge (sarcopénie) est plus rapide chez des patients diabétiques comparativement à des sujets non diabétiques de même âge.
Mécanismes en jeu dans le déconditionnement musculaire en fonction des pathologies
La connaissance des mécanismes mis en jeu dans le déconditionnement musculaire est essentielle dans un premier temps pour déterminer si ces mécanismes sont régulés par l’activité physique, et dans un deuxième temps pour déterminer quelles modalités d’exercice musculaire et d’entraînement peuvent réguler de façon favorable ces mécanismes.
Les études fondamentales de ces 15 dernières années conduites sur des modèles animaux ont permis d’identifier de nombreux acteurs moléculaires du déconditionnement musculaire. Même si le rôle d’un certain nombre d’entre eux reste encore à préciser chez l’humain, nous pouvons aujourd’hui sur la base de ces données présenter un schéma cohérent des acteurs moléculaires du déconditionnement musculaire pour certaines pathologies chroniques.
La dérégulation du contrôle de la balance entre la synthèse des protéines (axe Akt-mTOR
7
Akt-mTOR : Protein kinase B – Mammalian Target of Rapamycin.
de la voie IGF-1-Akt
8
IGF-1 : Insulin-like Growth Factor 1.
) et la dégradation des protéines (axe Akt-FoxO
9
de la voie IGF-1-Akt) constitue un mécanisme clé de ce déconditionnement. L’axe Akt-FoxO contribue à la régulation transcriptionnelle de 2 voies majeures de la protéolyse intracellulaire, le système ubiquitine-protéasome et le système autophagie-lysosome. Cette dérégulation, caractérisée par l’inhibition de l’axe Akt-mTOR et l’activation de l’axe Akt-FoxO, est en effet maintenant bien documentée pour la cachexie associée au cancer et celle associée à l’insuffisance respiratoire ou cardiaque. Par contre, les données cliniques font toujours défaut dans le contexte de l’accident vasculaire cérébral, celui des pathologies mentales ou encore celui de la polyarthrite rhumatoïde. Toutefois, les données expérimentales obtenues dans les modèles animaux de ces pathologies témoignent également d’une inhibition de la synthèse des protéines (axe Akt-mTOR) et d’une activation de la dégradation des protéines (axe Akt-FoxO). Enfin, alors que l’implication du système ubiquitine-protéasome a été bien démontrée (cancers, bronchopneumopathie chronique obstructive, insuffisance cardiaque), l’implication fonctionnelle et le rôle précis du système autophagie-lysosome dans ces pathologies restent pour l’essentiel à déterminer.
Même si les effets du stress oxydatif sur la régulation de l’homéostasie musculaire ne sont pas clairement établis, il apparaît aussi qu’une augmentation du stress oxydatif serait un acteur potentiel du déconditionnement musculaire au moins dans certaines pathologies comme la bronchopneumopathie chronique obstructive, les cancers, l’insuffisance cardiaque ou encore le diabète de type 2.
Il est important de souligner qu’en fonction de la vitesse d’évolution du déconditionnement musculaire, les cinétiques de régulation de ces mécanismes peuvent être différentes. On doit aussi considérer l’existence de fenêtres temporelles où les mécanismes du déconditionnement musculaire sont plus particulièrement activés, par exemple lors d’épisodes de décompensation dans le parcours de la pathologie. Dans ces conditions, des mécanismes moléculaires de lutte contre le déconditionnement peuvent même être activés (par exemple activation de l’axe Akt-mTOR chez le patient atteint de bronchopneumopathie chronique obstructive).
L’augmentation de l’expression de la myostatine, un régulateur négatif de la masse musculaire, constitue également une signature moléculaire commune à de nombreuses pathologies, et qui a été mise en évidence pour la bronchopneumopathie chronique obstructive, les cancers, l’accident vasculaire cérébral, l’insuffisance cardiaque ou encore le diabète de type 2. L’augmentation de l’expression de la myostatine peut réguler en aval la synthèse et la dégradation des protéines. D’autres facteurs circulants comme les cytokines pro-inflammatoires (Interleukine-1β, Interleukine-6 ou TNF-α
10
TNF-α : Tumor Necrosis Factor α.
) seraient également des régulateurs en amont des mécanismes intracellulaires du déconditionnement musculaire.
Enfin, il faut souligner que très peu de données cliniques sont disponibles pour les pathologies mentales et la polyarthrite rhumatoïde. Toutefois, sur la base des quelques études disponibles, on peut raisonnablement considérer que l’augmentation de l’expression de la myostatine et l’activation du système ubiquitine-protésome seraient impliquées dans le déconditionnement musculaire associé à ces pathologies.
Mécanismes moléculaires par lesquels l’activité physique améliore
les symptômes et la qualité de vie des patients
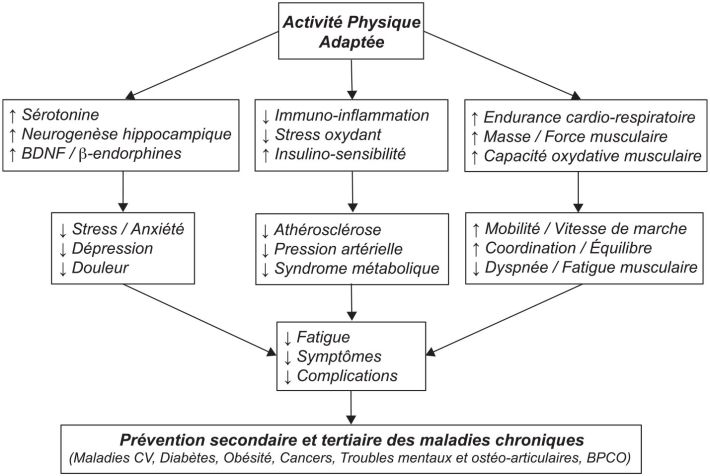
Les maladies chroniques s’accompagnent sur le long terme d’un déconditionnement musculaire et d’une augmentation de la masse grasse, en partie dus à la mobilité réduite et à une baisse de l’activité physique quotidienne. Les effets bénéfiques de l’activité physique sont très largement multifactoriels et impliquent plusieurs mécanismes d’action notamment sur les muscles squelettiques locomoteurs (figure ci-dessous

). Le type d’exercice physique est également déterminant dans les adaptations physiologiques observées. Les exercices d’endurance améliorent la fonction cardiaque et la résistance à la fatigue des muscles locomoteurs, tandis que les exercices de renforcement musculaire augmentent la masse et la force musculaires. Il est désormais établi que le muscle squelettique est également capable de communiquer à distance avec d’autres organes par l’intermédiaire de facteurs sécrétés,
i.e. les myokines. Bien que le répertoire des myokines soit en cours d’élaboration, des études récentes ont identifié plusieurs myokines capables de cibler l’hippocampe pour moduler la mémoire et la dépression (BDNF, GDNF
11
BDNF : Brain-Derived Neurotrophic Factor et GDNF : Glial cell Derived Neurotrophic Factor.
), le foie pour moduler la production hépatique de glucose (Interleukine-6), les muscles pour moduler la sensibilité à l’insuline (apeline), ainsi que de nombreux autres tissus et organes. Une partie des effets bénéfiques de l’activité physique s’explique également par son effet anti-inflammatoire au niveau systémique et par la production de facteurs analgésiques (β-endorphines, substance P). Les recherches futures devraient s’orienter vers l’identification de nouvelles myokines et des types d’exercices physiques les mieux adaptés à la prise en charge de chaque pathologie chronique.
II. programmes d’activité physique et pathologies chroniques
L’activité physique peut jouer un rôle central
dans l’ajustement psychologique du patient à sa maladie chronique
Faire adopter de nouveaux comportements vis-à-vis de l’activité physique nécessite de bien cerner ce qui se joue dans l’ajustement psychologique à une maladie chronique.
Différentes phases d’ajustement psychologique se succèdent suite à l’annonce du diagnostic. Ces phases dont la durée varie d’un individu à l’autre font partie d’un processus général appelé appropriation de la maladie chronique qui évite au patient de basculer dans la résignation. Ce processus exige une démarche active et éclairée de la part du patient et fait appel à cinq facteurs psychosociaux clés : les émotions positives, la flexibilité cognitive, le sens donné à l’existence, le soutien social et les stratégies actives pour faire face au stress. La pratique d’activité physique adaptée va jouer un rôle de facilitateur dans cette appropriation en favorisant par exemple l’introspection, les feedbacks sensoriels, la production d’affects positifs, une diminution du stress, la consolidation de l’estime de soi...
Une maladie chronique entraîne des erreurs de jugement de la part des patients entre leur niveau réel de pratique d’activité physique et la perception qu’ils en ont, ou entre leur capacité physique réelle et leur capacité perçue. Ces biais de perception résultent d’un processus de déconditionnement qui s’installe progressivement et insidieusement, peut-être avant même le diagnostic de la maladie. Dans une maladie comme la bronchopneumopathie chronique obstructive par exemple, c’est une sensation d’asphyxie provoquée par un effort physique, appelée dyspnée, qui active ce processus. Le patient évite alors tout effort physique autant par anticipation anxieuse de cette sensation que par sous-estimation de ses capacités. Ce cercle vicieux du déconditionnement provoque des répercussions qui vont bien au-delà de l’organe lésé et/ou de la fonction touchée, on parle de retentissements systémiques.
Un patient atteint de maladie chronique doit faire face aux éventuels effets secondaires ou séquelles des traitements et gérer l’évolution de sa maladie avec l’avancée en âge. Celle-ci peut se traduire par l’apparition d’autres maladies appelées comorbidités dont le risque de survenue est d’autant plus grand que les personnes sont âgées et/ou sédentaires. Une étude sur une population représentative montre que 23,2 % des patients ont plus de deux pathologies chroniques. D’autres problèmes de santé peuvent également survenir comme des symptômes anxio-dépressifs et des dysfonctionnements neurocognitifs. Des difficultés socioéconomiques peuvent se surajouter et aggraver la vulnérabilité de la personne. La pratique régulière de programmes personnalisés d’activité physique va permettre d’alléger ce fardeau en prévenant, retardant ou soulageant l’ensemble de ces complications.
De nombreuses études utilisant une méthodologie rigoureuse comme l’essai randomisé contrôlé démontrent les bénéfices de programmes en activité physique sur des variables psychologiques intégrées comme la qualité de vie, le bien-être, l’estime de soi, la fatigue, le stress et la symptomatologie anxio-dépressive chez différentes populations de patients atteints de maladies chroniques.
Des études d’implémentation montrent que la réussite des programmes d’activités physiques adaptées auprès des patients dépend en partie des compétences de l’encadrant comme l’empathie, la bienveillance, la capacité d’écoute et l’éthique. De même, le choix de l’intensité de l’effort physique perçu est important car il a un impact sur le maintien à long terme de la pratique. Un effort perçu comme trop intense provoque une réponse émotionnelle qui réduit les chances de maintien dans une pratique régulière après 6 mois.
Les connaissances des effets de l’activité physique sur la psychologie des personnes souffrant de maladie chronique pourraient être améliorées en s’affranchissant de différents biais de publications (études non publiées, études majoritairement nord-américaines...), ou méthodologiques (biais de sélection, sous-analyse d’essais médicamenteux, type de groupe contrôle, utilisation d’outils de mesure peu fiables et/ou sensibles), et en proposant une meilleure description des programmes d’activité physique. Des études interventionnelles restent nécessaires sur des marqueurs neurocognitifs (par exemple, ressources attentionnelles), émotionnels (kinésiophobie) et comportementaux (tabagisme).
Obésité : les activités d’endurance d’intensité modérée
à forte ont montré leur efficacité pour diminuer la masse grasse viscérale
L’obésité est caractérisée par une accumulation progressive de tissu adipeux au sein de l’organisme résultant principalement d’un déséquilibre important de la balance énergétique. Il est établi que cet excès de graisse, notamment au niveau abdominal, est associé à l’apparition de pathologies métaboliques, dont le diabète de type 2.
Chez les personnes obèses, selon une méta-analyse récente qui inclut 10 études de cohorte prospectives, avoir une bonne condition physique ou une pratique d’activité physique importante réduit la mortalité toutes causes indépendamment de l’indice de masse corporelle. Ainsi, les patients obèses actifs présentent un risque relatif de mortalité identique aux individus normo-pondérés. Pour autant, même en bonne condition physique, les personnes obèses conservent un risque supérieur aux sujets normo-pondérés de développer des pathologies cardiovasculaires ou un diabète de type 2. La pratique d’une activité physique aérobie ou combinée (aérobie et renforcement musculaire) améliore la condition physique chez les adultes obèses. Celle-ci, évaluée par l’augmentation du V̇O
2max, semble plus sensible à l’intensité qu’au volume global d’activité physique. En effet, on observe un effet dose-réponse pour une augmentation d’activité physique d’intensité modérée à forte
12
Les termes activité physique intense ou activité physique d’intensité élevée ou soutenue sont également utilisés.
.
Chez la personne adulte obèse, femme ou homme, le niveau d’activité physique globale évalué par accéléromètre est plus faible que chez des adultes normo-pondérés avec moins de pratique d’activités physiques modérées et fortes et plus de temps sédentaire. Cette pratique plus faible pourrait s’expliquer en partie par un coût énergétique plus élevé lors de l’activité physique chez le patient obèse. La prise en compte du caractère compliqué ou non de l’obésité est important. En effet, les patients obèses métaboliquement sains pratiquent une activité physique à des doses supérieures aux patients obèses non métaboliquement sains. Certaines complications pourraient également restreindre la pratique d’activité physique telles que la dyspnée d’effort, la présence d’arthroses ou de tendinites ou encore la sarcopénie chez le sujet âgé. Pour autant, les résultats des études randomisées ne rapportent pas de risques majorés lors de la pratique d’activité physique dès lors que l’intensité de l’exercice physique n’est pas maximale.
Mettre l’accent sur la diminution du tour de taille comme paramètre
de suivi plutôt que sur la perte de poids
Chez les patients obèses, l’effet de l’activité physique seule sur la perte de poids reste modeste quelle que soit la durée du programme. Seuls les programmes en aérobie et combiné engendrent une perte de poids avec une efficacité plus marquée des programmes proposant des exercices physiques à forte intensité. Le volume global de l’activité physique n’apparaît pas comme un facteur majeur, probablement parce qu’il induit des phénomènes de compensation (apport calorique augmenté). En fait, comme souligné dans la position de consensus de l’EASO (European Association for the Study of Obesity) en 2014, la prise en charge chez les patients obèses ne doit plus se focaliser sur la perte de poids mais sur la diminution du tour de taille et les changements de composition corporelle : diminution de masse grasse et prise de masse musculaire et amélioration des facteurs de risque cardiovasculaires. Chez les patients obèses, les exercices en endurance doivent être considérés comme la clé de voûte de tout programme visant à la perte de masse grasse notamment viscérale, facteur majeur de risque cardiovasculaire. Des activités physiques d’endurance d’intensité modérée à forte ont un effet plus marqué que des intensités plus faibles et sont donc préconisées. Quelques études randomisées contrôlées récentes suggèrent une efficacité supérieure des protocoles intensifs intermittents mais non épuisants sur la diminution de masse grasse en comparaison avec les intensités modérées continues. Pour autant, leur recommandation reste prématurée au vu du trop faible nombre d’études.
Cette perte de masse grasse viscérale peut être obtenue sans perte de poids associée. L’exercice aérobie semble même plus efficace que la diète pour diminuer la masse grasse viscérale. Non seulement les exercices en endurance limitent la reprise de poids après un programme hygiéno-diététique ou post-chirurgie bariatrique mais ils contribuent aussi sur le long terme au maintien de la diminution de la masse grasse viscérale.
Baser des recommandations sur le suivi de la perte de masse grasse viscérale apparaît difficile d’un point de vue pratique. Cependant, prendre en compte la diminution du tour de taille, indicateur indirect représentatif de la masse grasse abdominale, représente le critère idéal de suivi. Mais pour l’instant, il n’existe pas de données sur un potentiel effet dose entre l’activité physique et la diminution du tour de taille. Par conséquent, il n’est pas possible à ce jour de proposer des programmes sur une dose efficace pour la réduction du tour de taille.
Si les exercices de renforcement musculaire ont peu d’effet sur la perte de masse grasse, ils ont des effets intéressants sur le maintien et la prise de masse musculaire. Ainsi, les programmes devraient intégrer ce type d’exercices. Cependant, associer des exercices de renforcement musculaire avec des exercices aérobies (programme combiné) diminue les gains sur la masse grasse notamment viscérale. Pour autant, il existe relativement peu de données dans la littérature sur les effets de programme combiné associant exercices en endurance et en renforcement musculaire.
Effets bénéfiques de l’activité physique sur l’obésité
|
Niveau de preuve*
|
Effet bénéfique
|
|
A
|
Baisse de la masse grasse viscérale suite à un programme aérobie
Maintien du poids après perte de poids initiale
|
|
B
|
Baisse de la mortalité toutes causes
Perte de poids
Diminution du tour de taille
|
* Les niveaux de preuve sont ceux retrouvés dans la littérature, issus des classifications des différentes sociétés savantes ou évalués par les experts selon les recommandations de la HAS ; Cotation des niveaux de preuve selon les recommandations de la HAS : A : Preuve scientifique établie ; B : Présomption scientifique ; C : Faible niveau de preuve scientifique.
L’obésité est également associée à des facteurs de risque cardiovasculaires. L’activité physique seule permet de les réduire. En effet, les exercices en endurance diminuent les pressions artérielles, mais principalement chez les personnes obèses avec des niveaux de pression artérielle élevée en début de programme. De plus, l’activité physique en endurance réduit la stéatose hépatique non-alcoolique avec un effet dose-réponse. Le statut inflammatoire, la dysfonction endothéliale et le profil lipidique athérogène s’améliorent avec l’activité physique seule quelle que soit la modalité de pratique. Il importe de noter que les effets rapportés sont faibles à modérés pour tous les facteurs de risque cardiovasculaires. De manière intéressante, l’activité physique seule chez les personnes obèses est associée à une amélioration de la sensibilité à l’insuline, quelle que soit la modalité d’exercice physique réalisé. Elle diminue ainsi le risque de développer un diabète de type 2 chez ces patients.
Diabète de type 2 : la pratique d’une activité physique améliore le contrôle glycémique
L’introduction de l’activité physique dans le triptyque de la prise en charge du diabète, au même titre que la modification du régime alimentaire et le traitement médicamenteux est relativement récente. Cette approche non pharmacologique est un élément fondamental pour lutter contre la maladie et ses complications. Ces dernières sont principalement cardiovasculaires et dégénératives (rétinopathie, neuropathie, néphropathie) et définissent la sévérité de la maladie et son influence sur la vie quotidienne du patient.
Selon les trois méta-analyses les plus récentes, la pratique d’une activité physique par le patient diabétique de type 2 réduit le risque de mortalité toutes causes (entre -30 et -40 %), mais aussi celui de mortalité cardiovasculaire (-25 à -40 %), première cause de décès chez ces patients.
Une méta-analyse récente et deux études incluant un nombre important de patients montrent que la dose d’activité physique est fondamentale : une plus grande diminution de la mortalité est observée chez les patients les plus actifs. Par conséquent, il importe d’augmenter le niveau d’activité physique des patients, très souvent rapporté comme étant bien inférieur aux recommandations des sociétés savantes.
Pour obtenir une baisse significative de l’hémoglobine glyquée,
les meilleurs programmes d’activités physiques sont ceux associant
le renforcement musculaire et une activité d’endurance
Les effets de l’activité physique chez le patient diabétique de type 2 ont fait l’objet de très nombreuses études randomisées et contrôlées et qui ont également été compilées lors de plusieurs méta-analyses de grande ampleur depuis 2006. Les résultats sont particulièrement intéressants sur le contrôle de la glycémie, largement reconnue comme un facteur de risque majeur d’apparitions des complications de cette pathologie. L’homéostasie glycémique doit donc être un des objectifs principaux visé dans la prise en charge par l’activité physique. Son évaluation est aujourd’hui rendue possible sur une période longue de 8 à 12 semaines grâce à la mesure de l’hémoglobine glyquée (HbA1c). Cette dernière est également un très bon marqueur des complications à long terme. Une réduction de 0,6 % de l’HbA1c est considérée comme cliniquement significative et peut être un objectif de la prise en charge. Les programmes d’activités physiques en endurance, de renforcement musculaire ou une combinaison de ces deux types d’activités ont démontré des effets bénéfiques sur l’HbA1c, notamment pour des intensités modérées à élevées. Les programmes combinés associant activités physiques aérobies et de renforcement musculaire en comparaison avec un seul type d’activité (avec ou sans régime hypocalorique associé à l’exercice) semblent présenter les meilleurs résultats (niveau de preuve B). Les effets les plus significatifs sont retrouvés chez les patients présentant les niveaux d’HbA1c les plus importants et cette amélioration de l’équilibre glycémique par l’activité physique permet un allègement du traitement médicamenteux. Cette baisse des niveaux d’HbA1c s’explique par la diminution de la production hépatique du glucose, l’amélioration du transport et de l’utilisation du glucose dans le muscle et surtout la réduction de l’insulino-résistance.
Effet plus attendu, la prise en charge par l’activité physique concourt également à une amélioration de la condition physique des patients, et par conséquent à une diminution des facteurs de risque cardiovasculaires, notamment lorsque des activités en endurance sont proposées.
Le peu de travaux et la faible population de patients inclus dans les études ne permettent pas encore de recommander l’utilisation des programmes intermittents à haute intensité, mais d’après les dernières études, les meilleures améliorations des capacités fonctionnelles, notamment cardiorespiratoires, sont obtenues avec les niveaux d’intensité d’exercice les plus importants. Les programmes basés essentiellement sur des exercices de renforcement musculaire ont une incidence moindre sur la diminution du risque cardiovasculaire. Ces améliorations physiologiques et des capacités fonctionnelles sont indispensables puisqu’elles sont associées à une meilleure qualité de vie, notamment chez les patients avec les niveaux de condition physique les plus élevés.
Enfin, il faut rappeler qu’en plus des risques cardiovasculaires, les personnes atteintes de diabète de type 2 peuvent présenter de nombreuses complications spécifiques à la pathologie, notamment les neuropathies qui affectent plus de 40 % des patients. Les épisodes d’hypo- ou d’hyperglycémies en cours ou à proximité de l’effort questionnent parfois la prescription de l’activité physique chez ces patients. Néanmoins, de manière globale, les travaux disponibles démontrent clairement que les bénéfices liés à la pratique d’une activité physique contrebalancent significativement et très rapidement après le début de la prescription les événements indésirables ou les aggravations des complications existantes. Dans ce sens, les activités physiques en charge de type marche ou course à pied peuvent être envisagées même lorsque l’on s’adresse à des patients avec des antécédents d’ulcérations du pied parfaitement cicatrisés.
Effets bénéfiques de l’activité physique sur le diabète de type 2
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Baisse de la mortalité toutes causes et de la mortalité cardiovasculaire
Amélioration de l’équilibre glycémique (HbA1c)
|
|
B
|
Amélioration de la capacité aérobie (activités en endurance) et de la force musculaire (activités de renforcement musculaire)
Contrôle du poids
Pas d’apparition ou d’aggravation des complications
|
Avec l’ensemble de ces éléments, les dernières recommandations internationales pour les patients diabétiques de type 2 s’accordent pour recommander un volume hebdomadaire de 2,5 heures à des intensités modérées à fortes en associant des exercices d’endurance et de renforcement musculaire.
Si les activités sont plutôt réalisées à une intensité faible à modérée, il sera nécessaire d’augmenter le volume de pratique à 3,5 heures (210 minutes) par semaine. Les recommandations d’activités physiques « douces » (yoga, tai chi...) existantes pour les personnes âgées peuvent être transférables aux patients diabétiques, surtout chez les plus de 65 ans (niveau de preuve C).
Les caractéristiques des activités physiques permettent la mise en place de programmes d’activités physiques adaptées en fonction des capacités individuelles des patients et des niveaux de complications, de leurs besoins et attentes, de l’évaluation de leurs progrès ainsi que de l’environnement de pratique.
Pour savoir comment fidéliser le patient, installer et favoriser la continuité de l’activité physique sur l’ensemble de la vie, l’étude de la mise en œuvre de ces recommandations est absolument nécessaire. Dans ce sens, les effets à long terme de l’activité physique demandent à être mieux documentés. Enfin, au-delà des programmes individualisés et supervisés qui démontrent leur efficacité dans ce domaine, l’augmentation de l’activité spontanée de la vie quotidienne et le développement spécifique de programmes d’activité physique adaptée doivent être une priorité dans la prise en charge des patients diabétiques de type 2.
Bases théoriques des caractéristiques de la prise en charge par l’activité physique pour les patients diabétiques de type 2
|
Type d’exercice
|
Intensité préconisée
|
Durée totale* par semaine
|
Fréquence
|
|
Activités permettant de développer l’endurance (capacité aérobie)
Exercices impliquant une masse musculaire importante
|
Modérée à forte : 60-90 % FCmax
RPE : 5 à 8
Faible à modérée : < 40-60 % FCmax
RPE : < 5
Haute intensité intermittent > 100 % FCmax
RPE : 9-10
|
Minimum 2,5 h pour les intensités modérées à forte
Objectif de 3,5 h par semaine si l’intensité est faible à modérée pour toutes les séances
|
3 séances par semaine minimum
Possibilité de fractionner les exercices en plusieurs sessions de 10 min par jour (surtout pour les hautes intensités intermittentes)
Jamais 48 h sans exercice
|
|
Activités permettant de développer le renforcement musculaire
Exercices progressifs impliquant des groupes musculaires importants
|
Modérée à forte : > 50-75 1-RM
> 75 % 1-RM optimal pour la sensibilité à l’insuline
8 à 10 exercices différents
2 à 4 séries
8 à 10 répétitions
1 à 2 min repos
| |
2 séances par semaine au minimum
|
|
Activité permettant de développer la souplesse et l’équilibre
|
Faibles, activités « alternatives »
Prise en compte des patients vieillissants
|
60 minutes en plus
|
1 séance par semaine minimum
|
* activités d’endurance et de renforcement musculaire ; FCmax : fréquence cardiaque maximale ; RPE : échelle de pénibilité subjective de l’effort ; 1-RM : charge maximale.
Pathologies coronaires : les bénéfices de l’activité physique peuvent être optimisés en jouant sur l’intensité d’exercice
Le syndrome coronaire aigu, avec ou sans infarctus du myocarde, signe l’entrée du patient dans la pathologie coronaire. Plus de 7 millions de personnes souffrent d’un syndrome coronaire aigu dans le monde chaque année. Le taux de mortalité à un an est aujourd’hui de l’ordre de 10 %. Chez les patients qui survivent, 20 % souffrent d’un deuxième événement cardiovasculaire au cours de la première année. Dans ce cadre, la prévention par l’exercice physique est cruciale pour réduire les risques de récidives et améliorer la qualité de vie. Ce constat est fondé sur un socle de connaissances physiopathologiques bien documenté, des preuves établies et des recommandations précises. Ainsi, après un syndrome coronaire aigu et chez les patients à haut risque cardiovasculaire, les sociétés savantes recommandent l’activité physique à un niveau de classe 1 grade A. Il est de classe 1 grade B après une chirurgie coronaire et dans l’angor stable.
En France, les centres de soins de suite et de réadaptation sont les seules structures susceptibles de conduire et de superviser un programme de réentraînement à l’effort au cours d’un séjour de 3 à 4 semaines en hospitalisation complète ou de jour grâce à un encadrement pluridisciplinaire. Malheureusement, seuls 22 % des patients éligibles bénéficient d’un séjour complet en réadaptation cardiaque après un syndrome coronaire aigu. La réadaptation cardiaque supervisée à domicile n’existe pas encore en France.
Les méta-analyses montrent qu’un programme de réadaptation cardiaque fondé sur l’activité physique induit une baisse de 30 % de la mortalité d’origine cardiovasculaire, de 26 % de la mortalité totale et une diminution de 31 % du risque de réhospitalisation.
En tant que traitement non pharmacologique et sans danger, l’exercice physique est prescrit par le médecin cardiologue après une batterie d’évaluation qui permet de personnaliser le programme par la combinaison de la fréquence, l’intensité, la durée et la modalité de l’exercice.
Outre l’amélioration du pronostic, le réentraînement à l’effort apporte des bénéfices physiologiques incontestables pour la santé : amélioration de la fonction endothéliale contribuant à une régénération vasculaire et à l’angiogénèse (dès la 4e semaine d’entraînement en endurance), amélioration de l’équilibre sympathovagal, diminution de l’activité inflammatoire, amélioration des symptômes anxiété-dépression, du stress et des fonctions cognitives. Il permet aussi un contrôle des facteurs de risque cardiovasculaires (surcharge pondérale, contrôle du diabète, dyslipidémie, hypertension).
L’exercice intermittent à haute intensité est une modalité d’entraînement complémentaire à l’entraînement continu d’intensité modérée. Elle consiste à répéter de brèves périodes d’effort de haute intensité (> 85 % de V̇O2max ou du pic de puissance) entrecoupées de périodes d’effort de faible intensité ou de repos. Bien que les études les plus récentes montrent les mêmes bénéfices que pour les exercices d’intensité modérée, les protocoles d’exercice intermittent à haute intensité seraient plus adaptés aux patients fragiles et fatigables. L’objectif principal du programme est d’améliorer la consommation maximale d’oxygène du patient coronarien quelle que soit sa capacité physique de départ. Cependant, si la manipulation d’un seul paramètre d’exercice modifie considérablement les réponses cardiovasculaires, la variation de l’intensité doit être établie avec précaution pour maximiser les bénéfices, minimiser les risques d’accident et obtenir un maximum de plaisir pour le patient.
Concernant le type d’activité, les pratiques légères à modérées (type Tai Chi, Chi Gong) présentent aussi des effets positifs sur la santé. Le renforcement musculaire est complémentaire à l’entraînement aérobie et apporte des bénéfices additionnels sur le métabolisme du glucose, la composition corporelle, la densité osseuse, la force musculaire, la qualité de vie et la tolérance à l’effort.
Effets bénéfiques de l’activité physique sur les pathologies coronaires
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Baisse de la mortalité globale et cardiovasculaire et du nombre de réhospitalisations
Amélioration de la qualité de vie
Augmentation de V̇O2max et de la force musculaire
Baisse de la pression artérielle, amélioration de la fréquence cardiaque de récupération
et des marqueurs biologiques
|
|
B
|
Amélioration de la qualité du sommeil
Diminution des symptômes anxio-dépressifs
|
L’existence d’une relation dose-réponse, notamment le nombre de séances (par exemple, 12 versus 36) effectuées par les patients après un syndrome coronaire aigu, influence les résultats à long terme au niveau mortalité et risque de récidive de syndrome coronaire aigu. Cela pose le problème souvent constaté de l’inobservance des recommandations d’activité physique d’où la recherche de stratégies visant à soutenir les patients dans une pratique régulière : choix de la bonne activité physique pour chaque patient, suivi téléphonique, podomètre, coaching... Ces interventions doivent cibler les obstacles identifiés par les patients eux-mêmes afin d’être efficaces.
Au sein de la réadaptation cardiaque, l’activité physique est une prise en charge d’autant plus efficace qu’elle est instaurée précocement. Elle est sûre, globale et peu coûteuse. Un travail collaboratif en cours entre experts de différents pays européens devrait permettre de prescrire des programmes individualisés afin de maximiser les avantages cliniques et d’optimiser la sécurité.
Insuffisance cardiaque chronique : l’activité physique
fait partie du traitement pour tous les patients
L’insuffisance cardiaque chronique (ICC) est une pathologie fréquente et grave. Son incidence annuelle augmente régulièrement du fait du vieillissement de la population et de l’amélioration des traitements des pathologies cardiovasculaires et en particulier de la maladie coronaire. La mortalité à cinq ans de l’ICC reste très élevée (30-50 %), et dans les pays industrialisés son coût est estimé en moyenne à 2 % des dépenses totales de santé.
Deux formes d’ICC sont décrites, l’une à fonction systolique altérée et l’autre à fonction systolique préservée. La seconde est de description récente et concerne surtout des patients âgés présentant plusieurs comorbidités. Sa physiopathologie reste incomplètement expliquée.
Pendant très longtemps, la pratique d’activité physique a été contre-indiquée aux patients atteints d’ICC sous prétexte de laisser le cœur fatigué « se reposer », par crainte d’aggravation ou de complications de la pathologie sous-jacente. Ce n’est que dans les 20 dernières années que l’association d’une activité physique adaptée au traitement optimal de l’ICC a été proposée et progressivement recommandée par les différentes sociétés savantes.
Les progrès dans la connaissance de la physiopathologie de l’ICC ont permis de comprendre qu’un déconditionnement physique, d’aggravation insidieuse, pouvait rendre compte pour une large part d’une évolution progressive de l’ICC, d’une maladie du cœur vers une maladie systémique avec une atteinte associée des systèmes ventilatoire et musculaire squelettique. Ces altérations secondaires contribuent aux deux symptômes cliniques dominants de l’ICC, la dyspnée et la fatigue, qui permettent de chiffrer les degrés de gravité de l’ICC (classification NYHA
13
New York Heart Association.
de I à IV). Il a aussi été montré que l’inactivité physique aggrave le pronostic des patients atteints d’ICC et contribue à une augmentation de la mortalité précoce.
Cette meilleure compréhension de la physiopathologie a favorisé la réalisation de très nombreuses études sur les effets du réentraînement physique, surtout chez les patients atteints d’ICC avec une fonction systolique altérée. Les études chez les patients atteints d’ICC avec fonction systolique préservée sont plus rares. Elles ont démontré que l’activité physique n’aggravait pas la dysfonction myocardique et que sa pratique avait des effets bénéfiques chez les patients atteints d’ICC.
Le réentraînement physique chez les patients insuffisants cardiaques
est sûr, même chez les patients qui présentent
les atteintes les plus sévères
La sécurité du réentraînement physique chez les patients atteints d’ICC à fraction d’éjection altérée ou conservée, est prouvée et ceci quels que soient l’étiologie et le niveau de sévérité de l’ICC (stades NYHA II, III, IV). Le port d’un stimulateur ou d’un défibrillateur cardiaque ne contre-indique pas le réentraînement physique. De même, les patients atteints d’ICC avec assistance circulatoire et les transplantés cardiaques peuvent être réentraînés sans risque. Ainsi le réentraînement physique codifié, quelles que soient ses composantes (aérobie continue ou fractionnée, renforcement musculaire dynamique, gymnastique, respiratoire, électrostimulation musculaire périphérique...), réalisé dans une structure spécialisée ou bien à domicile après une bonne éducation sur sa pratique peut être proposé aux patients atteints d’ICC.
Le réentraînement cardiaque chez l’insuffisant cardiaque chronique améliore les capacités cardiorespiratoires, la force musculaire,
la qualité de vie et réduit le nombre de réhospitalisations
Après un programme de réentraînement physique supervisé, toutes les études rapportent une amélioration des capacités cardiorespiratoires surtout chez les patients atteints d’ICC modérée (NYHA II et III). Cette amélioration est objectivée par une augmentation du pic de V̇O2 qui est un paramètre majeur pour le pronostic mais aussi pour guider la thérapeutique la mieux adaptée individuellement chez les patients atteints d’ICC.
Cependant, l’effet bénéfique du réentraînement sur la mortalité des patients atteints d’ICC reste discuté. En effet, les conclusions initiales des méta-analyses qui étaient en faveur d’un effet bénéfique de l’activité physique sur la mortalité n’ont pas été totalement confirmées par les études ultérieures. C’est en particulier le cas de l’étude multicentrique prospective HF-Action qui analysait les effets d’un réentraînement physique sur la mortalité et les hospitalisations toutes causes de patients atteints d’ICC. En effet, les résultats en faveur d’un bénéfice n’ont été confirmés qu’après ajustement sur les facteurs de risque de mortalité principaux des patients atteints d’ICC. L’analyse de l’ensemble de ces études permet seulement de conclure à une tendance bénéfique de l’activité physique sur la mortalité des patients atteints d’ICC.
Le réentraînement physique en aérobie améliore les taux de peptides natriurétiques, BNP
14
BNP : Brain natriuretic peptide ; NT-pro-BNP : n terminal pro Brain natriuretic peptide.
et NT-pro-BNP, biomarqueurs myocardiques pronostics classiques chez les patients atteints d’ICC. Cette amélioration est corrélée à l’élévation du pic de V̇O
2 et à la baisse des événements cardiovasculaires. Les effets du réentraînement sur les marqueurs d’inflammation paraissent plus discutés.
L’effet bénéfique de l’activité physique sur le nombre et la gravité des ré-hospitalisations au moins à court terme des patients atteints d’ICC avec tous les bénéfices médicaux et économiques qui en découlent est prouvé.
De même, toutes les études rapportent chez ces patients un effet bénéfique du réentraînement sur la qualité de vie, lié à l’amélioration de la capacité cardiorespiratoire mais aussi de la force musculaire, indispensables à une meilleure autonomie.
Effets bénéfiques de l’activité physique sur l’insuffisance cardiaque chronique
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Amélioration de la qualité de vie, de la V̇O2 max et des marqueurs biologiques
|
|
B
|
Baisse de la mortalité et du nombre de réhospitalisations
|
En observant l’amorce d’une courbe en J entre la quantité totale hebdomadaire (≥ 7 METs
15
MET (Metabolic Equivalent Task) : unité consistant à déterminer l’intensité de l’effort au regard d’un facteur multiplicatif de la dépense énergétique de repos (le MET). Une activité physique sera qualifiée de légère si l’intensité est inférieure à 3 MET, de modérée entre 3 et 6 MET et élevée au-delà de 6 MET.
heures) du réentraînement physique et la survenue des événements cardiovasculaires chez les patients atteints d’ICC, une étude récente a évoqué la possibilité d’une dose maximale d’activité physique hebdomadaire à ne pas dépasser chez ces patients. Ces données méritent d’être confirmées par d’autres études.
Les effets d’un réentraînement hors protocole supervisé en institution ont également été étudiés. Ces études ont montré que la pratique d’une activité physique hors institution ou à domicile a des effets similaires et peut être proposée aux patients atteints d’ICC de manière sécurisée. C’est donc une alternative intéressante au réentraînement dans les centres de réadaptation aux capacités d’accueil limitées et pour le maintien d’une pratique régulière au long cours de l’activité physique.
L’entraînement aérobie fractionné est la modalité qui apporte
les bénéfices les plus importants
Le socle actuel du réentraînement physique des patients atteints d’ICC repose sur l’entraînement aérobie pour lequel il existe deux modalités d’entraînement : continu ou fractionné. Les études qui ont comparé les effets des entraînements aérobies continu et fractionné chez des patients atteints d’ICC ont montré que les deux modes étaient aussi bien tolérés par les patients. L’entraînement fractionné paraît plus efficace que l’entraînement continu sur le pic de V̇O2 à court terme dans la plupart des études. Les caractéristiques de l’entraînement fractionné, intensité et durée des phases d’effort et de récupération, chez les patients atteints d’ICC restent à préciser de même que les bénéfices de ce mode de réentraînement sur certains paramètres comme le remodelage ventriculaire et la fonction endothéliale. La persistance à long terme du bénéfice de l’entraînement fractionné sur le pic de V̇O2 dans la population des patients atteints d’ICC mérite aussi d’être étudiée.
Le renforcement musculaire dynamique est bien toléré par les patients atteints d’ICC sans risque d’aggravation notable. Il peut être isolé ou mieux, associé à un entraînement aérobie et semble améliorer les capacités cardiorespiratoires et musculaires et la qualité de vie.
Pour l’amélioration du pic de V̇O2, tous les modes d’exercice apparaissent bénéfiques. Mais les bénéfices les plus marqués sont observés avec dans l’ordre : l’entraînement aérobie fractionné, l’entraînement aérobie d’intensité modérée, l’électrostimulation, le réentraînement musculaire inspiratoire, l’association aérobie-renforcement musculaire et enfin le renforcement musculaire isolé.
D’autres modes d’activités physiques peuvent être proposés sans risque aux patients atteints d’ICC : danse de salon, Tai Chi, marche nordique, yoga, qui ont montré des bénéfices chez ces patients, mais doivent être confirmés par de nouvelles données plus solides.
Les méthodes de réentraînement à domicile avec télémonitorage ont aussi été évaluées ; elles n’ont pas été compliquées d’événements cardiovasculaires graves et ont prouvé leur efficacité sur la qualité de vie avec une possible amélioration de l’autonomie. Pour les patients atteints d’ICC réticents à suivre un programme de réentraînement, elles pourraient être une alternative.
La pratique d’une activité physique est recommandée
pour tous les insuffisants cardiaques chroniques
Les études concernant la tolérance et les effets bénéfiques du réentraînement physique ont concerné majoritairement des patients atteints d’ICC de gravité modérée (NYHA II et III), masculins, âgés en règle générale de moins de 70 ans et sans autre pathologie chronique associée. Ainsi, le réentraînement physique avec poursuite d’une activité physique au long cours est recommandé (classe 1 niveau de preuve A) pour tous les patients atteints d’ICC de classe NYHA I, II et III et cliniquement stables par les Sociétés Française, Européenne, Américaine du Nord, Canadienne de cardiologie. En outre, la pratique d’une activité physique d’intensité modérée à vigoureuse d’au moins 30 minutes au moins 5 fois par semaine est associée à une baisse des dépenses de santé significative par rapport aux patients inactifs.
Le programme de réentraînement physique doit comprendre 3 phases : une première phase hospitalière lors d’un épisode aigu, une deuxième (2-3 semaines) le plus souvent en institution spécialisée et une troisième qui devra être poursuivie indéfiniment.
La phase 1 se limite à la déambulation et/ou à la mobilisation du patient.
En phase 2, le programme structuré sera basé sur un entraînement aérobie, de type continu ou fractionné, au mieux associé à du renforcement musculaire dynamique réalisé 3 à 5 fois par semaine avec une durée de 30 minutes par séance. Le réentraînement fractionné n’est pas actuellement systématiquement recommandé en première intention à tous les patients. L’intensité de l’entraînement sera adaptée en fonction des tests d’effort réalisés régulièrement et aux sensations des patients.
Le renforcement musculaire de type dynamique (2 à 3 séances par semaine) sera encadré au début, il sollicitera des groupes musculaires différents avec des charges peu élevées et se fera à faible vitesse en évitant les phases statiques. Pour les patients les plus fragiles, un travail de type musculaire segmentaire individualisé peut être proposé.
Les indications d’autres modes de réentraînement, électrostimulation, musculation segmentaire, réentraînement des muscles inspiratoires, sont actuellement proposées au cas par cas à des patients atteints d’ICC particulièrement déconditionnés.
La phase 3 qui devra être poursuivie indéfiniment doit comprendre au moins 30 minutes d’activité physique modérée 5 fois par semaine. Les recommandations européennes conseillent d’y associer 2 à 3 séances par semaine de renforcement musculaire. Cette phase 3 est la plus problématique car l’adhésion des patients atteints d’ICC à l’activité physique autonome régulière et pérenne est faible (30-35 %).
Les bénéfices attendus de l’activité physique régulière chez les patients atteints d’ICC sont majeurs mais ils ne peuvent être maintenus qu’à la condition d’une observance poursuivie « à vie » de l’activité physique et donc d’une totale adhésion de ces patients aux recommandations d’activité physique proposées. Aujourd’hui moins de 20 % des patients atteints d’ICC bénéficient d’un programme de réhabilitation physique en hospitalisation ou en ambulatoire en phase 2. Ce faible pourcentage s’explique en partie par l’adhésion insuffisante des médecins traitants et de certains cardiologues aux recommandations.
L’adhésion au long cours des patients atteints d’ICC à l’activité physique nous paraît actuellement la problématique majeure. Nous expliquons encore mal pourquoi le niveau d’adhésion des patients atteints d’ICC diminue au fil du temps et des études complémentaires dans ces domaines paraissent justifiées. Par ailleurs, il faut insister sur le fait que la poursuite d’une activité physique n’a de chance d’être poursuivie que si elle est synonyme de plaisir. Il serait donc intéressant de valider l’apport de pratiques d’activité physique plus ludiques que le fait de pédaler sur vélo fixe 3 fois par semaine selon un protocole immuable. L’implication du patient atteint d’ICC dans la prise en charge de sa maladie et sa pratique d’activité physique, et dans le choix de son mode de réentraînement en phase 2 est un garant d’une meilleure adhésion au long cours. L’éducation thérapeutique en lien avec la pratique d’activité physique dès la phase 2 et/ou l’efficacité de séjours de « rappels » en centre de réhabilitation selon un calendrier individuel pourrait être évaluée.
Artériopathie oblitérante des membres inférieurs :
les programmes d’activité physique ont montré
leur efficacité chez les patients
L’artériopathie oblitérante des membres inférieurs (AOMI) est caractérisée par un rétrécissement du calibre des artères à destination des membres inférieurs, causé par l’athérosclérose, entraînant une claudication intermittente. La prévalence de cette maladie est d’environ 2 % chez les personnes de plus de 55 ans et peut atteindre 40 % après 80 ans tous sexes confondus. La réadaptation vasculaire est considérée comme le traitement de première intention pour traiter les patients. Elle est principalement basée sur l’activité de marche, sur l’éducation thérapeutique et sur l’activité physique adaptée et est très souvent mise en place conjointement avec le traitement médical dès le stade de claudication.
Concernant les bénéfices de la pratique d’une activité physique, il est admis qu’un programme de réadaptation vasculaire de trois mois basé sur des exercices physiques réduit la morbidité, la mortalité totale et cardiovasculaire des patients artéritiques symptomatiques et asymptomatiques. La mortalité cardiovasculaire est abaissée de près de 24 %. Les résultats de deux méta-analyses et deux revues Cochrane récentes montrent que l’exercice physique améliore la distance de marche sans douleur, ainsi que la distance de marche maximale parcourue chez les patients artéritiques. Et ce, associé à une amélioration de capacité aérobie, de l’anxiété, de la dépression, de la qualité de vie et à la correction des facteurs de risque cardiovasculaires. Ces résultats s’expliquent par l’amélioration des facteurs biomécaniques, de la fonction endothéliale, de la fonction mitochondriale, des paramètres inflammatoires, d’une réduction de la viscosité du sang et une très légère stimulation de l’angiogenèse. Tout ceci concourt à repousser le seuil d’apparition de la douleur, favorisant ainsi l’adhésion du patient à ce traitement non pharmacologique.
Effets bénéfiques de l’activité physique sur l’artériopathie oblitérante des membres inférieurs
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Baisse de la mortalité globale et cardiovasculaire
Augmentation de la distance de marche et de V̇O2max
Amélioration de la qualité de vie
|
|
C
|
Diminution des facteurs de risque cardiovasculaires et symptômes anxio-dépressifs
|
En général, trois différents modèles d’organisation de la réadaptation vasculaire sont décrits dans la littérature :
• une simple recommandation à l’entraînement à la marche ;
• un programme d’exercices supervisés ;
• un programme d’exercices que le patient va exécuter d’une manière autonome à son domicile.
De par le niveau de supervision, la réadaptation en centre associant marche et gymnastique, présente de meilleurs résultats que celle effectuée à domicile. Mais, les programmes d’exercices à domicile peuvent être efficaces grâce aux nouvelles technologies de monitoring.
Les études montrent que la fréquence optimale serait de 2 à 3 entraînements par semaine pour maximiser les bénéfices sur la santé. Concernant la durée, les protocoles adoptant des sessions de 30 à 60 minutes sont bien adaptés pour induire des augmentations remarquables de la distance de marche, idéalement étalés sur des périodes de 12 à 24 semaines. L’intensité des exercices est un point plus délicat à aborder car directement relié à la notion de douleur ou de gêne.
Malgré le bénéfice incontournable de la marche (c’est l’entraînement sur tapis roulant qui reste la méthode la plus utilisée dans les études cliniques), cette approche est très souvent limitée par les douleurs ressenties relativement tôt par les patients qui s’arrêtent après quelques minutes et doivent attendre entre 5 et 10 minutes que la gêne/la douleur s’estompe avant de redémarrer. De plus, du fait de cette limitation périphérique, l’intensité de l’exercice, et donc la sollicitation cardiovasculaire, reste souvent insuffisante pour obtenir un gain sur la capacité aérobie. Aussi le très faible volume d’exercice ne permet pas une dépense énergétique suffisante pour modifier favorablement les facteurs de risque cardiovasculaires. En complément de la marche, il convient donc de proposer du réentraînement à l’effort en utilisant des cycloergomètres à bras ou des entraînements de type fractionnés alternant l’exercice et la récupération.
Les programmes d’exercices supervisés sont recommandés comme traitement de première intention pour les patients atteints d’AOMI par les sociétés savantes américaines (niveau de preuve et de recommandation les plus élevés : 1A). Les sociétés savantes préconisent depuis de nombreuses années le « protocole de Gardner » qui consiste à marcher au moins 3 fois/semaine, 30 min à 1 heure, pendant 3 à 6 mois. Si possible, la claudication doit survenir en moins de 10 min. Le patient doit dépasser la première gêne, arriver à la limite de la douleur (échelle EVA 7/10), s’arrêter et surtout ne pas forcer, respecter un temps de repos de 5 min avant de repartir. Cette prescription doit être associée au travail des membres supérieurs mais aussi à une gymnastique spécifique au niveau des membres inférieurs, à des intensités vigoureuses sans toutefois dépasser des seuils de douleurs modérées.
Recommandation de pratique d’activités physiques d’après les recommandations de la Society for Vascular Surgery (2015)
|
Recommandation
|
Grade
|
Niveau de preuve
|
|
Recommandation en première intention d’un programme supervisé d’exercice
avec de la marche au minimum trois fois par semaine (30-60 minutes/session)
pour au moins 12 semaines pour tous les patients avec une claudication intermittente
|
1
|
A
|
|
Recommandation d’un exercice à domicile, avec un objectif d’au moins 30 minutes
de marche 3 à 5 fois par semaine quand un programme supervisé d’exercice
n’est pas accessible ou pour un bénéfice à long terme après un programme d’exercice supervisé
|
1
|
B
|
|
Chez les patients après revascularisation pour claudication intermittente,
un programme d’exercice supervisé ou à domicile est recommandé
en tant que thérapie adjuvante
|
1
|
B
|
D’une façon générale, malgré de bons résultats en termes de coût-efficacité, les programmes de réadaptation vasculaire restent pourtant peu utilisés, sous-prescrits et méconnus en France (faible nombre de centres proposant des programmes supervisés, méconnaissance des médecins vasculaires et des rééducateurs, augmentation du nombre d’actes interventionnels, observance difficile des personnes malades à moyen terme...). Il est essentiel de faciliter l’accès aux structures (centres, cabinets, associations) car le manque d’observance à la marche des patients atteints d’AOMI s’explique aussi par le manque de soutien psychologique. Les études basées sur de faibles effectifs avec des protocoles souvent variables démontrent que l’on manque encore de connaissances pour homogénéiser les techniques de rééducation vasculaire et favoriser l’observance des personnes malades sur le long cours.
Accident vasculaire cérébral : l’activité physique
est recommandée mais encore trop peu prescrite
Les accidents vasculaires cérébraux (AVC) constituent la première cause mondiale de handicap fonctionnel, la deuxième cause de décès et la troisième cause de handicap en général. L’AVC qui a longtemps été décrit comme une pathologie spécifique aux personnes âgées concerne de plus en plus les personnes de moins de 55 ans. Le mode de vie actuel et les facteurs de risque cardiovasculaires, avec en premier le tabagisme, jouent un rôle important dans cette évolution. L’effet bénéfique d’une activité physique régulière en prévention primaire des AVC et des accidents ischémiques transitoires est prouvé.
Les séquelles post-AVC sont neuromusculaires et aussi cognitives. Ces dernières ont un impact majeur sur l’autonomie motrice fonctionnelle et justifient qu’une « réhabilitation » cognitive soit associée au réentraînement physique. Cette « réhabilitation » cognitive dépasse le cadre de cette expertise et n’est donc pas abordée ici.
Après la survenue d’un AVC, les données scientifiques à notre disposition révèlent que les patients sont très peu actifs dans la vie quotidienne, leur niveau d’inactivité physique et de sédentarité est trop élevé. Ils présentent ainsi une faible capacité cardiorespiratoire.
Le réentraînement physique chez les patients après un accident vasculaire cérébral est sûr, même lorsque son début est précoce
Les principales méta-analyses soulignent le caractère globalement sûr du réentraînement physique chez le patient après un AVC, et relèvent qu’il n’aggrave pas la spasticité musculaire.
La discussion principale sur la sécurité du réentraînement post-AVC concerne le délai de sa mise en place après la survenue de celui-ci. Il est convenu de parler de mobilisation précoce lorsque l’activité physique est réalisée hors du lit dans les 24 à 72 premières heures après l’accident. Les quatre études contrôlées, sur de faibles échantillons, concluent à une absence de risque majoré sauf pour la mortalité si la réhabilitation est débutée dans les 24 premières heures. Il paraît donc que la mobilisation précoce, entre 24 et 72 heures après l’AVC, ne présente pas de risque significativement majoré pour le patient.
Après l’AVC, le risque cardiovasculaire individuel du patient doit être évalué en se basant sur les facteurs de risque mais aussi sur les examens cardiovasculaires classiques. Le patient est alors classé comme à risque faible, intermédiaire ou élevé. L’indication d’une épreuve d’effort maximale, sous traitement, avec contrôle électrocardiographique et tensionnel, avant le début du réentraînement, sera guidée par le niveau de risque cardiovasculaire du patient.
L’épreuve d’effort avec analyse des échanges gazeux est recommandée pour guider l’intensité du réentraînement mais elle reste difficile à réaliser chez nombre de ces patients et elle ne peut pas vraiment être remplacée par le test de marche de 6 minutes.
Une surveillance particulière doit être assurée lors du réentraînement chez les patients ayant présenté un AVC de cause hémorragique.
La pratique d’activité physique améliore les capacités cardiorespiratoires, la force musculaire et apporte un bénéfice
sur les activités de la vie quotidienne chez les patients après un accident vasculaire cérébral
Après la survenue d’un AVC, un réentraînement physique peut être recommandé avec un double objectif, améliorer les retentissements des séquelles de l’appareil locomoteur et/ou cognitives et prévenir une récidive par l’amélioration des facteurs de risque cardiovasculaires.
La grande variété des causes et des séquelles des AVC retentissant sur l’autonomie et la qualité de vie du patient limite les conclusions des études qui ont analysé les bénéfices du réentraînement et les protocoles d’activité physique les mieux adaptés. Dans les pays occidentaux, la réhabilitation physique globale fait partie du traitement optimal des patients après AVC, ce qui restreint les possibilités d’analyser ses effets spécifiques par des études contrôlées. Ainsi, la plupart des données exploitables sont issues d’études réalisées en Chine, avec les limites scientifiques qui en découlent, où la réhabilitation post-AVC n’est pas obligatoire.
Il est cependant prouvé que le réentraînement après un AVC est bénéfique pour la capacité cardiorespiratoire (pic de V̇O2 et test de marche de 6 minutes), sur la force musculaire, sur la déambulation et sur les activités de la vie quotidienne. Ces améliorations sont surtout dues à une amélioration des limites musculaires squelettiques et ostéo-articulaires et sont d’autant plus nettes que le patient est plus déconditionné. Les bénéfices sont plus marqués avec un entraînement aérobie associé à du renforcement musculaire, et semblent corrélés à la précocité et à la quantité (effet dose-réponse) du réentraînement.
Les effets bénéfiques de l’activité physique sur l’autonomie, les fonctions cognitives, et la mortalité des patients post-AVC sont moins bien démontrés, mais ils ont été moins étudiés. Des études de bonne qualité méthodologique complémentaires sont donc nécessaires.
La perte osseuse avec fragilisation squelettique est marquée après un AVC. Les fractures éventuelles aggravent la perte de mobilité et augmentent la mortalité chez ces patients. Le réentraînement physique pourrait avoir un effet bénéfique sur la structure osseuse des patients post-AVC. Mais ces résultats doivent être confirmés par des études randomisées contrôlées en aveugle réalisées sur de grandes populations.
L’effet des interventions sur le mode de vie, et en particulier du réentraînement sur l’amélioration des facteurs de risque cardiovasculaires et donc en prévention secondaire post-AVC n’est pas prouvé. Des études à la méthodologie rigoureuse, avec en particulier un encadrement des patients pour une évaluation réelle du changement de mode de vie et en particulier de la pratique d’activité physique, méritent d’être menées avant de conclure formellement.
Néanmoins, pour les patients ayant eu un accident ischémique transitoire ou un AVC sans séquelle importante, les résultats de différents essais randomisés contrôlés récents sont en faveur d’une efficacité de l’activité physique et d’un changement de mode vie sur les facteurs de risque cardiovasculaires, et pour certaines études sur les qualités fonctionnelles artérielles des patients. Mais ces études ont été réalisées sur de faibles échantillons et des études complémentaires sont nécessaires.
La qualité de vie est très altérée chez les patients post-AVC. Le réentraînement n’a qu’un impact modéré sur ce paramètre. Toutefois, des recherches complémentaires sont nécessaires pour préciser les effets spécifiques observés sur les deux versants, physique et cognitif, de la qualité de vie en fonction des modalités de réentraînement. Les intérêts respectifs d’un réentraînement encadré prolongé et/ou basé sur des stages courts méritent aussi d’être étudiés.
Effets bénéfiques de l’activité physique sur l’accident vasculaire cérébral
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Amélioration de la capacité aérobie (V̇O2) et de la capacité fonctionnelle (TM6)
|
|
B
|
Amélioration de la qualité de vie et des fonctions cognitives
|
|
C
|
Diminution des facteurs de risque cardiovasculaires et des récidives d’AVC
|
Pour une meilleure efficacité des programmes d’activité physique chez les patients post-AVC, le réentraînement physique global classique, basé sur du travail aérobie et du renforcement musculaire, mériterait d’être associé à une individualisation du mode de réentraînement réellement centrée sur le patient et à des programmes d’autogestion qui aident les patients à prendre une part active dans la gestion de leurs activités physiques à visée thérapeutique ou de loisir.
La majoration de l’activité physique à visée thérapeutique lors du temps libre du patient pourrait améliorer l’efficacité des protocoles proposés actuellement qui sont souvent ressentis négativement par le patient. De même, la pratique régulière de gestes journaliers, qui est une spécificité de la réhabilitation physique des patients post-AVC, est fortement recommandée, en association avec le réentraînement global classique, pour aider à une meilleure récupération fonctionnelle et donc à l’autonomie de ces patients. Vu la relation positive entre le volume d’activité et les effets bénéfiques sur la neuroplasticité, la pratique journalière avec une grande répétition des gestes les plus variés est même recommandée. Des protocoles de téléréhabilitation et de réalité virtuelle pourraient également être efficaces mais les résultats des études actuellement disponibles doivent être consolidés.
Le réentraînement doit être individualisé et s’adapter aux séquelles neuromusculaires et cognitives des patients après un accident vasculaire cérébral
Les études sur les effets du réentraînement chez les patients post-AVC ont concerné des adultes sans limite d’âge, touchés par un AVC ischémique ou hémorragique, sans trouble de conscience ni de détérioration précoce, sans signe d’hémorragie intracérébrale secondaire, de syndrome coronarien ou d’insuffisance cardiaque. Dans ce cadre, la majorité des recommandations insistent sur la nécessité d’une réhabilitation physique précoce pour les patients après un AVC mais sans s’accorder formellement sur le moment de sa mise en route. La mobilisation précoce hors-lit dans les 24 heures qui suivent l’AVC est surtout utile pour la prévention des complications. Elle ne semble pas s’accompagner d’un meilleur bénéfice fonctionnel en dehors peut-être de la qualité de la marche. Cependant, tous les patients post-AVC ne peuvent pas débuter une activité physique aussi précocement. Les recommandations proposent de sélectionner des patients ayant une fréquence cardiaque de repos entre 40 et 120 bpm et/ou une pression artérielle systolique entre 120 et 220 mmHg, et de surveiller ces paramètres et le niveau de conscience lors des 3 premiers jours de mobilisation.
Des règles de base pour la réhabilitation des patients post-AVC sont recommandées. Les patients post-AVC les plus sévères doivent être réentraînés dans des centres spécialisés avec une surveillance cardiovasculaire stricte. Les patients moins sévères peuvent reprendre l’entraînement en groupe avec une surveillance moins stricte voire à domicile en cas d’AVC anciens. En plus du traitement médical optimal, l’activité physique individualisée sera débutée le plus précocement possible, avec mobilisation passive initiale si besoin. Des tests d’évaluation fonctionnelle guideront l’activité physique individualisée (progressivement 3 à 5 séances par semaine de 20 à 60 minutes) qui associera travail aérobie et renforcement musculaire. Un programme d’autogestion de la pratique d’activité physique sera proposé au patient et conduit par un personnel formé. La surveillance sera adaptée au niveau de risque de chaque patient. En réadaptation tertiaire à domicile, l’activité physique journalière et poursuivie indéfiniment devra associer les activités journalières et une activité physique aérobie et de renforcement musculaire adaptée au niveau de handicap et à la capacité physique.
Malgré ces recommandations unanimes qui mériteraient cependant une meilleure codification, la prescription de l’activité physique pour les patients est encore limitée et la réalisation d’une épreuve d’effort est peu fréquente. Ceci peut s’expliquer par la crainte des thérapeutes qui pourrait être diminuée par une formation spécifique et la nécessité d’adapter les matériels de réentraînement aux spécificités des patients post-AVC.
Des études complémentaires de bonne qualité incluant de grands échantillons de patients sont indispensables pour démontrer l’intérêt et l’absence d’effet délétère d’une initiation de la réhabilitation dans les 24 premières heures post-AVC, pour définir les modes de réentraînement optimaux chez des patients avec un handicap fonctionnel sévère et enfin pour préciser l’effet de l’activité physique sur la mortalité, les morbidités et les fonctions cognitives des patients.
Bronchopneumopathie chronique obstructive : instaurer une pratique physique pérenne est fondamental
La bronchopneumopathie chronique obstructive (BPCO) qui se caractérise par une obstruction bronchique permanente et peu sensible aux bronchodilatateurs, connaît une prévalence dont la progression ne cesse d’inquiéter les spécialistes de santé publique. Elle est actuellement considérée comme la 3e cause de mortalité au niveau mondial. La mortalité associée à la BPCO diminue depuis quelques années chez les hommes et augmente chez les femmes. En France, la prévalence se situe entre 5 et 10 %, bien que très certainement sous-évaluée en raison d’un dépistage complexe et coûteux à mettre en œuvre. Les coûts directs de cette pathologie sont estimés entre 3 700 et 7 500 euros/an et par patient, auxquels il convient d’ajouter des coûts indirects (absentéisme, perte de productivité...) et des coûts personnels en termes de qualité de vie dégradée.
La survie des patients atteints de bronchopneumopathie chronique obstructive diminue de façon spectaculaire avec la réduction du niveau d’activité physique
L’activité physique, véritable pierre angulaire de la réhabilitation respiratoire, est reconnue depuis de nombreuses années comme l’unique méthode ayant un niveau de preuve de grade A pour l’amélioration de la qualité de vie, de la tolérance à l’effort et la réduction de la dyspnée et des exacerbations des patients atteints de BPCO. Plus récemment, de nombreux travaux ont complété ces données. Il a pu être ainsi mis en évidence que l’activité physique pouvait réduire la vitesse du déclin du VEMS
16
Volume d’air expiratoire maximal en une seconde.
, marqueur essentiel de la gravité de l’obstruction bronchique, et ainsi limiter l’apparition de cette pathologie ou ralentir sa progression. Au-delà, le niveau d’activité physique est également relié à la diminution des hospitalisations en lien avec la BPCO, ainsi qu’à la probabilité de survie des patients atteints de BPCO. Des travaux réalisés sur des suivis parfois longs (plus de 7 ans) rapportent en effet des résultats extrêmement homogènes mettant en évidence que la probabilité de survie des patients atteints de BPCO chute de façon spectaculaire avec la réduction du niveau d’activité physique habituelle. Ces données sont fondamentales, car le constat porté par la littérature sur le niveau d’activité physique habituel des patients atteints de BPCO est accablant : l’activité physique des patients atteints de BPCO est réduite de façon drastique. Cette réduction touche toutes les intensités d’activité physique (légère, modérée ou élevée) et s’avère d’autant plus marquée que la sévérité de la BPCO est importante : seuls 10 % des patients de grade III sont considérés comme actifs mais aucun au grade IV, stade d’obstruction bronchique le plus sévère. Au regard des recommandations de l’OMS, les patients atteints de BPCO sont nettement en deçà des niveaux de pratique impactant positivement la santé, alors que toutes les données longitudinales attestent de l’importance d’augmenter ce niveau d’activité physique pour limiter la mortalité et les exacerbations liées à la BPCO.
Selon une méta-analyse récente, l’activité physique dans un contexte de réhabilitation respiratoire semble jouer un rôle sur l’augmentation à 6 mois du niveau d’activité physique spontanée après le retour à domicile. La taille d’effet est relativement modeste mais significative (0,14 ; p = 0,04). Tout porte donc à croire qu’il est possible d’avoir une action durable sur le niveau d’activité physique spontanée des patients, mais que des progrès importants sont encore à faire pour en assurer la réalité sur le plus long terme. Quoi qu’il en soit, la mise en parallèle des faibles niveaux d’activité physique des patients atteints de BPCO mis en relation avec les impacts de l’activité physique sur la réduction des exacerbations, des hospitalisations, des symptômes et de la mortalité met en évidence le besoin fondamental d’instaurer une pratique physique pérenne chez ces patients.
L’évaluation des capacités physiques et de la tolérance à l’effort est recommandée de façon à pouvoir assurer une adéquation entre les capacités des patients et les intensités de pratique. L’épreuve d’effort cardiorespiratoire maximale est considérée comme la technique de référence qui peut être ensuite complétée par le test de marche de 6 minutes. Ce test peut toutefois présenter un effet plafond si la tolérance à l’effort n’est pas suffisamment impactée par la BPCO. Il conviendra dans ce cas de recourir au test navette incrémental (ISWT, test au cours duquel la vitesse est progressivement augmentée au moyen de signaux sonores pré-enregistrés). L’usage de la supplémentation aiguë en oxygène est nécessaire pour corriger des désaturations pendant l’exercice. Toutefois, il est acquis à présent que l’usage systématique de la supplémentation en oxygène lors des activités physiques n’améliore en rien ses effets.
Effets bénéfiques de l’activité physique sur la bronchopneumopathie chronique obstructive
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Effets obtenus par le réentraînement à l’effort dans le cadre de la réadaptation respiratoire :
Amélioration de la tolérance à l’effort générale (endurance, force) ; de la force et endurance des membres supérieurs ; de la dyspnée ; de l’état de santé et de la qualité de vie
Baisse du nombre d’hospitalisations et de leurs durées
Récupération plus rapide après une exacerbation
|
|
B
|
Augmentation de la survie
|
Un grand choix de pratiques différentes d’activité physique
sont validées pour le patient atteint de bronchopneumopathie chronique obstructive
La littérature met ensuite clairement en évidence que de nombreuses techniques peuvent être utilisées : entraînements en endurance bien sûr, validés par plusieurs méta-analyses depuis 1996, mais, plus récemment les entraînements fractionnés qui donnent des effets comparables pour des durées de pratique plus courtes. Ils sont mieux tolérés par les patients si la durée des pics d’intensité d’effort utilisés reste inférieure à 30 secondes. Les entraînements basse versus haute intensité ont fait l’objet de peu de travaux mais donnent des résultats globalement superposables pour des volumes de pratiques comparables ; les activités physiques aquatiques donnent également d’excellents résultats, ainsi que des pratiques plus douces comme le Tai Chi. Le renforcement musculaire est également efficace sur la tolérance générale à l’effort, mais induit également des effets spécifiques considérables sur la force (et de façon plus inconstante sur la masse musculaire) permettant de lutter contre la dysfonction musculaire, reconnue actuellement comme un déterminant significatif de la survie des patients. Les résultats inconstants sur la prise de masse et la typologie musculaire sont attribués à l’extrême variabilité des protocoles et il serait cohérent que les exercices soient réalisés à des charges proches de 70 % du 1-RM (charge ou force maximale) des patients ou pouvant être mobilisées entre 8 et 12 fois seulement. Il existe un nombre considérable de pratiques différentes qui ont fait la preuve de leur efficacité et l’activité physique des patients atteints de BPCO doit impérativement être pensée sous la forme d’une conjonction des différentes méthodes et conditions de pratiques, de façon à les rendre attractives, ludiques et variées ; car en définitive, le seul véritable enjeu à relever aujourd’hui ne réside pas tant dans l’amélioration fonctionnelle immédiate après la pratique, mais dans la capacité à modifier durablement le comportement des patients vis-à-vis de l’activité physique qui doit impérativement être systématiquement préservée voire amplifiée au quotidien.
Asthme : les activités d’endurance ont montré leur efficacité pour améliorer l’état de santé des patients
L’asthme est une maladie caractérisée par des épisodes réversibles d’altération plus ou moins sévère de la fonction respiratoire et une hyperréactivité bronchique considérable. Sa prévalence est d’environ 11 % chez les enfants et 7 % chez les adultes. Si la prévalence de l’asthme chez ces derniers est stable, elle a toutefois tendance à augmenter encore chez les enfants.
L’activité physique chez le patient asthmatique est un véritable paradoxe, car elle impacte positivement son état clinique, mais elle peut également provoquer un bronchospasme post-exercice. C’est souvent chez les asthmatiques une des principales raisons de leur crainte et d’une éviction plus ou moins importante des activités physiques. Pourtant, les effets rapportés sont réels : amélioration de l’aptitude physique aérobie qui s’accompagne d’une meilleure protection contre le bronchospasme post-exercice par une majoration considérable de la bronchodilatation d’exercice, amélioration de la qualité de vie et de l’état clinique des patients avec un accroissement significatif du nombre de jours passés sans symptôme respiratoire. L’hyperactivité bronchique est également réduite par l’activité physique ce qui se traduit par des réponses bronchiques réduites sous l’effet de tests médicamenteux ou lors de l’activité physique elle-même. Seuls les effets sur la fonction respiratoire de repos sont encore discutés, en raison de 2 méta-analyses arrivant à des résultats contradictoires. Aucune méta-analyse n’a pu être réalisée sur les intensités optimales de pratique, car le besoin d’améliorer l’aptitude physique aérobie et réduire ainsi la demande ventilatoire d’exercice est tel que les travaux se sont focalisés de façon quasi-exclusive sur des pratiques d’endurance.
Effets bénéfiques de l’activité physique sur l’asthme
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Amélioration de l’aptitude physique aérobie (V̇O2max) et endurance ; de la capacité d’exercice (puissance maximale) et de la qualité de vie
Augmentation du nombre de jours sans symptômes
|
|
B
|
Diminution du risque de bronchospasme post-exercice et de l’hyperréactivité bronchique
Amélioration du VEMS et de la survie
|
|
C
|
Diminution de l’état inflammatoire des voies aériennes
|
Les activités physiques d’endurance trouvent une place de choix dans l’optimisation de l’état de santé des asthmatiques en améliorant les capacités physiques d’endurance, en potentialisant la bronchodilatation d’exercice et en réduisant l’hyperréactivité bronchique, ce qui explique les répercussions secondaires positives sur l’état clinique quotidien et la qualité de vie des patients asthmatiques.
Pathologies ostéo-articulaires : l’activité physique occupe une place fondamentale dans le traitement
En 2016, l’étude Global Burden of Disease Study a montré que parmi 310 maladies chroniques, la lombalgie commune était la 1re cause d’années de vie vécues avec handicap dans le monde. L’ensemble des pathologies ostéo-articulaires arrivent en seconde position des principales causes de handicap. Le poids de ces pathologies est particulièrement important dans les pays à revenus élevés d’Asie, d’Europe Occidentale, d’Océanie et d’Amérique du Nord. En France, l’étude Handicap-Santé 2008-2009 a montré des résultats comparables : les pathologies ostéo-articulaires étaient la 1re cause de handicap perçu chez les sujets de plus de 40 ans.
Les recommandations nationales et internationales concernant le traitement des pathologies ostéo-articulaires préconisent l’association de mesures médicamenteuses et non médicamenteuses. Parmi celles-ci, l’activité physique adaptée est une des pierres angulaires du traitement et est largement recommandée afin de réduire et/ou prévenir les déficiences et limitations d’activité spécifiques et non spécifiques dans ces maladies.
Le terme d’« activité physique adaptée » est peu utilisé dans la littérature scientifique internationale et les articles scientifiques se réfèrent souvent aux termes « exercices » ou « exercices thérapeutiques » (« exercise therapy » en anglais). Ce terme générique désigne un programme structuré d’exercices, qui peut être un programme d’exercices spécifiques ou un programme d’activité physique non spécifique, ou l’association de ces deux programmes. Les exercices spécifiques visent à réduire et/ou prévenir les déficiences et les limitations d’activité spécifiques à la pathologie ostéo-articulaire sous-jacente (raideur, instabilité, déformation articulaire, faiblesse musculaire, troubles de la marche...). Les types d’exercices proposés concernent le renforcement musculaire, la mobilité, l’étirement ou la proprioception des articulations ou des groupes musculaires atteints. Le programme d’activité physique non spécifique quant à lui cherche à réduire et/ou prévenir les déficiences et les limitations d’activité liées à l’évolution chronique de la maladie ou à la iatrogénie, tels que la fatigue, les symptômes d’anxiété et de dépression, la baisse des performances musculaires globales qui contribuent au syndrome de déconditionnement à l’effort. Cette pratique cible l’amélioration des capacités aérobies et de la forme physique générale. Ces programmes peuvent être supervisés, par un professionnel de la rééducation ou par un professionnel de l’activité physique adaptée, ou non supervisés et se dérouler dans le milieu de vie du patient (domicile, club sportif, associations...).
Les données de la littérature ont été synthétisées en fonction de 3 grands groupes de pathologies ostéo-articulaires : 1) rachialgies chroniques, 2) arthrose périphérique et 3) rhumatismes inflammatoires chroniques et connectivites.
Activité physique et rachialgies chroniques
Dans la lombalgie chronique d’origine commune, l’activité physique adaptée sous la forme de programmes structurés associant exercices spécifiques et activité physique non spécifique, conduit à une réduction de la douleur et une amélioration de la fonction, en fin de traitement et à long terme, et diminue l’incapacité à travailler sur le long terme. Les programmes d’activité physique adaptée ont également un intérêt lorsqu’ils sont réalisés après un épisode de lombalgie afin de prévenir les récidives, réduire leur fréquence et le nombre de jours d’arrêt de travail dans les 2 années qui suivent l’épisode initial de lombalgie. Les différentes modalités d’activité physique adaptée ont été insuffisamment comparées entre elles pour établir une hiérarchie claire, mais la plupart des programmes ont en commun les exercices de renforcement musculaire des stabilisateurs du rachis, les exercices aérobies et les exercices de proprioception lombo-pelvienne. Les programmes multidisciplinaires de type « réentraînement à l’effort » associant exercices spécifiques, activité physique non spécifique et éducation thérapeutique montrent des résultats sur la réduction de la douleur et une amélioration de la fonction : à court terme, quel que soit le comparateur, et à long terme comparés aux soins usuels et à la kinésithérapie seule. Ils permettent un retour au travail avec des taux de reprise du travail de 32 % à 73 % à 1 ou 2 ans quand ils sont comparés à des programmes non multidisciplinaires. Cependant, les résultats observés dépendent du système de protection sociale du pays dans lequel ces programmes ont été évalués. L’adjonction de procédures de « facilitation » de la reprise du travail comme le temps partiel ou l’aménagement des activités professionnelles pourrait améliorer ces résultats. Parmi les activités physiques non spécifiques, le Tai Chi, le yoga, le Pilates et la marche semblent avoir un effet bénéfique sur la douleur et la fonction à court et moyen termes. Toutefois, le niveau de preuve pour ces activités est au mieux modéré et la pertinence clinique des effets observés débattue. Ces activités ont l’avantage d’être bien tolérées.
Dans les cervicalgies communes, il est difficile de faire une synthèse critique des données publiées du fait de l’inhomogénéité des patients, des faibles effectifs inclus dans les études et de la grande variété des interventions étudiées et de leurs comparateurs. En ce qui concerne les cervicalgies chroniques, les programmes d’activité physique adaptée ont un effet bénéfique sur la douleur et la fonction à la fin du traitement et à court terme (< 3 mois) et sont bien tolérés. Ils comportent des exercices visant le renforcement musculaire, le travail en endurance et les étirements de la région cervico-scapulothoracique et des membres supérieurs. En revanche, il n’existe pas de preuve d’efficacité des programmes d’activité physique adaptée dans les cervicalgies aiguës. Enfin, alors que le canal lombaire rétréci est une des causes les plus fréquentes de lombalgie chronique chez le sujet âgé, les études sur l’efficacité et la tolérance des programmes d’exercices spécifiques (par exemple exercices en flexion lombaire) et/ou d’activité physique non spécifique dans cette indication sont peu nombreuses et les niveaux de preuve très faibles à faibles, ce qui pourrait expliquer l’absence de recommandations nationales ou internationales pour le traitement des patients ayant un canal lombaire rétréci.
Activité physique et arthrose périphérique
L’activité physique adaptée sous la forme de programmes structurés associant exercices spécifiques et activité physique non spécifique à sec et/ou en balnéothérapie est systématiquement recommandée par les sociétés savantes dans le traitement de l’arthrose périphérique en soins primaires. Les données de la littérature sur l’intérêt de l’activité physique adaptée dans l’arthrose des membres inférieurs montrent de manière constante une efficacité des programmes structurés d’exercices sur la douleur et la fonction à court et moyen termes et l’absence d’effets indésirables graves. Dès 2002, les données de la littérature étaient suffisantes pour démontrer les bénéfices des exercices par rapport à l’absence d’exercices dans l’arthrose des membres inférieurs. Quel que soit le phénotype d’arthrose du genou, les exercices à sec et aquatiques ont toujours été jugés « appropriés » selon les recommandations 2014 de l’Osteoarthritis Research Society International. Parmi les activités physiques non spécifiques, le Tai Chi pourrait permettre une amélioration de la fonction à 3 mois, mais pas de réduction de la douleur ou du handicap. Les autres activités physiques non spécifiques réalisées à sec (par exemple la marche, certaines activités sportives), pourraient améliorer la fonction et les performances physiques à court et moyen termes, mais n’ont pas montré d’effet clair sur la douleur. Pour l’arthrose de la hanche, les données disponibles sont plus rares que pour l’arthrose du genou. Elles sont en faveur d’un effet bénéfique, faible à modéré, de l’activité physique adaptée sur la douleur et la fonction, à la fin du traitement et à moyen terme. Enfin, dans l’arthrose des mains, les exercices spécifiques pourraient avoir un effet bénéfique sur la douleur, la fonction et la raideur articulaire à court terme. Toutefois, le niveau de preuve est faible, la pertinence clinique des effets observés est discutable et l’intérêt des exercices dans l’arthrose des mains par rapport à l’absence d’exercices demeure incertain.
Activité physique et rhumatismes inflammatoires chroniques
et connectivites
Le pronostic fonctionnel des rhumatismes inflammatoires chroniques et des connectivites s’est considérablement amélioré au cours des 20 dernières années. Toutefois, les rhumatismes inflammatoires chroniques et les connectivites restent encore associés à des handicaps musculo-squelettiques. L’activité physique adaptée sous la forme de programmes structurés associant exercices spécifiques, activité physique non spécifique et éducation thérapeutique est recommandée quels que soient le stade, la sévérité ou l’activité de la maladie.
Dans la polyarthrite rhumatoïde, le niveau de preuve de l’efficacité des programmes d’exercices spécifiques ciblant l’atteinte de la main est élevé, avec une amélioration de la fonction de la main. Les activités physiques moins spécifiques telles que les exercices de renforcement musculaire global et les exercices aérobies à sec ou en balnéothérapie montrent des effets plus inconstants, dont l’amplitude est faible à modérée, sur la douleur, la force musculaire, la fonction globale et la qualité de vie.
Effets bénéfiques de l’activité physique sur les pathologies ostéo-articulaires
|
Pathologie
|
Niveau de preuve
|
Effet bénéfique
|
|
Lombalgie chronique
|
A
B
|
Diminution de la douleur et amélioration de la fonction
Diminution des récidives et amélioration du taux de reprise des activités professionnelles
|
|
Arthrose des membres inférieurs
|
A
|
Diminution de la douleur et amélioration de la fonction
|
|
Polyarthrite rhumatoïde et spondylarthrite ankylosante
|
A
B
|
Diminution de la douleur et amélioration de la fonction
Absence d’effets délétères
Amélioration de la qualité de vie (polyarthrite rhumatoïde)
|
|
Cervicalgies chroniques
|
B
|
Diminution de la douleur et amélioration de la fonction
|
Dans la spondylarthrite ankylosante, par rapport à l’absence de traitement, les programmes d’activité physique adaptée associant exercices spécifiques et activité physique non spécifique permettent une réduction des douleurs et une amélioration de la fonction à la fin du traitement et au cours du suivi. Par rapport aux soins usuels, les effets observés sont plus faibles. Dans la sclérodermie systémique, les programmes d’activité physique adaptée associant exercices spécifiques et activité physique non spécifique sont considérés comme un « traitement de fond ». Cependant, seules 7 études randomisées contrôlées ont évalué leur efficacité et leur tolérance. Les effectifs inclus étaient faibles et les interventions insuffisamment décrites, sauf dans une étude qui a échoué à montrer que ce type de programme était supérieur aux soins usuels pour réduire les limitations d’activité à 1 an. Dans la dermatomyosite et la polymyosite de l’enfant et de l’adulte, les programmes d’activité physique adaptée associant exercices spécifiques et activité physique non spécifique sont aussi considérés comme une modalité essentielle du traitement. Seules 7 études randomisées contrôlées ont évalué leur efficacité et leur tolérance. Ces études randomisées contrôlées suggèrent un effet positif sur les capacités aérobies, les performances musculaires et la réduction des limitations d’activité à court et moyen termes, mais elles présentent des limites méthodologiques majeures. Qu’il s’agisse des formes chroniques ou actives de la maladie, la tolérance à l’activité physique adaptée a été bonne et il n’a pas été rapporté de recrudescence des douleurs ou de signes d’activité de la maladie.
L’activité physique adaptée sous la forme de programmes structurés, supervisés ou non, associant exercices spécifiques ou activité physique non spécifique, doit être considérée comme un traitement de fond d’action lente des pathologies ostéo-articulaires inflammatoires et non inflammatoires. Quels que soient le stade, l’activité ou la sévérité de la maladie, elle vise à réduire ou prévenir de manière secondaire ou tertiaire les déficiences et limitations d’activité spécifiques et non spécifiques à ces maladies. Malgré les difficultés méthodologiques propres aux essais d’intervention non pharmacologique, les niveaux de preuve de l’efficacité et de l’innocuité de l’activité physique adaptée à court et moyen termes sont désormais considérés comme élevés dans la lombalgie chronique, l’arthrose des membres inférieurs, la polyarthrite rhumatoïde et la spondylarthrite ankylosante. Une optimisation du contenu et du mode de délivrance de ces programmes est encore nécessaire. Les niveaux de preuve sont encore insuffisants dans les cervicalgies chroniques, le canal lombaire rétréci, l’arthrose des mains ou les connectivites. L’intérêt d’un programme structuré d’activité physique adaptée n’est pas démontré dans les cervicalgies communes et la lombalgie aiguë.
Cancers : l’activité physique apporte des bénéfices
chez les patients à toutes les étapes de la maladie
En France, environ 3 millions de personnes vivent après avoir été atteints d’un cancer, et la moitié est âgé de 70 ans ou plus. Les localisations les plus fréquentes dans cette population sont le sein, la prostate et le côlon-rectum, suivies des hémopathies malignes et de l’endomètre. Après le diagnostic d’un cancer, les données de la littérature observent de façon convergente une diminution du niveau d’activité physique total et d’activité physique d’intensité élevée ainsi qu’une augmentation de la sédentarité. Par ailleurs, le surpoids, l’obésité et la prise de poids, observés pendant et après un cancer, sont associés à une augmentation du risque de récidive de certains cancers, à une augmentation de la morbidité et de la mortalité toutes causes confondues ainsi qu’à une augmentation de risque de second cancer.
Les effets secondaires à court, moyen et long termes, variables en fonction du type de cancer, des traitements et de l’évolution de la maladie, sont nombreux et conduisent à une altération de l’état général et de la qualité de vie des patients. Les données montrent, de façon constante, un déconditionnement physique avec une altération des capacités cardiorespiratoires et une diminution de la force et de la masse musculaires. Ce déconditionnement, d’origine multifactorielle, est un facteur de mauvais pronostic et provoque chez la majorité des patients une fatigue invalidante, une diminution de la qualité de vie et une intolérance à l’exercice.
De très nombreuses méta-analyses, essais randomisés et études prospectives, qui ont étudié les effets de l’activité physique chez les patients atteints de cancer, montrent un ratio bénéfice-risque favorable de celle-ci sur les conséquences de la maladie et les effets secondaires des traitements. La plupart des études a porté sur les cancers les plus fréquents, à savoir les cancers du sein, du côlon et de la prostate, et la grande majorité a évalué l’intérêt de l’activité physique chez les personnes atteintes de cancer à un stade limité, les bénéfices de l’exercice en phase avancée et métastatique ont été peu étudiés à ce jour.
Un programme d’activité physique améliore les capacités cardiorespiratoires, la composition corporelle et la fatigue dès le début du traitement
L’ensemble des essais randomisés et méta-analyses confirment le bénéfice de l’activité physique en termes d’amélioration des capacités cardiorespiratoires et physiques et ceci lorsque le programme d’activité physique est initié au début de la chimiothérapie, dès la fin des traitements, ou à distance de ceux-ci.
Les programmes d’intensité modérée et élevée ont permis d’obtenir des résultats positifs sur l’augmentation des capacités cardiorespiratoires et leur maintien dans le temps à condition de maintenir une bonne observance des exercices et de planifier un ajustement de l’intensité des exercices dans le temps.
Des exercices physiques ciblés sur le renforcement musculaire mis en œuvre pendant et dans les suites des traitements améliorent la force des groupes musculaires sollicités, mais les résultats en termes d’impacts sur la masse musculaire sont hétérogènes.
De nombreuses méta-analyses ont montré que l’activité physique pendant et/ou après le traitement est associée à une réduction du poids, de l’IMC, et de la masse grasse. Lorsque les études se limitent aux femmes ménopausées, elles montrent un bénéfice de l’activité physique sur la diminution du pourcentage de masse grasse et un gain ou maintien de la masse musculaire.
L’ensemble des méta-analyses (> 20) ayant étudié l’impact de l’activité physique sur la fatigue rapporte de façon convergente que l’activité physique, pendant et après les traitements diminue la fatigue, notamment chez les patients porteurs de tumeurs solides, les plus étudiées étant les cancers du sein et de la prostate. Les données les plus récentes suggèrent un bénéfice plus important lorsque l’activité physique est proposée dès le début des traitements. Le bénéfice semble plus important lorsqu’elle est réalisée dans le cadre d’un programme supervisé, comparé à l’activité physique non supervisée. L’activité physique de type aérobie, ou mixte (associant activité physique aérobie et de renforcement musculaire), semble être plus efficace sur la réduction de la fatigue que l’activité de renforcement musculaire. Les données sont en faveur d’une activité physique d’intensité modérée (10-12 MET.h/semaine). L’augmentation de l’intensité au-delà n’apporte pas de bénéfice supplémentaire en termes de fatigue, et a été inversement associée au bénéfice sur la fatigue dans certaines études.
L’activité physique pourrait jouer un rôle bénéfique pour plusieurs effets secondaires des traitements
L’activité physique régulière semble améliorer certaines douleurs liées aux cancers et aux traitements.
Chez les femmes atteintes de cancer du sein, l’activité physique pourrait prévenir la perte de la densité minérale osseuse associée à l’hormonothérapie et la ménopause précoce. Si l’activité physique n’a pas montré à ce jour de bénéfice réel dans la prévention du risque d’apparition de lymphœdème chez les patientes atteintes de cancer du sein, les études montrent de façon convergente l’absence d’une aggravation de risque de lymphœdème, et rapportent une amélioration de l’amplitude des mouvements de l’épaule après chirurgie avec curage ganglionnaire. La balance bénéfice-risque est en faveur d’une activité physique progressive et régulière en post-opératoire (exercices aérobies et de renforcement musculaire en respectant les précautions et recommandations d’hygiène de vie) (niveau de preuve A). Les délais entre chirurgie et début des exercices étaient très variables dans les études, de plusieurs jours à plusieurs semaines et ne permettent pas de formuler des recommandations. L’interdiction à pratiquer un exercice physique impliquant le membre supérieur du côté opéré n’est plus indiquée (niveau de preuve A).
Un bénéfice de l’activité physique sur la neuropathie périphérique chimio-induite a été suggéré, sur la toxicité cardiovasculaire ainsi qu’une amélioration du taux d’accomplissement des traitements (diminution de report, arrêt de traitement, ou réduction de dose).
L’activité physique pratiquée régulièrement améliore la qualité de vie
L’effet de l’activité physique sur la qualité de vie a fait l’objet de plus de 25 méta-analyses qui montrent de façon constante un bénéfice de l’exercice pratiqué régulièrement sur la qualité de vie des patients atteints de cancer, que les programmes soient initiés pendant les traitements ou en post-traitement. Les résultats disponibles concernent dans la grande majorité des cas les femmes traitées pour un cancer du sein, à visée curative. La diversité des programmes d’activité physique proposés dans ces études ne permet pas aujourd’hui de définir les caractéristiques d’un programme optimal. Néanmoins, une durée du programme d’intervention supérieure à 2 mois optimise les bénéfices sur la qualité de vie. L’intensité de l’activité aérobie semble également avoir une influence, et certaines méta-analyses mettent en avant une efficacité pour des activités supérieures à 3-4 MET. L’intensité doit augmenter progressivement jusqu’à un niveau optimal qui reste encore à déterminer. Des techniques plus douces (Yoga, etc.) semblent cependant pouvoir apporter un effet bénéfique en termes de qualité de vie. Une vigilance doit être apportée pour les programmes initiés pendant la phase de traitement car l’effet semble inverse lorsque des quantités hebdomadaires d’activité physique dépassent les 20 MET.h/semaine. L’adhésion des patients aux programmes d’activité physique proposés pendant cette phase semble favorisée par une quantité d’activité physique hebdomadaire plus faible.
Effets bénéfiques de l’activité physique sur les cancers
|
Niveau de preuve
|
Effet bénéfique
|
|
A
|
Amélioration des capacités aérobies (V̇O2max) pendant ou après traitement
Amélioration de la force musculaire et diminution du poids, IMC et masse grasse
Diminution de la fatigue pendant et après les traitements et amélioration de la qualité de vie
Résultats bénéfiques des programmes aérobie ou combiné en comparaison avec des programmes de renforcement musculaire seul sur la réduction de la fatigue
Pas d’effets secondaires spécifiques liés à l’exercice chez les patients atteints d’un cancer
|
|
B
|
Diminution du risque de récidive, mortalité globale et spécifique après cancer du sein et du côlon
|
|
B/C
|
Diminution de la durée d’hospitalisation et des complications post-opératoires chez les patients atteints de cancer broncho-pulmonaire avec activité physique en pré-opératoire
Amélioration des capacités fonctionnelles en situation métastatique
Intensité supérieure à l’intensité modérée n’apporte pas de bénéfice supplémentaire en termes de fatigue
|
|
C
|
Diminution des risques de récidive, mortalité globale et spécifique après cancer de la prostate
Diminution de certaines douleurs liées aux cancers et aux traitements, neuropathie chimio-induite et toxicité cardiovasculaire, perte de densité osseuse associée à l’hormonothérapie et la ménopause précoce
|
L’association d’un programme d’activité physique avec des techniques cognitivo-comportementales, des entretiens motivationnels en face-à-face complétés par un suivi téléphonique apparaissent comme des moyens de favoriser l’amélioration de la qualité de vie.
Chez des patients atteints de cancers du sein, du côlon et de la prostate, l’activité physique pratiquée avant ou après le diagnostic pourrait réduire la mortalité et le risque de récidive
Les méta-analyses des études de cohorte rapportent un effet bénéfique de l’activité physique pratiquée avant ou après le diagnostic, sur la réduction de la mortalité globale et spécifique et sur le risque de récidive chez des patients atteints de cancers non métastatiques du sein, du côlon (niveau de preuve B) et de la prostate (niveau de preuve C). Une relation dose-effet est suggérée. L’impact de l’activité physique sur la survie n’a pas fait l’objet d’essai randomisé. L’augmentation du niveau de l’activité physique post-diagnostique, par rapport au niveau pré-diagnostique, est associée à une réduction de la mortalité globale pour le cancer du sein.
Plusieurs mécanismes ont été proposés pour expliquer les effets de l’activité physique sur le développement et l’évolution tumorale, au niveau systémique et du micro-environnement tumoral. Une influence de l’activité physique sur plusieurs mécanismes ou voies de signalisation impliquées a été observée notamment celle de la sensibilité à l’insuline, des paramètres immuno-inflammatoires et de la régulation hormonale. Cependant, les données de la littérature ne permettent pas de conclure à l’existence d’un lien causal entre l’exercice et la survie des patients atteints de cancer.
Les études publiées à ce jour n’ont pas mis en évidence d’effets secondaires spécifiques liés à l’exercice chez les patients atteints d’un cancer. Deux recommandations pour la pratique clinique concluent sur la base des données de la littérature que la pratique d’une activité physique est sans risque pour les patients atteints de cancer, pendant et après les traitements, et que la fréquence des effets indésirables est similaire à celle observée chez des personnes indemnes de cancer. Une évaluation et adaptation de l’exercice sont importantes pour adapter la prescription d’activité physique aux capacités d’exercice, aux comorbidités et aux limitations relatives ou temporaires. En l’absence de limitations, une activité physique progressive et régulière d’au moins 150 min/semaine d’une intensité modérée à intense, conforme aux recommandations en population générale, est recommandée (niveau de preuve A).
Les objectifs et indications de l’activité physique peuvent varier en fonction de l’étape de la maladie et des traitements. Les données suggèrent un bénéfice de l’activité physique pré-opératoire sur la condition physique, la durée d’hospitalisation et les complications post-opératoires chez les patients atteints de cancer broncho-pulmonaire. Il est recommandé de combiner des activités de type aérobie et du renforcement musculaire et de pratiquer de manière progressive, en augmentant progressivement la fréquence, la durée et l’intensité de l’activité physique. Pendant les traitements et la phase post-thérapeutique immédiate, l’activité physique vise à prévenir le déconditionnement physique, la perte de la masse musculaire, la prise de poids, la fatigue, la détérioration de la qualité de vie, ainsi que certains effets secondaires de la maladie. L’activité physique après traitement vise à améliorer la condition physique, la fatigue et la qualité de vie, à prévenir le développement de comorbidités et de cancers secondaires et à réduire les risques de morbidité et de mortalité sur le long terme. Chez les patients atteints d’un cancer à un stade avancé ou métastatique, l’activité physique pourrait améliorer les capacités physiques fonctionnelles. Compte tenu de la diversité des situations cliniques, les données de la littérature sont insuffisantes pour formuler des recommandations systématiques en situation palliative et la pratique de l’activité physique doit être personnalisée en fonction de l’état clinique des patients et des comorbidités.
Dépression : un programme d’activité physique apporterait des bénéfices équivalents à ceux des traitements médicamenteux ou de psychothérapie
La dépression est la maladie qui provoque le plus d’invalidité dans le monde. Le diagnostic est complexe à établir en pratique clinique comme en recherche et peut varier selon les outils utilisés (auto-questionnaire, guide d’entretien, entretien), la classification utilisée (CIM-10 versus DSM-IV). Les troubles dépressifs sont sous-diagnostiqués, notamment chez les personnes âgées, les travailleurs surmenés, les jeunes mères et chez les patients souffrant d’une maladie chronique.
La prévalence des troubles dépressifs concerne trois millions de personnes en France avec deux fois plus de femmes que d’hommes. La distinction entre les formes modérées et sévères, entre les formes épisodiques et chroniques est parfois difficile. Elle explique en partie l’hétérogénéité des prévalences obtenues dans les études.
En France, l’usage de médicaments antidépresseurs est très important, souvent banalisé et utilisé comme seul recours. Il concerne 5 millions de personnes et 2,5 millions pour un épisode dépressif majeur.
Un trouble dépressif augmente le risque d’adopter un mode de vie sédentaire et de diminuer le niveau d’activité physique hebdomadaire. Plus la symptomatologie dépressive évaluée avec le Beck Depression Inventory est sévère chez les patients souffrant d’un épisode dépressif majeur et plus leur inactivité physique est importante. Cette association est aussi observée chez des patients ayant un trouble dépressif secondaire évalué par le Composite International Diagnostic Interview à une maladie d’origine organique comme l’infarctus du myocarde.
Certaines études montrent que l’inactivité physique conduit à une majoration des symptômes dépressifs.
Concernant les effets des programmes d’activité physique adaptée, plusieurs méta-analyses montrent des effets modérés à élevés sur les symptômes dépressifs. L’effet thérapeutique de programmes d’activité physique adaptée sur les troubles dépressifs est également observé chez des personnes âgées et des personnes atteintes de maladies chroniques (patients atteints d’obésité, de certaines pathologies cardiaques, patientes traitées pour un cancer du sein ou patients ayant une bronchopneumopathie chronique obstructive).
La plupart des études disponibles ont à ce jour évalué l’activité physique comme un complément d’autres thérapies, en particulier les médicaments antidépresseurs. Des essais randomisés contrôlés testent l’efficacité de programmes d’activité physique adaptée en tant qu’alternative et constatent une équivalence de bénéfices entre programme d’activité physique et médicament antidépresseur chez les patients ayant un trouble dépressif.
Après le traitement d’un épisode dépressif, une pratique physique régulière d’activité physique contribuerait à prévenir les récidives d’épisode dépressif.
Effets bénéfiques d’un programme d’activité physique adaptée sur la dépression
|
Niveau de preuve
|
Effets bénéfiques
|
|
A
|
Amélioration d’un trouble dépressif
Amélioration de la symptomatologie anxio-dépressive consécutive à une autre maladie chronique
|
|
B
|
Baisse de récidive d’un épisode dépressif
|
|
C
|
Baisse des tentatives de suicide
Baisse des suicides
|
Les effets antidépresseurs de l’activité physique relèvent à la fois de mécanismes biologiques et de processus psychosociaux. Aucun auteur n’a proposé de modèle intégré exhaustif à ce jour pour expliquer ces mécanismes. Différentes explications sont proposées :
• meilleur apport d’oxygène au système nerveux central (modèles physiologiques) ;
• influence sur la libération de cortisol et de sérotonine, stimulation des voies d’endorphine et facilitation du circuit de la récompense, facilitation de la neurogenèse dans l’hippocampe (modèles neurobiologiques) ;
• amélioration des fonctions exécutives : planification, coordination, focalisation, et apprentissage (modèles neuropsychologiques) et modification des niveaux de conscience, notamment du corps (body awareness) ;
• augmentation de la distraction, diminution des biais perceptifs/interprétatifs et diversion des pensées négatives (modèles cognitivistes) ;
• amélioration de l’efficacité personnelle, de la valeur physique perçue, de l’estime de soi et de la participation sociale (modèles psychosociologiques).
Enfin, l’effet placebo ne peut pas être totalement exclu.
Différentes sociétés savantes ont émis des recommandations :
• un programme d’activité physique chez les personnes touchées par des symptômes sub-syndromiques persistants ou une dépression modérée, encadrées par des professionnels compétents et comportant 3 séances par semaine de 45 à 60 minutes sur une durée de 10 à 14 semaines (National Institute for Health and Clinical Excellence, Royaume-Uni) ;
• une activité physique basée sur l’expérience vécue pour améliorer le bien-être et diminuer les symptômes dépressifs (National Clinical Practice Guideline, Allemagne) ;
• un programme d’activité physique adaptée en première intention, soit en thérapie unique pour des adultes touchés par un trouble dépressif de sévérité légère à modérée, soit en thérapeutique complémentaire aux traitements conventionnels pour les adultes souffrant d’un trouble dépressif modéré ou d’un épisode dépressif majeur (Canadian Network for Mood and Anxiety Treatment, Canada).
De façon globale, une tendance se dégage de la littérature en faveur de programmes d’activité physique adaptée comportant un minimum de 3 séances de 30 minutes par semaine avec des pratiques physiques mixtes (aérobie et résistance) supervisées et ceci durant 3 mois.
La prescription de programme en activité physique adaptée comme le prévoit la loi du 26 janvier 2016 de modernisation du système de santé français, en traitement exclusif ou associé d’un trouble dépressif, va nécessiter des solutions incitatives pour les patients (aide pour les transports, outils numériques engageant...) ainsi qu’une sensibilisation et formation des médecins et professionnels à l’activité physique adaptée.
Enfin, si le bénéfice thérapeutique de programmes en activité physique adaptée chez des adultes ayant un trouble dépressif est similaire à celui d’autres thérapeutiques reconnues comme les médicaments antidépresseurs et les psychothérapies en termes de réduction des symptômes, des études d’implémentations sont nécessaires pour affiner les modalités de la prescription de ces programmes. Elles permettraient de mieux préciser les effets de l’activité physique en fonction du type de trouble dépressif, des modalités d’intervention, du type de patient (âge, pathologies associées), de distinguer les effets des différentes thérapies associées à l’activité physique et de suivre les effets à moyen terme.
La standardisation de l’évaluation et de la surveillance
des programmes d’activité physique permettra
une amélioration des pratiques
Chez les personnes atteintes de maladies chroniques, comme nous l’avons vu, l’enjeu n’est plus seulement d’augmenter leur niveau d’activité physique hebdomadaire ou de viser un seuil de recommandation générale (par exemple, 10 000 pas par jour). Il s’agit de proposer des programmes efficaces permettant de limiter l’aggravation et les complications de leur maladie, de potentialiser les soins en améliorant l’état de santé et la durée de vie avec une bonne qualité de vie, voire dans certains cas de guérir leur maladie, et cela en toute sécurité. La littérature voit ainsi se multiplier les études testant des programmes en activité physique adaptée utilisant des pratiques corporelles individuelles ou de groupe supervisées et assistées ou non d’une nouvelle technologie. Le contexte de prescription va accélérer cette démarche de mise en œuvre de programmes santé fondés et validés par la science et encadrés par des professionnels spécialisés. Ces programmes efficaces et sûrs devront être décrits précisément, évalués et comparés en termes de bénéfices (efficacité), de risque (effets secondaires et risque d’interactions avec d’autres thérapeutiques), d’utilité (coûts/efficacité), de contrainte (fardeau supplémentaire) et de satisfaction (qualité de vie).
Mais, à ce jour, l’évaluation des programmes en activité physique adaptée comme d’autres interventions non médicamenteuses n’a pas encore atteint la rigueur de celle des médicaments. Par exemple, l’évaluation de la dose et de la nature d’activité physique n’est pas toujours satisfaisante. Si le nombre d’études comparatives montrant des bénéfices sur la santé et la qualité de vie augmente depuis le début des années 2000, elles laissent apparaître une grande hétérogénéité des méthodes et des contenus de pratique que ne manquent pas de souligner les méta-analyses. Il faut dire que ces protocoles s’avèrent extrêmement exigeants en ressources financières, humaines et matérielles. Ils sont aussi complexes à élaborer à cause de choix à opérer entre un idéal méthodologique (renforçant la validité interne)
17
Validité interne d’une étude. C’est la qualité de la méthode d’une étude. Elle reflète jusqu’à quel point on peut montrer que tous les aspects de la conception d’une étude et la manière dont l’étude a été menée ont pu protéger vis-à-vis de biais systématiques, de biais non systématiques et d’une erreur inférentielle.
et une faisabilité locale (renforçant la validité externe)
18
Validité externe d’une étude. Elle correspond à la cohérence avec les connaissances et les données qui ne sont pas celles de l’étude (physiopathologiques, pharmacologiques, épidémiologiques).
. Des travaux sont menés actuellement pour standardiser à un niveau international ces protocoles d’évaluation des programmes, de la conception à la restitution des résultats.
Compte tenu des bénéfices potentiels et des risques limités pour la santé des programmes en activité physique adaptée encadrés par des professionnels, certains auteurs encouragent le développement d’études d’implémentation visant à optimiser la mise en œuvre et la surveillance à moyen terme de ces programmes dans différents territoires et auprès de populations ayant des modes de vie et des cultures différentes. Ces études font appel de plus en plus souvent à des méthodologies mixtes (quantitatives et qualitatives) et des systèmes informatiques de traitement de grandes quantités de données. Elles devraient permettre d’optimiser les pratiques en activité physique et de signaler des incidents/accidents sur de larges populations de patients atteints de maladies chroniques.Compte tenu des bénéfices potentiels et des risques limités pour la santé des programmes en activité physique adaptée encadrés par des professionnels, certains auteurs encouragent le développement d’études d’implémentation visant à optimiser la mise en œuvre et la surveillance à moyen terme de ces programmes dans différents territoires et auprès de populations ayant des modes de vie et des cultures différentes. Ces études font appel de plus en plus souvent à des méthodologies mixtes (quantitatives et qualitatives) et des systèmes informatiques de traitement de grandes quantités de données. Elles devraient permettre d’optimiser les pratiques en activité physique et de signaler des incidents/accidents sur de larges populations de patients atteints de maladies chroniques.
 ). Le type d’exercice physique est également déterminant dans les adaptations physiologiques observées. Les exercices d’endurance améliorent la fonction cardiaque et la résistance à la fatigue des muscles locomoteurs, tandis que les exercices de renforcement musculaire augmentent la masse et la force musculaires. Il est désormais établi que le muscle squelettique est également capable de communiquer à distance avec d’autres organes par l’intermédiaire de facteurs sécrétés, i.e. les myokines. Bien que le répertoire des myokines soit en cours d’élaboration, des études récentes ont identifié plusieurs myokines capables de cibler l’hippocampe pour moduler la mémoire et la dépression (BDNF, GDNF11
), le foie pour moduler la production hépatique de glucose (Interleukine-6), les muscles pour moduler la sensibilité à l’insuline (apeline), ainsi que de nombreux autres tissus et organes. Une partie des effets bénéfiques de l’activité physique s’explique également par son effet anti-inflammatoire au niveau systémique et par la production de facteurs analgésiques (β-endorphines, substance P). Les recherches futures devraient s’orienter vers l’identification de nouvelles myokines et des types d’exercices physiques les mieux adaptés à la prise en charge de chaque pathologie chronique.
). Le type d’exercice physique est également déterminant dans les adaptations physiologiques observées. Les exercices d’endurance améliorent la fonction cardiaque et la résistance à la fatigue des muscles locomoteurs, tandis que les exercices de renforcement musculaire augmentent la masse et la force musculaires. Il est désormais établi que le muscle squelettique est également capable de communiquer à distance avec d’autres organes par l’intermédiaire de facteurs sécrétés, i.e. les myokines. Bien que le répertoire des myokines soit en cours d’élaboration, des études récentes ont identifié plusieurs myokines capables de cibler l’hippocampe pour moduler la mémoire et la dépression (BDNF, GDNF11
), le foie pour moduler la production hépatique de glucose (Interleukine-6), les muscles pour moduler la sensibilité à l’insuline (apeline), ainsi que de nombreux autres tissus et organes. Une partie des effets bénéfiques de l’activité physique s’explique également par son effet anti-inflammatoire au niveau systémique et par la production de facteurs analgésiques (β-endorphines, substance P). Les recherches futures devraient s’orienter vers l’identification de nouvelles myokines et des types d’exercices physiques les mieux adaptés à la prise en charge de chaque pathologie chronique.