| dc.contributor.author | Loirand, G | fr_FR |
| dc.contributor.author | Lompré, AM | fr_FR |
| dc.contributor.author | Savineau, JP | fr_FR |
| dc.contributor.author | Pacaud, P | fr_FR |
| dc.date.accessioned | 2012-07-11T08:41:52Z | |
| dc.date.available | 2012-07-11T08:41:52Z | |
| dc.date.issued | 1997 | fr_FR |
| dc.identifier.citation | Loirand, G ; Lompré, AM ; Savineau, JP ; Pacaud, P, Tonus des muscles lisses vasculaires : translissions du signal dépendantes et indépendantes du Ca2+, Med Sci (Paris), 1997, Vol. 13, N° 6-7; p.766-76 | fr_FR |
| dc.identifier.issn | 1958-5381 | fr_FR |
| dc.identifier.uri | http://hdl.handle.net/10608/461 | |
| dc.description.abstract | Les variations du Ca2+ libre intracellulaire jouent un rôle
complexe dans la régulation du tonus vasculaire. Le Ca2+
entre essentiellement dans les cellules musculaires lisses
par les canaux dépendants du potentiel ; celui-ci est réglé
par les concentrations intracellulaires de K+ et de Cl- dont
les canaux sont eux-mêmes dépendants du Ca2+. Les mouvements
de Ca2+ intracellulaire entre les lieux de stockage
(réticulum sarcoplasmique) et le cytoplasme sont réglés
d’une part, par les récepteurs de l’inositol 1,4,5-trisphosphate
et de la ryanodine et, d’autre part, par la Ca2+-
ATPase. La modulation de la force contractile des fibres
musculaires lisses est liée à la phosphorylation de la chaîne
légère de la myosine qui dépend de l’équilibre entre les
kinases et les phosphatases spécifiques. La MLCK (kinase
des chaînes légères de la myosine) est activée par un complexe
Ca2+-calmoduline formé lors de l’augmentation de la
concentration intracellulaire de Ca2+. L’activité de la MLCP
(phosphatase des chaînes légères de la myosine) dépend de
messagers intracellulaires (acide arachidonique, diacylglycérol,
PKC). La sensibilité de l’appareil contractile, à concentration
de Ca2+ libre cytoplasmique constante, est réglée
assez spécifiquement par l’inhibition de la MLCP, qui pourrait
être contrôlée, notamment par des protéines G. | fr |
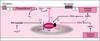
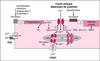
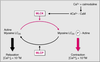
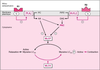
| dc.description.abstract | The main function of vascular smooth muscle tissue is the regulation of blood pressure through changes in the vascular tone. Two main factors regulate the contraction and relaxation of vascular smooth muscle cells: the cytosolic free Ca2+ concentration ([Ca2+](i)) and the Ca2+ sensitivity of the contractile elements. Schematically, constrictors increase [Ca2+](i) and the Ca2+ sensitivity of contractile apparatus while relaxant agonists have opposite effects. The sources of Ca2+ are both extracellular and intracellular. The sarcoplasmic reticulum (SR) is the physiological intracellular source of Ca2+. The Ca2+ storage capacity of SR involves intraluminal Ca2+ binding protein such as calsequestrin and calreticulin. Ca2+ is released from SR to the cytosol through InsP3 and ryanodine receptors for (InsP3-induced Ca2+ release and Ca2+-induced CA2+ release). During relaxation, the [Ca2+](i) is reduced in part by Ca2+ pumping into the SR by Ca2+-ATPase (SERCA). Several isoforms of SERCA are expressed in vascular smooth muscle. Ca2+ enters into vascular smooth cells through Ca2+ permeable ion channels. The capacitative Ca2+ entry and ligand-gated channels (P(2x)-purcinoceptors) allow extracellular Ca2+ to flow into the cytosol. However, voltage-dependent Ca2+ channels represent the main route for Ca2+ entry which is essentially modulated by the membrane potential. Ca2+-activated channels such as Cl- (Cl(Ca)) or K+ (K(Ca)) channels play a key role in the modulation of membrane potential. Activated Cl(Ca) channels depolarize whereas activated K(Ca) channels hyperpolarize the membrane thus causing increase and decrease in the vascular tone, respectively. Modulation of the force at constant [Ca2+](i) results from changes in the activities of kinases and phosphatases, acting on the regulatory light chain of myosin (MLC20) phosphorylation. Intracellular messages such as arachidonic acid or protein kinase modulate the activity of the MLC20 phosphatase and thus, the Ca2+ sensitivity. G protein-coupled Ca2+ sensitization also involves inhibition of the MLC20 phosphatase. Trimeric as well as monomeric G proteins (Rho p21, Ras p21) seem to be responsible for this mechanism. Recent studies, by identifying new regulatory mechanisms, provide a better understanding of the fundamental mechanisms regulating contractile properties of vascular smooth muscle and open new way for the treatment of vascular diseases. [References: 58] | en |
| dc.language.iso | fr | fr_FR |
| dc.publisher | Masson Périodiques, Paris | fr_FR |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [revue papier, ISSN : 0767-0974], 1997, Vol. 13, N° 6-7; p.766-76 | fr_FR |
| dc.title | Tonus des muscles lisses vasculaires : translissions du signal dépendantes et indépendantes du Ca2+ | fr |
| dc.title.alternative | Intracellular signalling and vascular tone | fr_FR |
| dc.type | Article | fr_FR |
| dc.contributor.affiliation | Institut de pharmacologie moleculaire et cellulaire, Cnrs UPR 411, 660, route des Lucioles, 06560 Valbonne, France; Cnrs Ura 1131, batiment 443, universite de Paris Sud, 91405 Paris, France; Laboratoire de physiologie, universite de Bordeaux II, 146, rue Leo-Saignat, 33076 Bordeaux, France | - |
| dc.identifier.doi | 10.4267/10608/461 | |