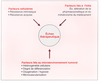
Les mécanismes de réparation de l'ADN : des cibles potentielles en pharmacologie du cancer.
Résumé
La résistance à la chimiothérapie est fréquente en cancérologie.
Une tumeur peut être intrinsèquement résistante aux
médicaments ou peut développer, au cours du traitement,
différents mécanismes de résistance. Ainsi, les cellules peuvent
neutraliser les lésions d’ADN provoquées par les
agents génotoxiques (alkylants, analogues du cis-platine)
grâce à des mécanismes de réparation aboutissant à l’excision
d’adduits* formés au niveau d’une base, l’excision de
base, ou l’excision de nucléotide. La réparation de l’ADN
par la O6-alkylguanine-ADN-méthyltransférase (MGMT) est
le mécanisme le mieux caracterisé ; l’inhibition de la
MGMT dans les cellules tumorales augmente la cytotoxicité
des chloro-nitrosourées, alors que son transfert dans des
cellules de la moelle osseuse protège celles-ci contre la myélosuppression
induite par ces médicaments. On est moins
avancé dans la compréhension des mécanismes de l’altération
de la réparation par excision de nucléotides dans les
cellules tumorales résistantes aux anti-cancéreux, mais
les connexions entre la réparation, la transcription et le
cycle cellulaire offrent des cibles multiples pour moduler
ou cibler la réparation dans le contexte thérapeutique. A major limitation in the treatment of human cancer is the frequent development of resistance to chemotherapy drugs, that may occur either de novo or acquired after drug exposure. Tumor cells cope with DNA damage by a variety of mechanisms including activation of DNA repair processes and delay or arrest of cell-cycle progression. Dysregulation of DNA repair mechanisms has been shown to contribute to drug resistance in human cancer cells maintained either in vitro or in vivo. The O6-methylguanine-DNA methyltransferase (MGMT) is a well characterized protein which is responsible for the removal of alkyl groups from DNA bases, mainly O6- alkylguanine. Its role in tumor drug resistance has brought potential applications for DNA repair in cancer therapy ranging from biochemical modulation, aimed at reducing MGMT expression in tumor cells, to gene therapy approaches aimed at increasing MGMT expression in bone marrow cells and therefore protecting against myelosuppression side effects of drugs such as chloronitrosoureas. Drug resistance has also been associated with abnormalities in DNA nucleotide excision repair pathway in a variety of human tumor cell lines originated from ovarian adenocarcinomas chronic lymphocytic leukemia, breast and lung cancers. However, the molecular basis of these abnormalities and their clinical relevance are still unknown. The inter-relationship between DNA repair, transcription, and several other processes that regulate the cell cycle indicates that checkpoint mechanisms are associated intimately with the DNA repair machinery. Numerous cell signaling pathways can also be triggered by DNA damage suggesting a role of cell signal transduction in the regulation of cellular response to DNA damage and DNA repair. The extraordinary progress in cloning genes involved in the regulation of DNA repair and cell cycle provides tools to begin to unfold the role of these pathways in cell response to external stress. It is likely that an understanding of these mechanisms may offer novel targets for cancer therapeutics.
Pour citer ce document
Alaoui-Jamali, M ; Sankar Mitra, S, Les mécanismes de réparation de l'ADN : des cibles potentielles en pharmacologie du cancer., Med Sci (Paris), 1996, Vol. 12, N° 6-7; p.766-73