Les protéines FXYD : nouveaux régulateurs de la Na,K-ATPase
Date
2006Auteur
Delprat, Benjamin
Bibert, Stéphanie
Geering, Käthi
Metadata
Afficher la notice complèteRésumé
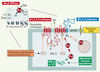
Les protéines FXYD appartiennent à une famille de petites protéines membranaires. Des études récentes suggèrent que six des sept membres de cette famille, FXYD1 (phospholemman), FXYD2 (sous-unité γ de la Na,K-ATPase), FXYD3 (Mat-8), FXYD4 (CHIF), FXYD5 (Ric) et FXYD7, sont des sous-unités auxiliaires de la Na, K-ATPase régulant son activité de manière tissu et isoforme spécifique. Ces résultats soulignent la complexité de la régulation des ions Na+ et K+ par la Na,K-ATPase qui est nécessaire pour assurer les fonctions propres de différents tissus comme la réabsorption du Na+ par le rein, la contraction musculaire et l’excitabilité neuronale. De plus, une mutation dans FXYD2 a été liée à certains cas d’hypomagnésémie, suggérant que des perturbations de la régulation de la Na,KATPase par les protéines FXYD seraient impliquées dans des états physiopathologiques. Une meilleure compréhension de ce nouveau mécanisme de régulation de la Na,K-ATPase pourrait nous aider à mieux comprendre son rôle dans les états physiopathologiques. Dans cet article, nous discutons les données les plus récentes sur le rôle des protéines FXYD dans la modulation de la Na, K-ATPase. Members of the FXYD protein family are small membrane proteins which are characterized by an FXYD motif, two conserved glycines and a serine residue. FXYD proteins show a tissue-specific distribution. Recent evidence suggests that 6 out of 7 FXYD proteins, FXYD1 (phospholemman), FXYD2 (γ subunit of Na,K-ATPase), FXYD3 (Mat-8), FXYD4 (CHIF), FXYD5 (Ric) and FXYD7 associate with Na,K-ATPase and modulate its transport properties e.g. its Na+ and/or its K+ affinity in a distinct way. These results highlight the complex regulation of Na+ and K+ transport which is necessary to ensure proper tissue functions such as renal Na+-reabsorption, muscle contractility and neuronal excitability. Moreover, mutation of a conserved glycine residue into an arginine residue in FXYD2 has been linked to cases of human hypomagnesemia indicating that dysregulation of Na,K-ATPase by FXYD proteins may be implicated in pathophysiological states. A better characterization of this novel regulatory mechanism of Na,K-ATPase may help to better understand its role in physiological and pathophysiological conditions.
Pour citer ce document
Delprat, Benjamin ; Bibert, Stéphanie ; Geering, Käthi ; Les protéines FXYD : nouveaux régulateurs de la Na,K-ATPase, Med Sci (Paris), 2006, Vol. 22, N° 6-7; p. 633-638 ; DOI : 10.1051/medsci/20062267633



